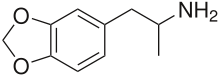
3,4-Metilenodioxianfetamina - 3,4-Methylenedioxyamphetamine
 | |
 | |
| Dados clínicos | |
|---|---|
| Vias de administração |
Oral, sublingual, insuflação, intravenosa |
| Código ATC | |
| Status legal | |
| Status legal | |
| Dados farmacocinéticos | |
| Metabolismo | Hepático ( CYP amplamente envolvido) |
| Excreção | Renal |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| ChEMBL | |
| Painel CompTox ( EPA ) | |
| ECHA InfoCard |
100.230.706 |
| Dados químicos e físicos | |
| Fórmula | C 10 H 13 N O 2 |
| Massa molar | 179,219 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
|
| |
3,4-Metilenodioxianfetamina (também conhecida como MDA e sass ) é uma droga empatogênica-entactogênica , psicoestimulante e psicodélica da família das anfetaminas, encontrada principalmente como droga recreativa . Em termos de farmacologia , o MDA atua mais importante como um agente liberador de serotonina-norepinefrina-dopamina (SNDRA). Na maioria dos países, a droga é uma substância controlada e sua posse e venda são ilegais.
O MDA raramente é procurado como uma droga recreativa em comparação com outras drogas da família das anfetaminas; entretanto, continua sendo uma droga importante e amplamente utilizada por ser um metabólito primário, produto da N-desalquilação hepática, do MDMA (ecstasy). Além disso, é comum encontrar MDA como um adulterant de MDMA ilicitamente produzido.
Usos
Médico
Atualmente, o MDA não tem uso médico aceito.
Recreativa
Embora ilegal, o MDA é comprado, vendido e usado como uma 'droga de amor' recreativa, devido ao aumento do humor e da empatia . Uma dose recreativa de MDA é algumas vezes citada como estando entre 100 e 160 mg.
Efeitos adversos
O MDA produz efeitos neurotóxicos serotonérgicos, que se acredita serem ativados pelo metabolismo inicial do MDA. Além disso, o MDA ativa uma resposta da neuroglia , embora isso diminua após o uso.
Overdose
Os sintomas de toxicidade aguda podem incluir agitação , sudorese , aumento da pressão arterial e frequência cardíaca , aumento dramático da temperatura corporal , convulsões e morte . A morte geralmente é causada por efeitos cardíacos e subsequente hemorragia cerebral ( derrame ).
Farmacologia
Farmacodinâmica
MDA é um substrato dos transportadores de serotonina , norepinefrina , dopamina e monoamina vesicular , bem como um agonista TAAR1 e, por essas razões, atua como um inibidor de recaptação e agente de liberação de serotonina , norepinefrina e dopamina (ou seja, é um SNDRA ). É também um agonista dos receptores 5-HT 2A , 5-HT 2B e 5-HT 2C da serotonina e mostra afinidade para os receptores α 2A - , α 2B - e α 2C -adrenérgicos e serotonina 5-HT 1A e Receptores 5-HT 7 .
O isômero óptico ( S ) do MDA é mais potente do que o isômero óptico ( R ) como psicoestimulante, possuindo maior afinidade pelos três transportadores de monoamina .
Em termos dos efeitos subjetivos e comportamentais do MDA, acredita-se que a liberação de serotonina é necessária para seus efeitos de empatógeno-entactogênio, a liberação de dopamina e norepinefrina é responsável por seus efeitos psicoestimulantes, a liberação de dopamina é necessária para seu efeito euforizante ( recompensador e viciante ) efeitos e agonismo direto do receptor 5-HT 2A da serotonina é o causador de seus efeitos psicodélicos.
Farmacocinética
A duração do medicamento foi relatada em cerca de 6 a 8 horas.
Química
MDA é uma fenetilamina metilenodioxilada substituída e um derivado de anfetamina . Em relação às outras fenetilaminas e anfetaminas, é o 3,4-metilenodioxi, derivado α-metil da β-feniletilamina , o derivado 3,4-metilenodioxi da anfetamina e o derivado N - desmetil do MDMA.
Sinônimos
Além de 3,4-metilenodioxianfetamina , o MDA também é conhecido por outros sinônimos químicos, como os seguintes:
- α-Metil-3,4-metilenodioxi-β-feniletilamina
- 1- (3,4-metilenodioxifenil) -2-propanamina
- 1- (1,3-benzodioxol-5-il) -2-propanamina
Síntese
O MDA é normalmente sintetizado a partir de óleos essenciais , como safrol ou piperonal . As abordagens comuns desses precursores incluem:
- A reacção de de safrol alceno grupo funcional com um halogéneo contendo ácido mineral seguido por alquilação da amina .
- Oxidação Wacker do safrol para produzir 3,4-metilenodioxifenilpropan-2-ona (MDP2P) seguida de aminação redutora ou via redução de sua oxima .
- Reação de Henry do piperonal com nitroetano seguida de redução do composto nitro .
- A reação de Darzens à heliotropina também foi realizada por J. Elks, et al. Isso dá MDP2P , que foi então submetido a uma reação de Leuckart.
Detecção em fluidos corporais
O MDA pode ser quantificado no sangue, plasma ou urina para monitorar o uso, confirmar um diagnóstico de envenenamento ou auxiliar na investigação forense de um trânsito ou outra violação criminal ou uma morte súbita. Alguns programas de rastreamento de abuso de drogas contam com amostras de cabelo, saliva ou suor. A maioria dos testes comerciais de triagem por imunoensaio de anfetamina apresentam reação cruzada significativa com o MDA e os principais metabólitos do MDMA, mas as técnicas cromatográficas podem distinguir facilmente e medir separadamente cada uma dessas substâncias. As concentrações de MDA no sangue ou na urina de uma pessoa que tomou apenas MDMA são, em geral, menos de 10% do medicamento original.
Derivados
O MDA constitui parte da estrutura central do protocilol agonista do receptor β-adrenérgico .
História
O MDA foi sintetizado pela primeira vez por C. Mannich e W. Jacobsohn em 1910. Foi ingerido pela primeira vez em julho de 1930 por Gordon Alles, que mais tarde licenciou a droga para Smith, Kline e French . O MDA foi usado pela primeira vez em testes em animais em 1939, e os testes em humanos começaram em 1941 na exploração de possíveis terapias para a doença de Parkinson . De 1949 a 1957, mais de 500 sujeitos humanos receberam MDA em uma investigação de seu uso potencial como antidepressivo e / ou anorexígeno por Smith, Kline e French . O Exército dos Estados Unidos também experimentou a droga, com o código EA-1298, enquanto trabalhava para desenvolver uma droga verdadeira ou agente incapacitante. Harold Blauer morreu em janeiro de 1953 após ser injetado por via intravenosa, sem seu conhecimento ou consentimento, com 450 mg da droga como parte do Projeto MKUltra . MDA foi patenteado como uma ataractic por Smith, Kline & French , em 1960, e como um anorexígeno sob o nome comercial "Amphedoxamine" em 1961. MDA começou a aparecer no recreativo de drogas cena por volta de 1963 a 1964. Foi então baratos e prontamente disponíveis como um produto químico de pesquisa de várias empresas de fornecimento científico. Vários pesquisadores, incluindo Claudio Naranjo e Richard Yensen , exploraram o MDA no campo da psicoterapia .
Sociedade e cultura
Nome
Quando o MDA estava em desenvolvimento como um medicamento farmacêutico em potencial, recebeu o nome não proprietário internacional (DCI) de tenanfetamina .
Status legal
Austrália
MDA é uma substância proibida de acordo com os Padrões de Venenos . Uma substância do cronograma 9 é listada como "Substâncias que podem ser abusadas ou mal utilizadas, cuja fabricação, posse, venda ou uso deve ser proibido por lei, exceto quando exigido para pesquisa médica ou científica, ou para fins analíticos, de ensino ou treinamento com aprovação da Comunidade e / ou Autoridades de Saúde Estaduais ou Territoriais. "
Estados Unidos
O MDA é uma substância controlada de Classe I nos Estados Unidos.
Pesquisar
Em 2010, a capacidade do MDA de invocar experiências místicas e alterar a visão em voluntários saudáveis foi estudada. O estudo concluiu que o MDA é uma "ferramenta potencial para investigar experiências místicas e percepção visual []".


