halogeneto de metal alcalino - Alkali metal halide
Halogenetos de metais alcalinos (também conhecidos como halogenetos de metais alcalinos ) são a família de compostos inorgânicos com a fórmula química MX, em que M é um metal alcalino e X é um halogéneo . Estes compostos são as fontes frequentemente comercialmente significativas destes metais e de halogenetos. O mais conhecido destes compostos é o cloreto de sódio , o sal de mesa .
Conteúdo
Estrutura
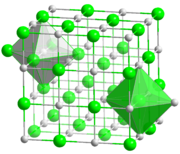
A maioria dos halogenetos de metais alcalinos cristalizar com as cúbicos de face centrada reticulados. Nesta estrutura ambos os metais e de halogenetos apresentam geometria de coordenação octaédrica , em que cada ião tem um número de coordenação de seis. Cloreto de césio, brometo, e iodeto de cristalização num cúbica de corpo centrado treliça que acomoda número de coordenação de oito para o catião de metal maior (e também o anião).
propriedades
Os halogenetos de metais alcalinos existem incolores cristalinos sólidos, embora, como pós moídos finamente aparecer branco. Eles derreter a uma temperatura elevada, geralmente várias centenas de graus para líquidos incolores. Seu alto ponto de fusão reflete suas altas energias de treliça . A temperaturas ainda mais elevadas, estes líquidos evaporar para dar gases compostas de moléculas diatómicas.
Estes compostos dissolvem-se em solventes polares para dar soluções iónicas que contêm aniões e catiões altamente solvatada. halogenetos alcalinos dissolver grandes quantidades de metal alcalino correspondente: césio é completamente miscíveis em todas as temperaturas acima do ponto de fusão.
O quadro abaixo fornece as ligações para cada um dos artigos individuais para estes compostos. Os números ao lado os compostos mostram a diferença electronegatividade entre os elementos com base na escala de Pauling . Quanto maior for o número, mais iónico o sólido é.
| Metais alcalinos | |||||||
|---|---|---|---|---|---|---|---|
| Lítio | Sódio | Potássio | Rubídio | Césio | |||
| Flúor | LiF (3,0) | NaF (3,1) | KF (3,2) | RBF (3,2) | CsF (3,3) | ||
| Cloro | LiCl (2,0) | De NaCl (2,1) | KCl (2,2) | RbCl (2.2) | CsCl (2,3) | ||
| Bromo | LiBr (1,8) | NaBr (1,9) | KBr (2,0) | RBBR (2,0) | CsBr (2,1) | ||
| Iodo | LiI (1,5) | Nal (1,6) | Kl (1,7) | RBI (1,7) | Csl (1,8) | ||
Referências
- ^ Greenwood, NN; & Earnshaw, A. (1997). Chemistry of the Elements (2a ed.), Oxford: Butterworth-Heinemann. ISBN 0-7506-3365-4 .
- ^ Wells, AF (1984) Química Inorgânica estrutural, Oxford: Clarendon Press. ISBN 0-19-855370-6 .
- ^ Huheey, James E .; Keiter, Ellen A .; Kieter, Richard L. (1993). Química inorgânica: princípios de estrutura e reactividade (4. ed.). Cambridge, Massachusetts [ua]: Harper. p. 377. ISBN 006042995X .
Outras leituras
| Este inorgânico composto relacionados com o artigo é um esboço . Você pode ajudar a Wikipédia expandindo-o . |