Tabelas periódicas alternativas - Alternative periodic tables
| Parte de uma série no |
| Tabela periódica |
|---|
Tabelas periódicas alternativas são tabulações de elementos químicos que diferem em sua organização da representação tradicional do sistema periódico .
Mais de mil foram concebidos, muitas vezes por razões didáticas , uma vez que nem todas as correlações entre os elementos químicos são efetivamente capturadas pela tabela periódica padrão.
Principais estruturas alternativas
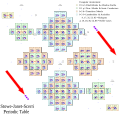
Tabela periódica à esquerda (Janet, 1928)
A tabela periódica esquerda de Charles Janet é a alternativa mais amplamente usada para a representação tradicional do sistema periódico. Organiza os elementos de acordo com um enchimento orbital idealizado (em vez de valência ). Por exemplo, os elementos Sc a Zn são mostrados como um bloco 3d implicando em ocupação orbital [Ar] 4s 2 3d x . (Embora Cr e Cu sejam exceções na fase gasosa, as configurações idealizadas não estão muito distantes do estado fundamental e a diferença de energia é pequena o suficiente para ser controlada pelo ambiente químico.)
| f 1 | f 2 | f 3 | f 4 | f 5 | f 6 | f 7 | f 8 | f 9 | f 10 | f 11 | f 12 | f 13 | f 14 | d 1 | d 2 | d 3 | d 4 | d 5 | d 6 | d 7 | d 8 | d 9 | d 10 | p 1 | p 2 | p 3 | p 4 | p 5 | p 6 | s 1 | s 2 | |
| 1s | H | Ele | ||||||||||||||||||||||||||||||
| 2s | Li | Ser | ||||||||||||||||||||||||||||||
| 2p 3s | B | C | N | O | F | Ne | N / D | Mg | ||||||||||||||||||||||||
| 3p 4s | Al | Si | P | S | Cl | Ar | K | Ca | ||||||||||||||||||||||||
| 3d 4p 5s | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | Como | Se | Br | Kr | Rb | Sr | ||||||||||||||
| 4d 5p 6s | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | CD | No | Sn | Sb | Te | eu | Xe | Cs | BA | ||||||||||||||
| 4f 5d 6p 7s | La | Ce | Pr | WL | PM | Sm | Eu | D'us | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | C | Ré | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | No | Rn | Fr | Ra |
| 5f 6d 7p 8s | Ac | º | Pa | você | Np | Pu | Sou | Cm | Bk | Cf | Es | Fm | Md | Não | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | 119 | 120 |
| bloco f | bloco d | bloco p | bloco s | |||||||||||||||||||||||||||||
Em comparação com o layout comum, a tabela da etapa esquerda tem estas alterações:
- O hélio é colocado no grupo 2 (não no grupo 18).
- Os grupos 1 e 2 (o bloco s), incluindo os elementos 119 e 120 no período estendido 8, são movidos para o lado direito da tabela.
- O bloco s é deslocado uma linha para cima e todos os elementos que não estão no bloco estão agora uma linha abaixo da tabela padrão. Por exemplo, a maior parte da quarta linha da tabela padrão é a quinta linha desta tabela.
No resultado, a ordem ainda é consistente pelo número atômico ( Z ), 1–120.
Espiral bidimensional (Benfey, 1964)
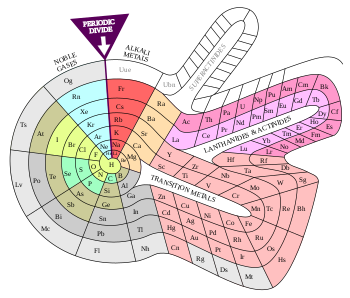
Na tabela periódica de Theodor Benfey , os elementos formam uma espiral bidimensional, partindo do hidrogênio e dobrando-se em torno de duas penínsulas, os metais de transição , os lantanídeos e os actinídeos . A superactinide ilha já está entalhado em. A tabela Benfey tem alguns aspectos exclusivos que muito poucas mesas representam. Um exemplo disso é a localização do hidrogênio na espiral. Na maioria das tabelas, o hidrogênio parece ser o "estranho". A razão para isso é porque o hidrogênio, embora tenha a mesma configuração de elétrons de valência que os metais alcalinos , tem as propriedades de um halogênio . A mesa Benfey contorna esse dilema expandindo a caixa de hidrogênio em torno dos metais alcalinos e dos halogênios.
Tridimensional, semelhante a uma flor (Paul Giguère, 1966)
A tabela periódica 3-D de Paul Giguère consiste em quatro outdoors conectados com os elementos escritos na frente e no verso. O primeiro outdoor tem os elementos do grupo 1 na frente e os elementos do grupo 2 na parte traseira, com hidrogênio e hélio totalmente omitidos. Em um ângulo de 90 °, o segundo outdoor contém os grupos 13 a 18 na frente e atrás. Dois outros painéis, cada um fazendo ângulos de 90 °, contêm os outros elementos.
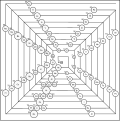
Tridimensional, físico (Timothy Stowe, 1986)
A tabela periódica do físico de Timothy Stowe é tridimensional com os três eixos representando o número quântico principal , o número quântico orbital e o número quântico magnético orbital . O hélio é novamente um elemento do grupo 2 .
Elementos repetidos (Ronald L. Rich, 2005)
Ronald L. Rich propôs uma tabela periódica onde os elementos aparecem mais de uma vez quando apropriado. Ele observa que o hidrogênio compartilha propriedades com elementos do grupo 1 com base na valência , com elementos do grupo 17 porque o hidrogênio é um não-metal, mas também com o grupo de carbono com base em semelhanças na ligação química com metais de transição e uma eletronegatividade semelhante . Nessa versão da tabela periódica, o carbono e o silício também aparecem no mesmo grupo do titânio e do zircônio .
ADOMAH (Valery Tsimmerman, 2006)
A tabela ADOMAH é uma adaptação da tabela da etapa esquerda. Cada coluna estritamente vertical da tabela tem o mesmo valor do número quântico principal n . Por exemplo, n = 3 para Fe. Cada bloco de elementos tem o mesmo valor do número quântico secundário l. Por exemplo, l = 2 para Fe. Cada entrada de elemento junto com todos os elementos anteriores corresponde à configuração eletrônica desse elemento (com 20 exceções de 118 elementos conhecidos). Por exemplo, a configuração eletrônica do Fe é determinada começando em H, que é 1s 1 , e contando na ordem dos números atômicos. Isso dá uma configuração de 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 ou, resumidamente, [Ar] 4s 2 3d 6 .
Os quatro blocos da tabela Adomah podem ser reorganizados de modo que se encaixem, espaçados equidistantemente, dentro de um tetraedro regular . Este último, por sua vez, se encaixa em um cubo.
Variantes do layout clássico
Da tabela periódica original de Mendeleev, os elementos foram basicamente organizados por valência (grupos em colunas) e a repetição nela (períodos em linhas). Com o passar dos anos e com as descobertas na estrutura atômica, esse esquema foi ajustado e expandido, mas não mudou como princípio.

A tabela periódica mais antiga é a tabela de formato curto (colunas I-VIII) de Dmitri Mendeleev , que mostra parentesco químico secundário. Por exemplo, os metais alcalinos e os metais de cunhagem (cobre, prata, ouro) estão na mesma coluna porque ambos os grupos tendem a ter uma valência de um. Este formato ainda é usado por muitos, como mostrado por esta tabela de forma abreviada russa contemporânea , que inclui todos os elementos e nomes de elementos até o roentgênio .
HG Deming usou a chamada tabela periódica longa (18 colunas) em seu livro "General Chemistry", que apareceu nos Estados Unidos pela primeira vez em 1923 (Wiley), e foi o primeiro a designar as duas primeiras e as cinco últimas grupos principais com a notação "A" e os grupos de transição intermediários com a notação "B".
A numeração foi escolhida de forma que os óxidos característicos dos grupos B correspondessem aos dos grupos A. Os grupos do ferro, cobalto e níquel não foram designados nem A nem B. O grupo dos gases nobres foi originalmente anexado (por Deming) ao lado esquerdo da tabela periódica. O grupo foi posteriormente mudado para o lado direito e geralmente rotulado como grupo VIIIA.
Extensão da tabela periódica
Na tabela periódica estendida , sugerida por Glenn T. Seaborg em 1969, ainda elementos desconhecidos são incluídos até o número atômico 168. Períodos teóricos acima do período regular 7 são adicionados.
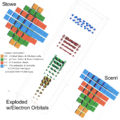
No campo de pesquisa de superátomos , aglomerados de átomos têm propriedades de átomos individuais de outro elemento. Sugere-se estender a tabela periódica com uma segunda camada a ser ocupada com esses compostos do cluster . A última adição a esta mesa de vários andares é o cluster de alumínio íon Al-
7, que se comporta como um átomo de germânio multivalente .
Em outubro de 2020, os cientistas relataram uma forma não empírica de apresentar os números de Mendeleev e de organizar o espaço químico.
Galeria
Referências
Leitura adicional
- Uma revisão de 1974 das tabelas então conhecidas é considerada uma obra definitiva sobre o tema: Mazurs, EG Representações Gráficas do Sistema Periódico durante Cem Anos. Alabama; University of Alabama Press, 1974, ISBN 0-8173-3200-6 .
- Hjørland, Birger (2011). A tabela periódica e a filosofia da classificação . Knowledge Organization, 38 (1), 9–21.
links externos
- Representando a Tabela Periódica de Diferentes Maneiras, um site com curadoria da Rede de Conhecimento da Associação de Alunos da Universidade Estadual de Michigan
- Tabela periódica espiral moderna de Robert Harrison
- Tabela Periódica do Passo Esquerdo de Janet
- Correcção para físico tabela periódica oferecido por Jeries Rihani como Meitnério ocupa a posição que Hassium deve ter.
- Um artigo com fio sobre tabelas periódicas alternativas
- Uma seleção de tabelas periódicas
- http://periodicspiral.com/ organiza a tabela periódica em uma espiral (hexagonal).
- Rotaperiod.com Uma nova tabela periódica.
- Observe a topologia de camiseta da espiral Z.
- Nova Tabela Periódica dos Elementos, em uma disposição periódica quadrada-triangular.
- Tabela Periódica baseada em configurações eletrônicas
- Banco de dados de tabelas periódicas
- Fractal Periódico dos Elementos
- Bob Doyle Tabela Periódica dos Elementos Um reagrupamento por propriedades usadas para explicar melhor o agrupamento de elétrons
- Site de Eric Scerri sobre a tabela periódica
- Tabela Periódica do Earth Scientist
- ^ Kauffman, George B. (1975). "Representações gráficas do sistema periódico durante cem anos (Mazurs, Edward G.)" . Journal of Chemical Education . 52 (9): A436. doi : 10.1021 / ed052pA436.1 .