Hidreto de alumínio - Aluminium hydride

|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Hidreto de alumínio |
|
|
Nome IUPAC sistemático
Alumane |
|
| Outros nomes
Alane
Hidreto alumínico |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.029.139 |
| 245 | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| AlH 3 | |
| Massa molar | 29,99 g / mol |
| Aparência | cristais sólidos cristalinos brancos, não voláteis, altamente polimerizados, em forma de agulha |
| Densidade | 1,477 g / cm 3 , sólido |
| Ponto de fusão | 150 ° C (302 ° F; 423 K) começa a decompor a 105 ° C (221 ° F) |
| reage | |
| Solubilidade | solúvel em éter reage em etanol |
| Termoquímica | |
|
Capacidade de calor ( C )
|
40,2 J / mol K |
|
Entropia molar padrão ( S |
30 J / mol K |
| -11,4 kJ / mol | |
|
Energia livre de Gibbs (Δ f G ˚)
|
46,4 kJ / mol |
| Compostos relacionados | |
|
Compostos relacionados
|
Hidreto de alumínio e lítio , diborano |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O hidreto de alumínio (também conhecido como alano ou alumane) é um composto inorgânico com a fórmula Al H 3 . Apresenta-se como um sólido branco e pode ser tingido de cinza com tamanho de partícula e níveis de impureza decrescentes. Dependendo das condições de síntese, a superfície do alano pode ser passivada com uma fina camada de óxido e / ou hidróxido de alumínio. Alane e seus derivados são usados como agentes redutores em síntese orgânica .
Estrutura
Alane é um polímero. Portanto, sua fórmula às vezes é representada pela fórmula (AlH 3 ) n . Alane forma numerosos polimorfos , que são denominados α-alano, α'-alano, β-alano, γ-alano, δ-alano, ε-alano e ζ-alano. α-Alane tem uma morfologia cúbica ou romboédrica, enquanto α'-alane forma cristais em forma de agulha e γ-alane forma um feixe de agulhas fundidas. Alane é solúvel em tetrahidrofurano (THF) e éter. A taxa de precipitação do alano sólido a partir do éter varia com o método de preparação.
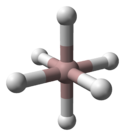
A estrutura cristalina do α-alano foi determinada e apresenta átomos de alumínio rodeados por 6 átomos de hidrogênio que se conectam a 6 outros átomos de alumínio. As distâncias Al-H são todas equivalentes (172pm) e o ângulo Al-H-Al é 141 °.
 |
 |

|
| Célula unitária α-AlH 3 | Coordenação de Al | Coordenação H |
α-Alane é o polimorfo mais estável termicamente. β-alano e γ-alano são produzidos juntos e convertidos em α-alano após aquecimento. δ, ε e θ-alano são produzidos em ainda outras condições de cristalização. Embora sejam menos estáveis termicamente, os polimorfos δ, ε e θ não se convertem em α-alano durante o aquecimento.
Formas moleculares de alane
O AlH 3 monomérico foi isolado em baixa temperatura em uma matriz sólida de gás nobre e mostrou ser plano. O dímero Al 2 H 6 foi isolado em hidrogênio sólido. É isoestrutural com diborano (B 2 H 6 ) e digalano (Ga 2 H 6 ).
Preparação
Hidretos de alumínio e vários complexos dos mesmos são conhecidos há muito tempo. Sua primeira síntese foi publicada em 1947, e uma patente para a síntese foi concedida em 1999. O hidreto de alumínio é preparado tratando o hidreto de alumínio e lítio com tricloreto de alumínio . O procedimento é complicado: atenção deve ser dada à remoção do cloreto de lítio .
- 3 LiAlH 4 + AlCl 3 → 4 AlH 3 + 3 LiCl
A solução de éter de alano requer uso imediato, porque o material polimérico precipita rapidamente como um sólido. Sabe-se que as soluções de hidreto de alumínio se degradam após 3 dias. O hidreto de alumínio é mais reativo do que LiAlH 4 .
Existem vários outros métodos para a preparação de hidreto de alumínio:
- 2 LiAlH 4 + BeCl 2 → 2 AlH 3 + Li 2 BeH 2 Cl 2
- 2 LiAlH 4 + H 2 SO 4 → 2 AlH 3 + Li 2 SO 4 + 2 H 2
- 2 LiAlH 4 + ZnCl 2 → 2 AlH 3 + 2 LiCl + ZnH 2
- 2 LiAlH 4 + I 2 → 2 AlH 3 + 2 LiI + H 2
Síntese eletroquímica
Vários grupos mostraram que alane pode ser produzido eletroquimicamente . Diferentes métodos de produção de alano eletroquímico foram patenteados. A geração eletroquímica de alano evita impurezas de cloreto. Dois mecanismos possíveis são discutidos para a formação de alano na célula eletroquímica de Clasen contendo THF como solvente, hidreto de alumínio e sódio como eletrólito, um ânodo de alumínio e um fio de ferro (Fe) submerso em mercúrio (Hg) como cátodo. O sódio forma um amálgama com o cátodo de Hg evitando reações colaterais e o hidrogênio produzido na primeira reação pode ser capturado e reagido de volta com o amálgama de mercúrio de sódio para produzir hidreto de sódio. O sistema de Clasen não resulta em perda de material inicial. Para ânodos insolúveis, ocorre a reação 1, enquanto para ânodos solúveis, a dissolução anódica é esperada de acordo com a reação 2:
- AlH 4 - - e - → AlH 3 · nTHF + 1 ⁄ 2 H 2
- 3AlH 4 - + Al - 3e - → 4AlH 3 · nTHF
Na reação 2, o ânodo de alumínio é consumido, limitando a produção de hidreto de alumínio para uma determinada célula eletroquímica.
A cristalização e recuperação de hidreto de alumínio a partir de alano gerado eletroquimicamente foi demonstrada.
Hidrogenação de alta pressão de metal de alumínio
α-AlH 3 pode ser produzido por hidrogenação de alumínio metálico a 10GPa e 600 ° C (1.112 ° F). A reação entre o hidrogênio liquefeito produz α-AlH 3 que pode ser recuperado em condições ambientais.
Reações
Formação de adutos com bases de Lewis
AlH 3 forma facilmente adutos com bases de Lewis fortes . Por exemplo, os complexos 1: 1 e 1: 2 se formam com a trimetilamina . O complexo 1: 1 é tetraédrico na fase gasosa, mas na fase sólida é dimérico com centros de hidrogênio em ponte, (NMe 3 Al (μ-H)) 2 . O complexo 1: 2 adota uma estrutura trigonal bipiramidal . Alguns adutos (por exemplo, dimetiletilamina alano, NMe 2 Et · AlH 3 ) se decompõem termicamente para dar alumínio metálico e podem ter uso em aplicações MOCVD .
Seu complexo com o éter dietílico se forma de acordo com a seguinte estequiometria:
- AlH 3 + (C 2 H 5 ) 2 O → H 3 Al · O (C 2 H 5 ) 2
A reação com hidreto de lítio em éter produz hidreto de alumínio e lítio :
- AlH 3 + LiH → LiAlH 4
Redução de grupos funcionais
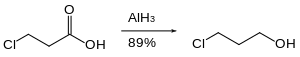
Na química orgânica, o hidreto de alumínio é usado principalmente para a redução de grupos funcionais. Em muitos aspectos, a reatividade do hidreto de alumínio é semelhante à do hidreto de alumínio e lítio . O hidreto de alumínio reduzirá aldeídos , cetonas , ácidos carboxílicos , anidridos , cloretos de ácido , ésteres e lactonas a seus álcoois correspondentes . Amidas , nitrilas e oximas são reduzidas às suas aminas correspondentes .
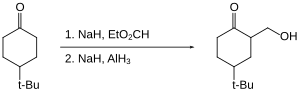
Em termos de seletividade de grupo funcional, alano difere de outros reagentes de hidreto. Por exemplo, na seguinte redução de ciclohexanona, o hidreto de alumínio e lítio dá uma razão trans: cis de 1,9: 1, enquanto o hidreto de alumínio dá uma razão trans: cis de 7,3: 1.
Alane permite a hidroximetilação de certas cetonas (que é a substituição de CH por C-CH 2 OH na posição alfa ). A cetona em si não é reduzida, pois é "protegida" como seu enolato.
Os organohaletos são reduzidos lentamente ou não são reduzidos pelo hidreto de alumínio. Portanto, grupos funcionais reativos, como ácidos carboxílicos, podem ser reduzidos na presença de haletos.
Os grupos nitro não são reduzidos pelo hidreto de alumínio. Da mesma forma, o hidreto de alumínio pode realizar a redução de um éster na presença de grupos nitro.
O hidreto de alumínio pode ser usado na redução de acetais a dióis parcialmente protegidos.
O hidreto de alumínio também pode ser usado na reação de abertura do anel de epóxido, conforme mostrado abaixo.
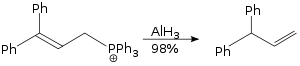
A reação de rearranjo alílico realizada usando hidreto de alumínio é uma reação S N 2 , e não é estericamente exigente.
O hidreto de alumínio ainda reduz o dióxido de carbono a metano sob aquecimento:
- 4 AlH 3 + 3 CO 2 → 3 CH 4 + 2 Al 2 O 3
Hidroaluminação
Foi demonstrado que o hidreto de alumínio adiciona aos álcoois propargílicos . Usado junto com o tetracloreto de titânio , o hidreto de alumínio pode adicionar ligações duplas . A hidroboração é uma reação semelhante.
Combustível
Em sua forma passivada, Alane é um candidato ativo para armazenar hidrogênio e pode ser usado para geração de energia eficiente por meio de aplicações de células de combustível, incluindo células de combustível e veículos elétricos e outras aplicações de energia leve. AlH 3 contém até 10% de hidrogênio em peso, correspondendo a 148g H 2 / L, ou duas vezes a densidade de hidrogênio do H 2 líquido . Em sua forma não passivada, alane também é um aditivo de combustível de foguete promissor , capaz de entregar ganhos de eficiência de impulso de até 10%.
Precauções
Alane não é espontaneamente inflamável. Deve ser tratado de forma semelhante ao de outros agentes redutores de hidreto de metal complexo, como hidreto de alumínio e lítio. Alane se decompõe no ar e na água, embora a passivação diminua muito a taxa de decomposição. O alano passivado é geralmente atribuído a uma classificação de perigo de 4.3 (produtos químicos que, em contato com a água, emitem gases inflamáveis).
Referências
links externos
- Hidreto de alumínio no banco de dados químico da EnvironmentalChemistry.com
- Armazenamento de hidrogênio do Laboratório Nacional de Brookhaven
- Triidrido de alumínio em elementos da Web