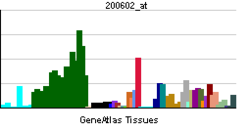
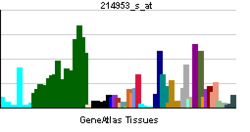
Proteína precursora de beta amilóide - Amyloid-beta precursor protein

A proteína precursora de beta-amilóide ( APP ) é uma proteína de membrana integral expressa em muitos tecidos e concentrada nas sinapses dos neurônios . Ele funciona como um receptor de superfície celular e tem sido implicado como um regulador da formação de sinapses, plasticidade neural , atividade antimicrobiana e exportação de ferro . É codificado pelo gene APP e regulado pela apresentação do substrato . APP é mais conhecido como a molécula precursora cuja proteólise gera beta amilóide (Aβ), um polipeptídeo contendo 37 a 49 resíduos de aminoácidos , cuja forma fibrilar amilóide é o principal componente das placas amilóides encontradas nos cérebros de pacientes com doença de Alzheimer .
Genética
A proteína precursora de beta-amilóide é uma proteína antiga e altamente conservada . Em humanos , o gene APP está localizado no cromossomo 21 e contém 18 exons que medem 290 quilobases . Várias isoformas de splicing alternativas de APP foram observadas em humanos, variando em comprimento de 639 a 770 aminoácidos, com certas isoformas preferencialmente expressas em neurônios; alterações na proporção neuronal dessas isoformas têm sido associadas à doença de Alzheimer. Proteínas homólogas foram identificadas em outros organismos, como Drosophila (moscas da fruta), C. elegans (lombrigas) e todos os mamíferos . A região beta amilóide da proteína, localizada no domínio que atravessa a membrana, não é bem conservada entre as espécies e não tem nenhuma conexão óbvia com as funções biológicas de estado nativo de APP .
Mutações em regiões críticas da proteína precursora de amilóide, incluindo a região que gera amilóide beta (Aβ), causam suscetibilidade familiar à doença de Alzheimer. Por exemplo, verificou-se que várias mutações fora da região Aβ associadas à doença de Alzheimer familiar aumentam dramaticamente a produção de Aβ.
Uma mutação (A673T) no gene APP protege contra a doença de Alzheimer. Esta substituição é adjacente ao local de clivagem da beta secretase e resulta em uma redução de 40% na formação de beta amilóide in vitro.
Estrutura


Uma série de domínios estruturais distintos, amplamente dobrados de forma independente , foram identificados na sequência de APP. A região extracelular, muito maior do que a região intracelular, é dividida nos domínios E1 e E2, ligados por um domínio ácido (AcD); E1 contém dois subdomínios, incluindo um domínio semelhante ao fator de crescimento (GFLD) e um domínio de ligação de cobre (CuBD) interagindo fortemente. Um domínio inibidor de serina protease, ausente da isoforma diferencialmente expresso no cérebro, é encontrado entre a região ácida e o domínio E2. A estrutura cristalina completa do APP ainda não foi resolvida; no entanto, os domínios individuais foram cristalizados com sucesso, o domínio semelhante ao fator de crescimento , o domínio de ligação de cobre , o domínio E1 completo e o domínio E2.
Processamento pós-tradução
APP sofre extensa modificação pós-tradução, incluindo glicosilação , fosforilação , sialilação e sulfatação de tirosina , bem como muitos tipos de processamento proteolítico para gerar fragmentos de peptídeo. É comumente clivado por proteases da família da secretase ; A alfa secretase e a beta secretase removem quase todo o domínio extracelular para liberar fragmentos carboxi-terminais ancorados na membrana que podem estar associados à apoptose . A clivagem pela gama secretase dentro do domínio que abrange a membrana após a clivagem da beta-secretase gera o fragmento beta-amilóide; gama secretase é um grande complexo de múltiplas subunidades cujos componentes ainda não foram totalmente caracterizados, mas incluem a presenilina , cujo gene foi identificado como um importante fator de risco genético para Alzheimer.
O processamento amiloidogênico da APP tem sido associado à sua presença em jangadas lipídicas . Quando as moléculas de APP ocupam uma região de jangada lipídica da membrana, elas são mais acessíveis e clivadas diferencialmente pela beta secretase, enquanto as moléculas de APP fora de uma jangada são clivadas diferencialmente pela alfa secretase não amiloidogênica. A atividade da gama secretase também foi associada a jangadas lipídicas. O papel do colesterol na manutenção do lipid raft foi citado como uma provável explicação para as observações de que o colesterol alto e o genótipo da apolipoproteína E são os principais fatores de risco para a doença de Alzheimer.
Função biológica
Embora o papel biológico nativo da APP seja de interesse óbvio para a pesquisa de Alzheimer, um entendimento completo permaneceu ilusório.
Formação e reparo sináptico
O papel mais comprovado da APP é na formação e reparo sináptico; sua expressão é regulada positivamente durante a diferenciação neuronal e após lesão neural. Os papéis na sinalização celular , potencialização de longo prazo e adesão celular foram propostos e apoiados por pesquisas ainda limitadas. Em particular, as semelhanças no processamento pós-tradução convidaram a comparações para o papel de sinalização da proteína do receptor de superfície Notch .
Os camundongos knockout para APP são viáveis e têm efeitos fenotípicos relativamente menores , incluindo diminuição da potenciação de longo prazo e perda de memória sem perda geral de neurônios. Por outro lado, camundongos transgênicos com expressão de APP regulada positivamente também foram relatados para mostrar potenciação prejudicada de longo prazo.
A inferência lógica é que, porque Aβ se acumula excessivamente na doença de Alzheimer, seu precursor, APP, também estaria elevado. No entanto, os corpos celulares neuronais contêm menos APP em função de sua proximidade com as placas amilóides. Os dados indicam que este déficit em APP resulta de um declínio na produção ao invés de um aumento na catálise. A perda de APP de um neurônio pode afetar déficits fisiológicos que contribuem para a demência.
Recombinação somática
Nos neurônios do cérebro humano , a recombinação somática ocorre com frequência no gene que codifica a APP. Neurônios de indivíduos com doença de Alzheimer esporádica apresentam maior diversidade do gene APP devido à recombinação somática do que neurônios de indivíduos saudáveis.
Transporte neuronal anterógrado
As moléculas sintetizadas nos corpos celulares dos neurônios devem ser transportadas para fora, para as sinapses distais. Isso é realizado por meio de transporte anterógrado rápido . Verificou-se que o APP pode mediar a interação entre carga e cinesina e, assim, facilitar esse transporte. Especificamente, uma curta sequência de 15 aminoácidos do peptídeo do terminal carboxi citoplasmático é necessária para a interação com a proteína motora.
Além disso, foi demonstrado que a interação entre APP e cinesina é específica para a sequência peptídica de APP. Em uma experiência recente envolvendo o transporte de grânulos coloridos conjugados com peptídeo , os controles foram conjugados a um único aminoácido, glicina , de modo que exibam o mesmo grupo de ácido carboxílico terminal que o APP sem a sequência de 15 aminoácidos interveniente mencionada acima. As contas de controle não eram móveis, o que demonstrou que a porção terminal COOH dos peptídeos não é suficiente para mediar o transporte.
Exportação de ferro
Uma perspectiva diferente sobre a doença de Alzheimer é revelada por um estudo em camundongos que descobriu que a APP possui atividade ferroxidase semelhante à ceruloplasmina , facilitando a exportação de ferro por meio da interação com a ferroportina ; parece que esta atividade é bloqueada pelo zinco aprisionado pelo Aβ acumulado na doença de Alzheimer. Foi demonstrado que um único polimorfismo de nucleotídeo no 5'UTR do mRNA de APP pode interromper sua tradução.
A hipótese de que a APP tem atividade ferroxidase em seu domínio E2 e facilita a exportação de Fe (II) é possivelmente incorreta, uma vez que o sítio de ferroxidase proposto de APP localizado no domínio E2 não tem atividade ferroxidase.
Como o APP não possui atividade de ferroxidase dentro de seu domínio E2, o mecanismo de efluxo de ferro modulado por APP da ferroportina está sob escrutínio. Um modelo sugere que a APP atua para estabilizar a proteína ferroportina de efluxo de ferro na membrana plasmática das células, aumentando assim o número total de moléculas de ferroportina na membrana. Esses transportadores de ferro podem então ser ativados por ferroxidases de mamíferos conhecidas (ou seja, ceruloplasmina ou hepestina).
Regulação hormonal
A proteína precursora de amiloide-β (AβPP), e todas as secretetases associadas, são expressas no início do desenvolvimento e desempenham um papel fundamental na endocrinologia da reprodução - com o processamento diferencial de AβPP por secretetases que regulam a proliferação de células-tronco embrionárias humanas (hESC) também como sua diferenciação em células precursoras neurais (NPC). O hormônio da gravidez gonadotrofina coriônica humana (hCG) aumenta a expressão de AβPP e proliferação de hESC, enquanto a progesterona direciona o processamento de AβPP para a via não amiloidogênica, que promove a diferenciação de hESC em NPC.
AβPP e seus produtos de clivagem não promovem a proliferação e diferenciação de neurônios pós-mitóticos; em vez disso, a superexpressão de AβPP de tipo selvagem ou mutante em neurônios pós-mitóticos induz a morte apoptótica após sua reentrada no ciclo celular . Postula-se que a perda de esteróides sexuais (incluindo progesterona), mas a elevação do hormônio luteinizante , o equivalente adulto de hCG, pós- menopausa e durante a andropausa, conduz a produção de β-amiloide e a reentrada de neurônios pós-mitóticos no ciclo celular .
Interações
Demonstrou-se que a proteína precursora de amiloide interage com:
APP interage com reelin , uma proteína implicada em uma série de distúrbios cerebrais, incluindo a doença de Alzheimer.
Referências
Leitura adicional
- Beyreuther K, Pollwein P, Multhaup G, Mönning U, König G, Dyrks T, Schubert W, Masters CL (setembro 1993). "Regulação e expressão do precursor da proteína amilóide beta / A4 de Alzheimer na saúde, doença e síndrome de Down". Anais da Academia de Ciências de Nova York . 695 (1 Transdução): 91–102. doi : 10.1111 / j.1749-6632.1993.tb23035.x . PMID 8239320 . S2CID 22058428 .
- Straub JE, Guevara J, Huo S, Lee JP (junho de 2002). "Simulações dinâmicas de longo tempo: explorando as vias de dobramento de um peptídeo abeta amilóide de Alzheimer". Contas de pesquisa química . 35 (6): 473–81. doi : 10.1021 / ar010031e . PMID 12069633 .
- Annaert W, De Strooper B (2003). "Uma perspectiva biológica celular na doença de Alzheimer". Revisão Anual de Biologia Celular e do Desenvolvimento . 18 (1): 25–51. doi : 10.1146 / annurev.cellbio.18.020402.142302 . PMID 12142279 .
- Koo EH (novembro de 2002). "A proteína precursora beta-amilóide (APP) e a doença de Alzheimer: o rabo abana o cão?" . Traffic . 3 (11): 763–70. doi : 10.1034 / j.1600-0854.2002.31101.x . PMID 12383342 . S2CID 40411806 .
- Van Nostrand WE, Melchor JP, Romanov G, Zeigler K, Davis J (novembro de 2002). "Efeitos patogênicos das mutações da angiopatia amilóide cerebral no precursor da proteína beta amilóide". Anais da Academia de Ciências de Nova York . 977 (1): 258–65. Bibcode : 2002NYASA.977..258N . doi : 10.1111 / j.1749-6632.2002.tb04824.x . PMID 12480759 . S2CID 22567664 .
- Ling Y, Morgan K, Kalsheker N (novembro de 2003). "Proteína precursora amilóide (APP) e a biologia do processamento proteolítico: relevância para a doença de Alzheimer". The International Journal of Biochemistry & Cell Biology . 35 (11): 1505–35. doi : 10.1016 / S1357-2725 (03) 00133-X . PMID 12824062 .
- Kerr ML, Small DH (abril de 2005). "Domínio citoplasmático do precursor da proteína beta-amilóide da doença de Alzheimer: função, regulação da proteólise e implicações para o desenvolvimento de drogas". Journal of Neuroscience Research . 80 (2): 151–9. doi : 10.1002 / jnr.20408 . PMID 15672415 . S2CID 31985212 .
- Maynard CJ, Bush AI, Masters CL, Cappai R, Li QX (junho de 2005). "Metals and amyloid-beta in Alzheimer's disease" . International Journal of Experimental Pathology . 86 (3): 147–59. doi : 10.1111 / j.0959-9673.2005.00434.x . PMC 2517409 . PMID 15910549 .
- Tickler AK, Wade JD, Separovic F (agosto de 2005). O papel dos peptídeos Abeta na doença de Alzheimer ". Letras de proteínas e peptídeos . 12 (6): 513–9. doi : 10.2174 / 0929866054395905 . PMID 16101387 .
- Reinhard C, Hébert SS, De Strooper B (dezembro de 2005). "A proteína precursora de beta-amilóide: integrando a estrutura com a função biológica" . The EMBO Journal . 24 (23): 3996–4006. doi : 10.1038 / sj.emboj.7600860 . PMC 1356301 . PMID 16252002 .
- Watson D, Castaño E, Kokjohn TA, Kuo YM, Lyubchenko Y, Pinsky D, Connolly ES, Esh C, Luehrs DC, Stine WB, Rowse LM, Emmerling MR, Roher AE (dezembro de 2005). "Características físico-químicas da Abeta oligomérica solúvel e seu papel patológico na doença de Alzheimer". Pesquisa Neurológica . 27 (8): 869–81. doi : 10.1179 / 016164105X49436 . PMID 16354549 . S2CID 25687818 .
- Calinisan V, Gravem D, Chen RP, Brittin S, Mohandas N, Lecomte MC, Gascard P (2006). "Novos insights sobre funções potenciais para a superfamília das proteínas 4.1 das proteínas no epitélio renal" . Fronteiras em Biociências . 11 (1): 1646–66. doi : 10.2741 / 1911 . PMID 16368544 .
- Vetrivel KS, Thinakaran G (janeiro de 2006). "Processamento amiloidogênico da proteína precursora beta-amilóide em compartimentos intracelulares". Neurology . 66 (2 Suplemento 1): S69–73. doi : 10.1212 / 01.wnl.0000192107.17175.39 . PMID 16432149 . S2CID 35965729 .
- Gallo C, Orlassino R, Vineis C (fevereiro de 2006). "[Hemorragias intraparenquimais recorrentes em um paciente com angiopatia amiloidótica cerebral: descrição de um caso de autópsia]". Pathologica . 98 (1): 44–7. PMID 16789686 .
- Coulson EJ (agosto de 2006). "Será que o receptor de neurotrofina p75 medeia a toxicidade induzida por Abeta na doença de Alzheimer?" . Journal of Neurochemistry . 98 (3): 654–60. doi : 10.1111 / j.1471-4159.2006.03905.x . PMID 16893414 . S2CID 20879380 .
- Menéndez-González M, Pérez-Pinera P, Martínez-Rivera M, Calatayud MT, Blázquez Menes B (2006). "Processamento de APP e envolvimento do domínio APP-KPI na cascata amilóide". Doenças Neuro-Degenerativas . 2 (6): 277–83. doi : 10.1159 / 000092315 . PMID 16909010 . S2CID 45002038 .
- Neve RL, McPhie DL (abril de 2007). "Disfunção da sinalização da proteína precursora amilóide em neurônios leva à síntese de DNA e apoptose" . Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease . 1772 (4): 430–7. doi : 10.1016 / j.bbadis.2006.10.008 . PMC 1862818 . PMID 17113271 .
- Chen X, Stern D, Yan SD (dezembro de 2006). "Disfunção mitocondrial e doença de Alzheimer". Current Alzheimer Research . 3 (5): 515–20. doi : 10.2174 / 156720506779025215 . PMID 17168650 .
- Caltagarone J, Jing Z, Bowser R (abril de 2007). "As adesões focais regulam a sinalização Abeta e a morte celular na doença de Alzheimer" . Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease . 1772 (4): 438–45. doi : 10.1016 / j.bbadis.2006.11.007 . PMC 1876750 . PMID 17215111 .
- Wolfe MS (fevereiro de 2007). “Quando a perda é ganho: a função proteolítica da presenilina reduzida leva ao aumento de Abeta42 / Abeta40. Ponto de discussão sobre o papel das mutações da presenilina na doença de Alzheimer” . Relatórios EMBO . 8 (2): 136–40. doi : 10.1038 / sj.embor.7400896 . PMC 1796780 . PMID 17268504 .
links externos
- Artigo GeneReviews / NCBI / NIH / UW sobre Doença de Alzheimer Familiar de Início Precoce
- Amilóide + Proteína + Precursor na Biblioteca Nacional de Medicina dos EUA. Cabeçalhos de Assuntos Médicos (MeSH)
- Gene Entrez: proteína precursora de beta amilóide APP (A4) (peptidase nexin-II, doença de Alzheimer)
- Localização do genoma humano APP e página de detalhes do gene APP no navegador do genoma UCSC .