Antraceno - Anthracene

|
|

|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Antraceno |
|
|
Nome IUPAC sistemático
Triciclo [8.4.0.0 3,8 ] tetradeca-1,3,5,7,9,11,13-heptaeno |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 1905429 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard |
100,003,974 |
| Número EC | |
| 67837 | |
| KEGG | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 14 H 10 | |
| Massa molar | 178,234 g · mol −1 |
| Aparência | Incolor |
| Odor | Fraco aromático |
| Densidade | 1,28 g / cm 3 (25 ° C) 0,969 g / cm 3 (220 ° C) |
| Ponto de fusão | 216 ° C (421 ° F; 489 K) a 760 mmHg |
| Ponto de ebulição | 341,3 ° C (646,3 ° F; 614,5 K) a 760 mmHg |
| 0,022 mg / L (0 ° C) 0,044 mg / L (25 ° C) 0,29 mg / L (50 ° C) 0,00045% p / p (100 ° C, 3,9 MPa) |
|
| Solubilidade | Solúvel em álcool , (C 2 H 5 ) 2 O , acetona , C 6 H 6 , CHCl 3 , CS 2 |
| Solubilidade em etanol | 0,76 g / kg (16 ° C) 1,9 g / kg (19,5 ° C) 3,28 g / kg (25 ° C) |
| Solubilidade em metanol | 18 g / kg (19,5 ° C) |
| Solubilidade em hexano | 3,7 g / kg |
| Solubilidade em tolueno | 9,2 g / kg (16,5 ° C) 129,4 g / kg (100 ° C) |
| Solubilidade em tetracloreto de carbono | 7,32 g / kg |
| log P | 4,56 |
| Pressão de vapor | 0,01 kPa (125,9 ° C) 0,1 kPa (151,5 ° C) 13,4 kPa (250 ° C) |
|
Constante da lei de Henry ( k H ) |
0,0396 L · atm / mol |
| UV-vis (λ max ) | 345,6 nm, 363,2 nm |
| −129,8 × 10 −6 cm 3 / mol | |
| Condutividade térmica | 0,1416 W / (m · K) (240 ° C) 0,1334 W / (m · K) (270 ° C) 0,1259 W / (m · K) (300 ° C) |
| Viscosidade | 0,602 cP (240 ° C) 0,498 cP (270 ° C) 0,429 cP (300 ° C) |
| Estrutura | |
| Monoclínico (290 K) | |
| P2 1 / b | |
| D5 2h |
|
|
a = 8,562 Å, b = 6,038 Å, c = 11,184 Å
α = 90 °, β = 124,7 °, γ = 90 °
|
|
| Termoquímica | |
|
Capacidade de calor ( C )
|
210,5 J / (mol · K) |
|
Entropia molar padrão ( S |
207,5 J / (mol · K) |
| 129,2 kJ / mol | |
| 7061 kJ / mol | |
| Perigos | |
| Pictogramas GHS |
 
|
| Palavra-sinal GHS | Aviso |
| H302 , H305 , H315 , H319 , H335 , H410 | |
| P261 , P273 , P305 + 351 + 338 , P501 | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | 121 ° C (250 ° F; 394 K) |
| 540 ° C (1.004 ° F; 813 K) | |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
100-149 mg / kg (ratos, oral) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O antraceno é um hidrocarboneto policíclico aromático (PAH) sólido de fórmula C 14 H 10 , consistindo em três anéis de benzeno fundidos . É um componente do alcatrão de carvão . O antraceno é usado na produção do corante vermelho alizarina e outros corantes. O antraceno é incolor, mas exibe uma fluorescência azul (pico de 400–500 nm) sob radiação ultravioleta .
Ocorrência e produção
O alcatrão de carvão, que contém cerca de 1,5% de antraceno, continua sendo a principal fonte desse material. As impurezas comuns são fenantreno e carbazol . A forma mineral do antraceno é chamada de freitalita e está relacionada a um depósito de carvão. Um método clássico de laboratório para a preparação de antraceno é por ciclodesidratação de diarilcetonas substituídas por o-metil ou o-metileno na chamada reação de Elbs .
Reações
Redução
A redução do antraceno com metais alcalinos produz os sais de ânions radicais profundamente coloridos M + [antraceno] - (M = Li, Na, K). A hidrogenação dá 9,10- diidroantraceno , preservando a aromaticidade dos dois anéis flanqueadores.
Cycloadditions
O antraceno fotodimeriza pela ação da luz ultravioleta :
O dímero , chamado diantraceno (ou às vezes parantraceno), é conectado por um par de novas ligações carbono-carbono, o resultado da cicloadição [4 + 4] . Ele reverte para antraceno termicamente ou com irradiação UV abaixo de 300 nm. Os derivados de antraceno substituídos se comportam de maneira semelhante. A reação é afetada pela presença de oxigênio .
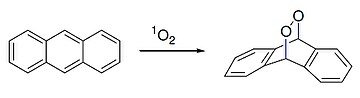
O antraceno também reage com o oxigênio singlete dienófilo em uma ciclcarregação [4 + 2] ( reação de Diels-Alder ):
Com eletrófilos
A oxidação química ocorre prontamente, dando antraquinona , C 14 H 8 O 2 (abaixo), por exemplo, usando peróxido de hidrogênio e acetilacetonato de vanadila .
A substituição eletrofílica do antraceno ocorre na posição 9. Por exemplo, a formilação fornece 9-antracenocarboxaldeído . A substituição em outras posições é efetuada indiretamente, por exemplo, começando com a antroquinona. A bromação de antraceno dá 9,10-dibromoantraceno.
Usos
O antraceno é convertido principalmente em antraquinona , um precursor de corantes.
Nicho
O antraceno, um semicondutor orgânico com gap largo, é usado como cintilador para detectores de fótons , elétrons e partículas alfa de alta energia . Plásticos, como o poliviniltolueno , podem ser dopados com antraceno para produzir um cintilador de plástico que é aproximadamente equivalente à água para uso em dosimetria de radioterapia . O espectro de emissão do antraceno atinge o pico entre 400 nm e 440 nm.
Ele também é usado em conservantes de madeira , inseticidas e materiais de revestimento .
O antraceno é comumente usado como um traçador de UV em revestimentos isolantes aplicados a placas de circuito impresso. O traçador de antraceno permite que o revestimento isolante seja inspecionado sob luz ultravioleta. O antraceno também é usado na fabricação de antraquinona.
Derivados

Uma variedade de derivados do antraceno encontram usos especializados. Derivados com um grupo hidroxila são 1-hidroxiantraceno e 2-hidroxiantraceno, homólogo ao fenol e naftóis , e o hidroxiantraceno (também chamado de antrol e antracenol) são farmacologicamente ativos. O antraceno também pode ser encontrado com vários grupos hidroxila, como no 9,10-di-hidroxiantraceno .
Ocorrência
O antraceno, como muitos outros hidrocarbonetos aromáticos policíclicos , é gerado durante os processos de combustão. A exposição ao homem ocorre principalmente por meio da fumaça do tabaco e da ingestão de alimentos contaminados com produtos da combustão.
Toxicologia
Muitas investigações indicam que o antraceno não é carcinogênico: "resultados consistentemente negativos em vários testes de genotoxicidade in vitro e in vivo". Os primeiros experimentos sugeriram o contrário, porque as amostras brutas estavam contaminadas com outros compostos aromáticos policíclicos . Além disso, é facilmente biodegradado no solo. É especialmente suscetível à degradação na presença de luz.
Veja também
- 9,10-Ditioantraceno , derivado com dois grupos tiol adicionados ao anel central
- Fenantreno
- Tetraceno
Referências
Fontes citadas
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92ª ed.). CRC Press . ISBN 978-1439855119.