Bioquímica do arsênico - Arsenic biochemistry

A bioquímica do arsênio se refere a processos bioquímicos que podem usar o arsênio ou seus compostos, como o arsenato . O arsênio é um elemento moderadamente abundante na crosta terrestre e, embora muitos compostos de arsênio sejam frequentemente considerados altamente tóxicos para a maioria da vida, uma grande variedade de compostos organoarsênicos é produzida biologicamente e vários compostos orgânicos e inorgânicos de arsênio são metabolizados por numerosos organismos . Esse padrão é geral para outros elementos relacionados, incluindo selênio , que pode exibir efeitos benéficos e deletérios. A bioquímica do arsênio tornou-se tópica, uma vez que muitos compostos tóxicos de arsênio são encontrados em alguns aquíferos , afetando potencialmente muitos milhões de pessoas por meio de processos bioquímicos.
Fontes de arsênico
Compostos organoarsênicos na natureza
A evidência de que o arsênico pode ser um nutriente benéfico em níveis residuais abaixo do fundo ao qual os organismos vivos estão normalmente expostos foi revisada. Alguns compostos organoarsênicos encontrados na natureza são a arsenobetaína e a arsenocolina, ambas encontradas em muitos organismos marinhos. Alguns nucleosídeos contendo As (derivados de açúcar) também são conhecidos. Vários desses compostos organoarsênicos surgem por meio de processos de metilação . Por exemplo, o fungo Scopulariopsis brevicaulis produz quantidades significativas de trimetilarsina se o arsênio inorgânico estiver presente. O composto orgânico arsenobetaína é encontrado em alguns alimentos marinhos, como peixes e algas, e também em cogumelos em concentrações maiores. Em ambientes limpos, a espécie de cogumelo comestível Cyanoboletus pulverulentus hiperacumula arsênio em concentrações que chegam a 1.300 mg / kg em peso seco; O ácido cacodílico é o principal composto de As. Uma composição muito incomum de compostos organoarsênicos foi encontrada em trufas de veado ( Elaphomyces spp.). A ingestão média de uma pessoa é de cerca de 10–50 µg / dia. Valores em torno de 1000 µg não são incomuns após o consumo de peixes ou cogumelos; no entanto, há pouco perigo em comer peixe, uma vez que esse composto de arsênico é quase não tóxico.
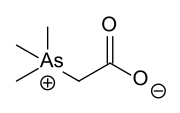
- Compostos organoarsênicos representativos encontrados na natureza.
Arsenobetaína , um dos compostos de arsênico mais comuns na natureza. Também comum é a arsenocolina, que tem CH 2 OH no lugar de CO 2 H).
Trimetilarsina , produzida por ação microbiana em pigmentos derivados de arseniato
Derivados de ribose contendo arsênio (R = vários grupos)
Uma fonte tópica de arsênico são os pigmentos verdes, uma vez populares em papéis de parede, por exemplo, o verde Paris . Uma variedade de doenças foi atribuída a esse composto, embora sua toxicidade tenha sido exagerada.
A trimetilarsina , antes conhecida como gás de Gosio, é um composto organoarsênico com odor intenso e comumente produzido por ação microbiana em substratos de arsênio inorgânico.
Os compostos de arsênio (V) são facilmente reduzidos a arsênio (III) e poderiam ter servido como um aceptor de elétrons na Terra primordial. Os lagos que contêm uma quantidade substancial de arsênio inorgânico dissolvido abrigam uma biota tolerante ao arsênio .
Alegações incorretas de vida à base de arsênio (substituição de fósforo)
Embora o fosfato e o arsenato sejam estruturalmente semelhantes, não há evidências de que o arsênio substitua o fósforo no DNA ou RNA . Um experimento de 2010 envolvendo a bactéria GFAJ-1 que fez essa afirmação foi refutado em 2012.
Compostos antropogênicos de arsênio
Fontes antropogênicas (artificiais) de arsênio, como as fontes naturais, são principalmente óxidos de arsênio e os ânions associados. As fontes de arsênico artificiais incluem resíduos do processamento de minerais, granjas de suínos e aves. Por exemplo, muitos minérios, especialmente minerais de sulfeto , estão contaminados com arsênio, que é liberado na torrefação (queima no ar). Nesse processamento, o arsenieto é convertido em trióxido de arsênio , que é volátil em altas temperaturas e é liberado na atmosfera. As granjas de aves e suínos usam intensamente o composto organoarsênico roxarsone como antibiótico na ração. Algumas madeiras são tratadas com arseniato de cobre como conservante. Os mecanismos pelos quais essas fontes afetam os organismos vivos "a jusante" permanecem incertos, mas provavelmente são diversos. Uma via comumente citada envolve a metilação .
O ácido monometilado, ácido metanearsônico (CH 3 AsO (OH) 2 ), é um precursor de fungicidas (nome comercial Neoasozin) no cultivo de arroz e algodão. Derivados do ácido fenilarsônico (C 6 H 5 AsO (OH) 2 ) são usados como aditivos alimentares para animais, incluindo ácido 4-hidroxi-3-nitrobenzenoearsônico (3-NHPAA ou Roxarsone), ácido ureidofenilarsônico e ácido p -arsanílico . Essas aplicações são controversas, pois introduzem formas solúveis de arsênio no meio ambiente.
Drogas à base de arsênico
Apesar de, ou possivelmente por causa de, sua conhecida toxicidade, as poções e drogas que contêm arsênico têm uma história na medicina e no charlatanismo que continua até o século XXI. Começando no início do século 19 e continuando no século 20, a solução de Fowler , uma mistura tóxica de arsenito de sódio , foi vendida. O composto organoarsenic Salvarsan foi o primeiro agente quimioterápico sintético , descoberto por Paul Ehrlich . O tratamento, no entanto, levou a muitos problemas, causando complicações de saúde duradouras. Por volta de 1943, foi finalmente substituído pela penicilina . O medicamento relacionado Melarsoprol ainda é usado contra a tripanossomíase africana de estado avançado (doença do sono), apesar de sua alta toxicidade e efeitos colaterais possivelmente fatais.
O trióxido de arsênio (As 2 O 3 ) inibe o crescimento celular e induz a apoptose (morte celular programada) em certos tipos de células cancerosas, que normalmente são imortais e podem se multiplicar sem limites. Em combinação com o ácido retinóico totalmente trans , é aprovado pela FDA como tratamento de primeira linha para a leucemia promielocítica .
Metilação de arsênico
O arsênio inorgânico e seus compostos, ao entrar na cadeia alimentar , são progressivamente metabolizados (desintoxicados) por meio de um processo de metilação . A metilação ocorre por meio de reações alternadas de metilação redutiva e oxidativa, ou seja, redução do arsênio pentavalente a trivalente seguida da adição de um grupo metil (CH 3 ).

Em mamíferos, a metilação ocorre no fígado por metiltransferases , sendo os produtos (CH 3 ) 2 AsOH ( ácido dimetilarsínico ) e (CH 3 ) 2 As (O) OH ( ácido dimetilarsínico ), que possuem os estados de oxidação As (III) e As (V), respectivamente. Embora o mecanismo de metilação do arsênio em humanos não tenha sido elucidado, a fonte de metil é a metionina , o que sugere um papel da S-adenosil metionina . A exposição a doses tóxicas começa quando a capacidade de metilação do fígado é excedida ou inibida.
Existem duas formas principais de arsênio que podem entrar no corpo, arsênio (III) e arsênio (V). O arsênio (III) entra nas células através das aquaporinas 7 e 9, que é um tipo de aquagliceroporina. Os compostos de arsênio (V) usam transportadores de fosfato para entrar nas células. O arsênio (V) pode ser convertido em arsênio (III) pela enzima purina nucleosídeo fosforilase . Isso é classificado como uma etapa de bioativação, pois embora o arsênio (III) seja mais tóxico, é mais facilmente metilado.
Existem duas rotas pelas quais os compostos de arsênio inorgânico são metilados. A primeira rota usa metiltransferase de arsênio Cyt19 para metilar o arsênio (III) em um composto de arsênio mono-metilado (V). Este composto é então convertido em um composto de arsênio mono-metilado (III) usando Glutationa S-Transferase Omega-1 ( GSTO1 ). O composto de arsênio mono-metilado (V) pode então ser metilado novamente por Cyt19 arsênio metiltransferase, que forma um composto de dimetil arsênio (V), que pode ser convertido em um composto de dimetil arsênio (III) pela Glutationa S-Transferase Omega-1 ( GTSO1). A outra rota usa glutationa (GSH) para se conjugar com arsênio (III) para formar um complexo de arsênio (GS) 3 . Este complexo pode formar um complexo GS de arsênio (III) monometilado, usando metiltransferase de arsênio Cyt19, e este complexo GS monometilado está em equilíbrio com o arsênio monometilado (III). A metiltransferase de arsênio Cyt19 pode metilar o complexo mais uma vez, e isso forma um complexo GS de arsênio dimetilado, que está em equilíbrio com um complexo de dimetil arsênio (III). Ambos os compostos de arsênio mono-metilado e di-metilado podem ser facilmente excretados na urina. No entanto, o composto monometilado mostrou ser mais reativo e mais tóxico do que os compostos de arsênio inorgânico para hepatócitos humanos (fígado), queratinócitos na pele e células epiteliais brônquicas (pulmões).
Estudos em animais experimentais e humanos mostram que tanto o arsênio inorgânico quanto os metabólitos metilados atravessam a placenta para o feto ; no entanto, há evidências de que a metilação aumenta durante a gravidez e que pode ser altamente protetora para o organismo em desenvolvimento.
A metilação enzimática do arsênio é um processo de desintoxicação; pode ser metilado em metilarsenita, dimetilarsenita ou trimetilarsenita, todos trivalentes. A metilação é catalisada pela metiltransferase de arsênio (AS3MT) em mamíferos, que transfere um grupo metil no cofator S-adenometionina (SAM) para o arsênio (III). Um ortólogo do AS3MT é encontrado nas bactérias e é denominado CmArsM. Esta enzima foi testada em três estados (livre de ligante, ligada a arsênio (III) e ligada a SAM). Os locais de ligação do arsênio (III) geralmente usam grupos tiol de resíduos de cisteína. A catálise envolve tiolatos de Cys72, Cys174 e Cys224. Em uma reação SN2, a carga positiva no átomo de enxofre SAM puxa o elétron de ligação do carbono do grupo metil, que interage com o par de arsênio solitário para formar uma ligação As-C, deixando SAH.
Excreção
Em humanos, a principal via de excreção da maioria dos compostos de arsênio é pela urina . A meia-vida biológica do arsênio inorgânico é de cerca de 4 dias, mas é ligeiramente mais curta após a exposição ao arsenato do que ao arsenito. Os principais metabolitos excretados na urina de seres humanos expostos ao arsénio inorgânico são mono- e dimetilada ácidos de arsénio , em conjunto com alguns arsénio inorgânico não metabolizado.
A biotransformação do arsênio para excreção é feita principalmente por meio da via do fator 2 relacionado ao fator nuclear eritróide 2 ( Nrf2 ). Em condições normais, o Nrf2 liga-se à proteína 1 associada a ECH semelhante a Kelch ( Keap1 ) na sua forma inativa. Com a absorção de arsênio dentro das células e as reações subsequentes que resultam na produção de espécies reativas de oxigênio (ROS), o Nrf2 se desfaz e se torna ativo. Keap1 tem porções tiol reativas que se ligam a ROS ou espécies de arsênio eletrofílico, como o arsênio monometilado (III) e induz a liberação de Nrf2, que então viaja através do citoplasma para o núcleo . O Nrf2 então ativa o elemento responsivo a antioxidantes (ARE), bem como o elemento responsivo eletrofílico (EpRE), os quais contribuem para o aumento das proteínas antioxidantes. De particular interesse nestas proteínas antioxidantes é a heme oxigenase 1 ([HO-1]), NAD (P) H-quinona oxidoredutase 1 (NQO1) e γ-glutamilcisteína sintase (γGCS) que trabalham em conjunto para reduzir as espécies oxidativas, tais como peróxido de hidrogênio para diminuir o estresse oxidativo sobre a célula. O aumento em γGCS causa um aumento na produção de arsenito triglutationina (As (SG) 3 ), um aduto importante que é absorvido pela proteína associada a múltiplas drogas 1 ou 2 ( MRP1 ou MRP2 ) que remove o arsênio da célula e para a bile para excreção. Este aduto também pode se decompor em arsênico inorgânico.
De particular importância na excreção de arsênio são as múltiplas etapas de metilação que podem aumentar a toxicidade do arsênio devido ao MMeAsIII ser um potente inibidor da glutationa peroxidase, glutationa redutase, piruvato desidrogenase e tioredoxina redutase.
Toxicidade de arsênico
O arsênico é uma causa de mortalidade em todo o mundo; os problemas associados incluem doenças cardíacas, respiratórias, gastrointestinais, hepáticas, nervosas e renais.
O arsênio interfere na longevidade celular pela inibição alostérica de um complexo enzimático metabólico essencial piruvato desidrogenase (PDH), que catalisa a oxidação do piruvato a acetil-CoA por NAD + . Com a enzima inibida, o sistema de energia da célula é interrompido, resultando em um episódio de apoptose celular . Bioquimicamente, o arsênico impede o uso de tiamina, resultando em um quadro clínico semelhante à deficiência de tiamina . O envenenamento com arsênico pode aumentar os níveis de lactato e levar à acidose láctica .
A genotoxicidade envolve a inibição do reparo e metilação do DNA. O efeito cancerígeno do arsênio surge do estresse oxidativo induzido pelo arsênio. A alta toxicidade do arsênico naturalmente levou ao desenvolvimento de uma variedade de compostos de arsênio como armas químicas , por exemplo, cloreto dimetilarsênico. Alguns foram empregados como agentes de guerra química , especialmente na Primeira Guerra Mundial . Essa ameaça levou a muitos estudos sobre antídotos e a um conhecimento mais amplo da interação dos compostos de arsênio com os organismos vivos. Um dos resultados foi o desenvolvimento de antídotos como o anti-Lewisite britânico . Muitos desses antídotos exploram a afinidade do As (III) pelos ligantes tiolato , que convertem organoarsenicais altamente tóxicos em derivados menos tóxicos. É geralmente assumido que os arsenatos se ligam aos resíduos de cisteína nas proteínas.
Em contraste, o óxido de arsênio é um medicamento quimioterápico aprovado e eficaz para o tratamento da leucemia promielocítica aguda (APL).
Toxicidade de arsênicos pentavalentes
Devido à sua estrutura e propriedades semelhantes, os metabólitos do arsênio pentavalente são capazes de substituir o grupo fosfato de muitas vias metabólicas. A substituição de fosfato por arseniato é iniciada quando o arseniato reage com a glicose e o gluconato in vitro. Esta reação gera glicose-6-arsenato e 6-arsenogluconato, que atuam como análogos para glicose-6-fosfato e 6-fosfogluconato. No nível do substrato, durante a glicólise , a glicose-6-arseniato se liga como substrato à glicose-6-fosfato desidrogenase e também inibe a hexoquinase por meio de feedback negativo. Ao contrário da importância do fosfato na glicólise, a presença de arseniato restringe a geração de ATP por formar um produto anidrido instável, por meio da reação com D-gliceraldeído-3-fosfato. O anidrido 1-arsenato-3-fosfo-D-glicerato gerado hidrolisa prontamente devido ao comprimento de ligação mais longo de As-O em comparação com PO. No nível mitocondrial, o arsenato desacopla a síntese de ATP ligando-se ao ADP na presença de succinato , formando assim um composto instável que acaba resultando em uma diminuição do ganho líquido de ATP. Os metabólitos do arsenito (III), por outro lado, têm efeito limitado sobre a produção de ATP nos glóbulos vermelhos.
Toxicidade de arsenicais trivalentes
Enzimas e receptores que contêm grupos funcionais tiol ou sulfidrila são ativamente direcionados por metabólitos de arsenito (III). Esses compostos contendo enxofre são normalmente glutationa e o aminoácido cisteína. Os derivados de arsenito geralmente têm maior afinidade de ligação em comparação com os metabólitos de arsenato. Essas ligações restringem a atividade de certas vias metabólicas. Por exemplo, a piruvato desidrogenase (PDH) é inibida quando o ácido monometilarsônico (MMA III ) tem como alvo o grupo tiol do cofator de ácido lipóico. O PDH é um precursor da acetil-CoA , portanto, a inibição do PDH eventualmente limita a produção de ATP na cadeia de transporte de elétrons , bem como a produção de intermediários da gliconeogênese .
Estresse oxidativo
O arsênio pode causar estresse oxidativo por meio da formação de espécies reativas de oxigênio (ROS) e espécies reativas de nitrogênio (RNS). As espécies reativas de oxigênio são produzidas pela enzima NADPH oxidase , que transfere elétrons do NADPH para o oxigênio, sintetizando um superóxido , que é um radical livre reativo. Este superóxido pode reagir para formar peróxido de hidrogênio e uma espécie reativa de oxigênio. A enzima NADPH oxidase é capaz de gerar espécies mais reativas de oxigênio na presença de arsênio, devido à subunidade p22phax, responsável pela transferência de elétrons, ser regulada positivamente pelo arsênio. As espécies reativas de oxigênio são capazes de estressar o retículo endoplasmático , o que aumenta a quantidade de sinais de resposta da proteína não dobrada. Isso leva à inflamação, proliferação celular e, eventualmente, à morte celular. Outro mecanismo pelo qual espécies reativas de oxigênio causam morte celular seria por meio do rearranjo do citoesqueleto , que afeta as proteínas contráteis.
As espécies reativas de nitrogênio surgem quando as espécies reativas de oxigênio destroem a mitocôndria . Isso leva à formação de espécies reativas de nitrogênio, que são responsáveis por danificar o DNA no envenenamento por arsênio. O dano mitocondrial é conhecido por causar a liberação de espécies reativas de nitrogênio, devido à reação entre os superóxidos e o óxido nítrico (NO). O óxido nítrico (NO) é uma parte da regulação celular, incluindo o metabolismo , crescimento, divisão e morte celular . O óxido nítrico (NO) reage com espécies reativas de oxigênio para formar peroxinitrito . Em casos de exposição crônica ao arsênio, os níveis de óxido nítrico são reduzidos, devido às reações do superóxido. A enzima NO sintase (NOS) usa L-arginina para formar óxido nítrico, mas esta enzima é inibida por compostos monometilados de arsênio (III).
Dano de DNA
É relatado que o arsênio causa modificações no DNA , como aneuploidia , formação de micronúcleos , anormalidades cromossômicas , mutações de deleção , troca de cromátides irmãs e reticulação de DNA com proteínas. Foi demonstrado que o arsênio não interage diretamente com o DNA e é considerado um mutagênico fraco , mas, em vez disso, ajuda na mutagenicidade de outros carcinógenos . Por exemplo, um aumento sinérgico na atividade mutagênica do arsênio com luz ultravioleta foi observado em células humanas e de outros mamíferos após a exposição das células tratadas com ultravioleta ao arsênio. Uma série de observações experimentais sugere que a genotoxicidade do arsênio está principalmente ligada à geração de espécies reativas de oxigênio (ROS) durante sua biotransformação. A produção de ROS é capaz de gerar adutos de DNA, quebras de fita de DNA, ligações cruzadas e aberrações cromossômicas. O dano oxidativo é causado pela modificação de nucleobases do DNA , em particular 8-oxoguanina (8-OHdG) que leva a mutações G: C a T: A. O arsênico inorgânico também pode causar quebra da fita de DNA, mesmo em baixas concentrações.
Inibição de reparo de DNA
A inibição dos processos de reparo do DNA é considerada um dos principais mecanismos de genotoxicidade do arsênio inorgânico. O reparo por excisão de nucleotídeos (NER) e o reparo por excisão de base (BER) são os processos implicados no reparo do dano à base do DNA induzido por ROS após a exposição ao arsênio. Em particular, o mecanismo NER é a principal via para reparar distorções volumosas na dupla hélice do DNA, enquanto o mecanismo BER está principalmente implicado no reparo de quebras de fita simples induzidas por ROS, mas o arsênio inorgânico também pode reprimir o mecanismo BER.
Mecanismos neurodegenerativos
O arsênico é altamente prejudicial para o sistema imunológico inato e adaptativo do corpo. Quando a quantidade de proteínas não dobradas e mal dobradas no estresse do retículo endoplasmático é excessiva, a resposta da proteína não dobrada (UPR) é ativada para aumentar a atividade de vários receptores que são responsáveis pela restauração da homeostase. A enzima-1 que requer inositol (IRE1) e a proteína quinase do retículo endoplasmático quinase (PERK) são dois receptores que restringem a taxa de tradução. Por outro lado, as proteínas não dobradas são corrigidas pela produção de chaperonas , que são induzidas pelo fator ativador de transcrição 6 (ATF6). Se o número de proteínas errôneas aumenta, outro mecanismo é ativo, o que desencadeia a apoptose . O arsênico demonstrou, evidentemente, aumentar a atividade desses sensores de proteína.
Disfunção imunológica
A exposição ao arsênio em crianças pequenas distorce a proporção de células T auxiliares ( CD4 ) em relação às células T citotóxicas ( CD8 ), que são responsáveis pela imunodepressão. Além disso, o arsênio também aumenta o número de moléculas inflamatórias secretadas pelos macrófagos . A quantidade excessiva de granulócitos e monócitos leva a um estado crônico de inflamação, que pode resultar no desenvolvimento de câncer .
Tratamento de envenenamento por arsênico
Existem três moléculas que atuam como agentes quelantes que se ligam ao arsênico. Estes três são British Anti-Lewisite (BAL, Dimercaprol), succimer ( DMSA ) e Unithiol ( DMPS ).
Quando esses agentes quelam o arsênio inorgânico, ele é convertido em uma forma orgânica de arsênio porque está ligado ao agente quelante orgânico. Os átomos de enxofre dos grupos tiol são o local de interação com o arsênio. Isso ocorre porque os grupos tiol são nucleofílicos, enquanto os átomos de arsênio são eletrofílicos . Uma vez ligadas ao agente quelante, as moléculas podem ser excretadas e, portanto, átomos de arsênio inorgânico livres são removidos do corpo.
Outros agentes quelantes podem ser usados, mas podem causar mais efeitos colaterais do que British Anti-Lewisite (BAL, Dimercaprol), succimer ( DMSA ) e ( DMPS ). DMPS e DMSA também têm um índice terapêutico mais alto que o BAL.
Essas drogas são eficazes para o envenenamento agudo por arsênio, que se refere aos efeitos instantâneos causados pelo envenenamento por arsênio. Por exemplo, dores de cabeça, vômitos ou suores são alguns dos exemplos comuns de um efeito instantâneo. Em comparação, efeitos tóxicos crônicos surgem mais tarde, e inesperadamente, como danos a órgãos. Normalmente, é tarde demais para evitá-los, uma vez que aparecem. Portanto, medidas devem ser tomadas assim que surgirem efeitos tóxicos agudos.
Veja também
- Compostos de arsênico
- Extremófilo
- Geomicrobiologia
- Tipos hipotéticos de bioquímica
- Química Organoarsênica