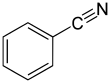
Benzonitrila - Benzonitrile
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Benzonitrila |
|||
|
Nome IUPAC sistemático
Benzenocarbonitrila |
|||
| Outros nomes | |||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 3DMet | |||
| 506893 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100,002,596 |
||
| Número EC | |||
| 2653 | |||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 2224 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
|
C 6 H 5 (CN) |
|||
| Massa molar | 103,12 g / mol | ||
| Densidade | 1,0 g / ml | ||
| Ponto de fusão | -13 ° C (9 ° F; 260 K) | ||
| Ponto de ebulição | 188 a 191 ° C (370 a 376 ° F; 461 a 464 K) | ||
| <0,5 g / 100 ml (22 ° C) | |||
| -65,19 · 10 −6 cm 3 / mol | |||
|
Índice de refração ( n D )
|
1,5280 | ||
| Perigos | |||
| Pictogramas GHS |

|
||
| Palavra-sinal GHS | Aviso | ||
| H302 , H312 | |||
| P264 , P270 , P280 , P301 + 312 , P302 + 352 , P312 , P322 , P330 , P363 , P501 | |||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | 75 ° C (167 ° F; 348 K) | ||
| 550 ° C (1.022 ° F; 823 K) | |||
| Limites explosivos | 1,4-7,2% | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Benzonitrila é o composto químico com a fórmula C
6 H
5 (CN) , abreviado como Ph CN. Este composto orgânico aromático é um líquido incolor com um odor doce de amêndoa amarga. É usado principalmente como precursor da resina benzoguanamina .
Produção
É preparado pela amoxidação do tolueno , ou seja, sua reação com amônia e oxigênio (ou ar) entre 400 a 450 ° C (752 a 842 ° F).
-
C
6 H
5 CH
3 + 3/2 O
2 + NH
3 → C
6 H
5 (CN) + 3 H
2 O
Em laboratório pode ser preparado pela desidratação da benzamida ou pela reação de Rosenmund-von Braun com cianeto cuproso ou NaCN / DMSO e bromobenzeno .
Formulários
Usos de laboratório
O benzonitrila é um solvente útil e um precursor versátil para muitos derivados. Ele reage com aminas para fornecer benzamidas N-substituídas após hidrólise. É um precursor da difenilcetimina Ph
2 C = NH (p.e. 151 ° C, 8 mm Hg) via reação com brometo de fenilmagnésio seguido por metanólise .
O benzonitrila forma complexos de coordenação com metais de transição que são solúveis em solventes orgânicos e convenientemente instáveis. Um exemplo é PdCl
2 (PhCN)
2 . Os ligantes de benzonitrila são facilmente substituídos por ligantes mais fortes, tornando os complexos de benzonitrila intermediários sintéticos úteis.
História
O benzonitrila foi relatado por Hermann Fehling em 1844. Ele descobriu o composto como um produto da desidratação térmica do benzoato de amônio . Ele deduziu sua estrutura a partir da reação análoga já conhecida do formato de amônio, produzindo formonitrila. Ele também cunhou o nome benzonitrila, que deu o nome a todo o grupo de nitrilas .
Em 2018, foi relatado que o benzonitrila foi detectado no meio interestelar .