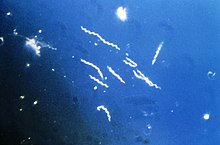
Borrelia burgdorferi -Borrelia burgdorferi
| Borrelia burgdorferi | |
|---|---|
|
|
| Borrelia burgdorferi | |
|
Classificação científica |
|
| Domínio: | Bactérias |
| Filo: | Spirochaetes |
| Pedido: | Spirochaetales |
| Família: | Spirochaetaceae |
| Gênero: | Borrelia |
| Espécies: |
B. burgdorferi
|
| Nome binomial | |
|
Borrelia burgdorferi Johnson et al. 1984 emend. Baranton et al. 1992
|
|
Borrelia burgdorferi sensu stricto é uma espécie bacteriana daclassedas espiroquetas do gênero Borrelia e é um dos agentes causadores da doença de Lyme em humanos. Junto com algumas genoespécies semelhantes, algumas das quais também causam a doença de Lyme, compõe o complexo de espécies de Borrelia burgdorferi sensu lato . O complexo atualmente compreende 20 genoespécies aceitas e 3 propostas. B. burgdorferi sensu stricto existe na América do Norte e na Eurásia e até 2016 era a única causa conhecida da doença de Lyme na América do Norte. As espécies de Borrelia são gram-negativas .
Microbiologia
Borrelia burgdorferi deve o seu nome ao pesquisador Willy Burgdorfer , que isolou a bactéria pela primeira vez em 1982.
Morfologia
B. burgdorferi se assemelha a outras espiroquetas por ter uma membrana externa e uma interna com uma fina camada de peptidoglicano entre elas . No entanto, a membrana externa carece de lipopolissacarídeo . Sua forma é uma onda plana. Tem cerca de 0,3 μm de largura e 5 a 20 μm de comprimento.
B. burgdorferi é um espiroqueta móvel microaeróbio com sete a 11 flagelos perisplásmicos agrupados em cada extremidade que permite que a bactéria se mova em meios de baixa e alta viscosidade, o que está relacionado ao seu alto fator de virulência.
Metabolismo
B. burgdorferi é uma espiroqueta microaerofílica de crescimento lento com um tempo de duplicação de 24 a 48 horas.
Vida útil
B. burgdorferi circula entre carrapatos Ixodes e um hospedeiro vertebrado em um ciclo enzoótico . B. burgdorferi que vive em um carrapato é adquirido principalmente por meio de alimentação de sangue de um hospedeiro vertebrado infectado e competente, mas existem casos raros de transmissão transovariana. Uma vez infectado, o carrapato transmitirá B. burgdorferi alimentando-se de outro vertebrado para completar o ciclo. Os carrapatos podem transmitir B. burgdorferi aos humanos, mas os humanos são hospedeiros sem saída, com pouca probabilidade de continuar o ciclo de vida do espiroqueta. As ninfas transformam-se em carrapatos adultos, que geralmente se alimentam de mamíferos maiores que não são capazes de sustentar a sobrevivência de B. burgdorferi .
Doença
A doença de Lyme é uma zoonótica , doença transmitida por vector transmitida pelo Ixodes carrapato (também no vector para Babesia e Anaplasma ). O carrapato ninfal infectado transmite B. burgdorferi através de sua saliva para o ser humano durante sua alimentação de sangue.
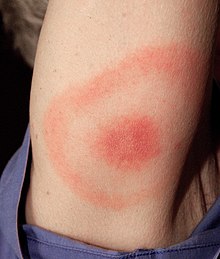
A apresentação clínica da doença de Lyme é mais conhecida pela erupção cutânea característica (também conhecida como eritema crônico migrans ), mas também pode incluir miocardite , cardiomiopatia , arritmia , artrite , artralgia , meningite , neuropatias e paralisia do nervo facial, dependendo do estágio de infecção.
As infecções por B. burgdorferi foram encontradas em possível associação com linfomas cutâneos primários de células B (PCBCLs), onde uma revisão da literatura primária, em 2010, observou que a maioria dos PCBCLs examinados não responderam aos antibióticos; portanto, como no caso da associação de Chlamydophila psittaci com o linfoma do tecido linfóide associado à mucosa anexial ocular (MALT), a conclusão de trabalho foi que "se B. burgdorferi está realmente associado a PCBCL, então há ampla variabilidade geográfica e outros fatores são provavelmente envolvidos ".
A progressão da doença segue 3 estágios.
Estágio 1
O estágio 1 é conhecido como estágio inicial localizado e ocorre aproximadamente 3 dias - 1 mês após a inoculação. Afeta a área local ao redor da picada e é caracterizada por edema local e / ou erupção cutânea em "olho de boi" vermelho (também conhecido como eritema crônico migrans ) visto como um círculo eritematoso circundando um centro definido que se expande para fora. Pode atingir 15 cm de diâmetro. Assim que a erupção começa a diminuir, os primeiros sintomas podem se manifestar como sintomas "semelhantes aos da gripe". Nesse estágio, os antibióticos são mais eficazes para prevenir o crescimento e os sintomas da doença antes que os sintomas principais se manifestem.
Estágio 2
O estágio 2 é conhecido como o estágio de disseminação precoce e ocorre semanas - meses após a infecção, se não for tratado. A bactéria se espalha pelo sangue através do corpo para afetar os órgãos. Muitas vezes se apresenta com sintomas gerais, como febre, calafrios, fadiga e linfadenopatia, bem como sintomas específicos de órgãos. Pode afetar o coração, causando miocardite e arritmias , como bloqueios atrioventriculares (que, se significativos o suficiente, podem exigir a inserção de um marca-passo). Pode afetar o sistema músculo-esquelético, causando artrite transitória não inflamatória e / ou artralgias . Pode afetar o sistema nervoso, manifestando-se como paralisia facial (paralisia de Bell , classicamente bilateral), fadiga e perda de memória.
Estágio 3
O estágio 3 é conhecido como estágio de disseminação tardia e ocorre meses - anos após a infecção inicial. Os efeitos do terceiro estágio incluem encefalite ou meningite, bem como artropatias migratórias (mais comumente do joelho).
A anaplasmose e a babesiose também são patógenos comuns transmitidos por carrapatos transportados pelo carrapato Ixodes que infectam humanos de forma semelhante à Borrelia burgdorferi . Consequentemente, é possível para um carrapato Ixodes co-infectar um hospedeiro com duas ou todas as outras doenças. Quando um hospedeiro é co-infectado, os efeitos combinados das doenças agem sinergicamente, muitas vezes provando causar sintomas piores do que uma única infecção. Os seres humanos co-infectados tendem a apresentar uma manifestação mais grave da doença de Lyme. Além disso, eles tendem a adquirir uma gama mais ampla de sintomas secundários, como sintomas semelhantes aos da gripe. Mais estudos e pesquisas devem ser feitos para determinar o efeito sinérgico da coinfecção e seu efeito no corpo humano.
Variação de gravidade
Até o momento, existem três fatores que podem contribuir para a gravidade da manifestação clínica da doença de Lyme. A presença de espaçadores ribossômicos, plasmídeos e a proteína C da superfície externa (OspC) são indicadores da gravidade da infecção. Além disso, os próprios humanos variam em sua resposta à infecção. A variação na resposta leva a diferentes manifestações clínicas e diferentes infecções em diferentes órgãos.
Informações adicionais sobre a doença de Lyme e sua causa
A terapia antibiótica resolve os sintomas clínicos, na maioria dos casos, durante os estágios iniciais da infecção. Sintomas persistentes ou recorrentes podem se desenvolver posteriormente em um subgrupo de pacientes. Os mecanismos subjacentes, patogênese e tratamento de PTLDS permanecem desconhecidos. Portanto, é de grande importância desenvolver uma vacina que impeça a incidência de infecções graves transmitidas por carrapatos, como borreliose de Lyme. A maioria dos esforços de pesquisa concentra-se na identificação de antígenos B. burgdorferi ou proteínas de carrapatos que são necessários para a sobrevivência de espiroquetas dentro de carrapatos, em uma tentativa de interferir na transmissão de patógenos de carrapatos ou infectividade nos hospedeiros, evitando assim a doença de Lyme.
Patogênese molecular
Depois que o patógeno é transmitido, ele se aclimata às condições dos mamíferos. Borrelia burgdorferi irá alterar suas glicoproteínas e proteases em sua membrana plasmática para facilitar sua disseminação pelo sangue. Durante a infecção, B. burgdorferi expressará proteínas que irão interagir com as células endoteliais , plaquetas , condrócitos e a matriz extracelular . Essa interação inibe o funcionamento adequado das áreas infectadas, levando às manifestações patológicas da doença de Lyme. Em resposta, o hospedeiro iniciará uma resposta inflamatória para tentar remover a infecção.
Borrelia burgdorferi , também, expressa pelo menos sete proteínas de ligação ao plasminogênio para interferência do fator H no nível de ativação. Isso faz parte de uma estratégia de evasão do sistema complemento que leva ao bloqueio a jusante da resposta imunológica.
Além disso, Borrelia burgdorferi tem uma estratégia para inibir diretamente a via clássica do sistema complemento. Uma lipoproteína borrelial BBK32, expressa na superfície de Borrelia burgdorferi , liga-se ao complexo de protease C1 da via clássica. Mais especificamente, BBK32 interage com a subunidade C1r de C1. O domínio C-terminal da proteína BBK32 medeia a ligação. Como resultado, C1 fica preso em uma forma inativa.
Genética
B. burgdorferi (cepa B31) foi o terceiro genoma microbiano já sequenciado , após o sequenciamento de Haemophilus influenzae e Mycoplasma genitalium em 1995. Seu cromossomo linear contém 910.725 pares de bases e 853 genes . O método de sequenciamento usado foi a espingarda do genoma completo . O projeto de sequenciamento, publicado na Nature em 1997 e na Molecular Microbiology em 2000, foi conduzido no The Institute for Genomic Research . No geral, o genoma de B. burgdorferi estranhamente consiste em um cromossomo megabase e uma variedade de plasmídeos circulares e lineares que variam em tamanho de 9 a 62 quilobases. O cromossomo megabase, ao contrário de muitas outras eubactérias, não tem relação com a virulência da bactéria ou com a interação parasita-hospedeiro. Alguns dos plasmídeos são necessários para o ciclo de vida de B. burgdorferi , mas não para a propagação da bactéria em cultura.
As variações genômicas de B. burgdorferi contribuem para vários graus de infecção e disseminação. Cada grupo genômico possui antígenos variados em seu receptor de membrana, que são específicos para a infecção do hospedeiro. Um desses receptores de membrana é a proteína de superfície OspC. A proteína de superfície OspC mostra-se um forte indicador da identificação da classificação genômica e do grau de disseminação. O número variável de loci OspC são indicações e determinantes para as variações de B. burgdorferi . A proteína de superfície também está na vanguarda da pesquisa atual de vacinas para a doença de Lyme via Borrelia .
Evolução
Cepas de B. burgdorferi geneticamente diversas , conforme definido pela seqüência de ospC , são mantidas no nordeste dos Estados Unidos. A seleção de equilíbrio pode atuar sobre ospC ou uma sequência próxima para manter a variedade genética de B. burgdorferi . A seleção de equilíbrio é o processo pelo qual várias versões de um gene são mantidas dentro do pool genético em frequências inesperadamente altas. Dois modelos principais que controlam o equilíbrio de seleção de B.burgdorferi são a seleção dependente de frequência negativa e o polimorfismo de nicho múltiplo . Esses modelos podem explicar como B. burgdorferi se diversificou e como a seleção pode ter afetado a distribuição das variantes de B. burgdorferi , ou a variação de características específicas da espécie, em certos ambientes.
Seleção dependente de frequência negativa
Na seleção dependente de frequência negativa, as variantes raras e incomuns terão uma vantagem seletiva sobre as variantes que são muito comuns em um ambiente. Para B. burgdorferi , as variantes de baixa frequência serão vantajosas porque os hospedeiros potenciais serão menos propensos a montar uma resposta imunológica à proteína externa OspC específica da variante.
Polimorfismo de nicho múltiplo
Os nichos ecológicos são todas as variáveis em um ambiente, como recursos, competidores e respostas, que contribuem para a aptidão do organismo. O polimorfismo de múltiplos nichos afirma que a diversidade é mantida dentro de uma população devido à quantidade variável de nichos e ambientes possíveis. Portanto, quanto mais nichos diversos, maior a probabilidade de polimofrismo e diversidade. Para B. burgdorferi , nichos de vértebras variados, como cervos e camundongos, podem afetar a seleção de balanceamento geral para variantes.
Veja também
Referências
Leitura adicional
- Velázquez, Encarna; Peix, Álvaro; Gómez-Alonso, Alberto (março de 2011). "Microorganismos y cáncer: evidencias científicas y nuevas hipótesis" [Microorganismos e câncer: evidências científicas e novas hipóteses]. Cirugía Española (em espanhol). 89 (3): 136–144. doi : 10.1016 / j.ciresp.2010.08.006 . PMID 21292247 .
- Koči, Juraj; Bista, Sandhya; Chirania, Payal; Yang, Xiuli; Kitsou, Chrysoula; Rana, Vipin Singh; Sim, Ozlem Buyuktanir; Sonenshine, Daniel E .; Pal, Utpal (17 de março de 2021). "Anticorpos contra domínios semelhantes a EGF em ortólogos Ixodes scapularis BM86 impactam a alimentação de carrapatos e a sobrevivência de Borrelia burgdorferi" . Relatórios científicos . 11 (1): 6095. bibcode : 2021NatSR..11.6095K . doi : 10.1038 / s41598-021-85624-5 . PMC 7971074 . PMID 33731754 .
links externos
| Scholia tem um perfil de tópico para Borrelia burgdorferi . |
- Entrevista em vídeo de Eva Sapi , PhD em Borrelia Biofilms
- Navegador de taxonomia NCBI Borrelia
- Página do genoma de Borrelia burgdoferi B31