Trióxido de carbono - Carbon trioxide
|
|
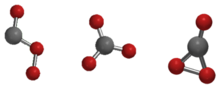 Os isômeros C s , D 3h e C 2v do trióxido de carbono
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Dioxiran-3-ona
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
|
PubChem CID
|
|
|
|
|
|
| Propriedades | |
| C O 3 | |
| Massa molar | 60,008 g · mol −1 |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
| Referências da Infobox | |
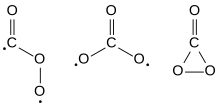
O trióxido de carbono ( CO 3 ) é um óxido de carbono instável (um oxocarbono ). Os possíveis isômeros de trióxido de carbono incluem aqueles com grupos de pontos de simetria molecular C s , D 3h e C 2v . O C 2v estado, que consiste de um dioxirano foi demonstrado que é o estado fundamental da molécula. O trióxido de carbono não deve ser confundido com o íon carbonato estável (CO 3 2− ).
O trióxido de carbono pode ser produzido, por exemplo, na zona de deriva de uma descarga corona negativa por reações entre o dióxido de carbono (CO 2 ) e o oxigênio atômico (O) criado a partir do oxigênio molecular por elétrons livres no plasma . Outro método relatado é a fotólise do ozônio O 3 dissolvido em CO 2 líquido , ou em misturas de CO 2 / SF 6 a -45 ° C, irradiado com luz de 253,7 nm. A formação de CO 3 é inferida, mas parece decair espontaneamente pela rota 2CO 3 → 2CO 2 + O 2 com uma vida útil muito menor que 1 minuto. O trióxido de carbono pode ser feito soprando ozônio em gelo seco (CO 2 sólido ) e também foi detectado em reações entre o monóxido de carbono (CO) e o oxigênio molecular (O 2 ). Junto com o isômero C2v do estado fundamental , a primeira detecção espectroscópica do isômero D 3h foi em gelos de dióxido de carbono irradiados por elétrons .
Referências
Leitura adicional
- Sobek V .; Skalný JD (1993). "Um modelo simples de processos na região de deriva de descarga corona negativa em uma mistura de ar com halocarbonos". Czechoslovak Journal of Physics . 43 (8): 807. Bibcode : 1993CzJPh..43..807S . doi : 10.1007 / BF01589802 . S2CID 120356317 .
- Pople JA ; Seeger U .; Seeger R .; Schleyer P. v. R. (2004). "A estrutura do carbonato". Journal of Computational Chemistry . 1 (2): 199–203. doi : 10.1002 / jcc.540010215 . S2CID 98748631 .
- Moll NG; Clutter DR; Thompson WE (1966). "Carbonato: sua produção, espectro infravermelho e estrutura estudada em uma matriz de CO 2 sólido ". The Journal of Chemical Physics . 45 (12): 4469–4481. Bibcode : 1966JChPh..45.4469M . doi : 10.1063 / 1.1727526 .
- Gimarc BM; Chou TS (1968). "Geometria e Estrutura Eletrônica do Trióxido de Carbono". The Journal of Chemical Physics . 49 (9): 4043–4047. Bibcode : 1968JChPh..49.4043G . doi : 10.1063 / 1.1670715 .
- DeMore WB; Dede C. (1970). "Dependência da pressão da formação de trióxido de carbono na reação em fase gasosa de O (1D) com dióxido de carbono". Journal of Physical Chemistry . 74 (13): 2621–2625. doi : 10.1021 / j100707a006 .
- Francisco JS; Williams IH (1985). "Um estudo teórico do campo de força do trióxido de carbono". Física Química . 95 (3): 373. Bibcode : 1985CP ..... 95..373F . doi : 10.1016 / 0301-0104 (85) 80160-9 .
