Corpo carotídeo - Carotid body
| Corpo carotídeo | |
|---|---|
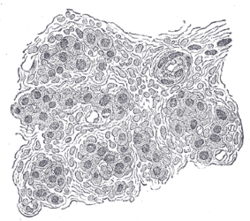 Seção de parte do corpo carotídeo humano. Altamente ampliado. Numerosos vasos sanguíneos são vistos seccionados entre as células.
| |
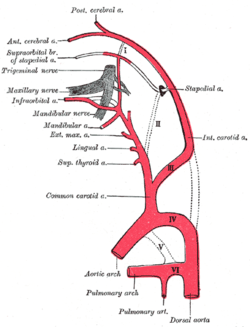 Diagrama mostrando as origens dos principais ramos das artérias carótidas.
| |
| Detalhes | |
| Nervo | ramo do nervo glossofaríngeo para seio carotídeo |
| Identificadores | |
| Latina | glomus caroticum |
| Malha | D002344 |
| TA98 | A12.2.04.007 |
| TA2 | 3886 |
| FMA | 50095 |
| Terminologia anatômica | |
O corpo carotídeo é um pequeno aglomerado de células quimiorreceptoras e células sustentaculares de suporte . O corpo carotídeo está localizado na adventícia , na bifurcação (bifurcação) da artéria carótida comum , que percorre os dois lados do pescoço .
O corpo carotídeo detecta mudanças na composição do sangue arterial que flui por ele, principalmente a pressão parcial do oxigênio arterial , mas também do dióxido de carbono . Também é sensível a mudanças no pH do sangue e na temperatura .
Estrutura
O corpo carotídeo é composto por dois tipos de células, chamadas células glômicas : as células glômicas tipo I são quimiorreceptores periféricos e as células glômicas tipo II são células sustentaculares de suporte.
- As células Glomus tipo I são derivadas da crista neural . Eles liberam uma variedade de neurotransmissores , incluindo acetilcolina , ATP e dopamina, que acionam EPSPs em neurônios sinapses que levam ao centro respiratório . Eles são inervados por axônios do nervo glossofaríngeo que coletivamente são chamados de nervo do seio carotídeo.
- As células Glomus tipo II se assemelham às células gliais , expressam o marcador glial S100 e agem como células de suporte.
Função
O corpo carotídeo funciona como um sensor: ele responde a um estímulo, principalmente a pressão parcial de O 2 , que é detectado pelas células do tipo I (glômus), e dispara um potencial de ação através das fibras aferentes do nervo glossofaríngeo , que retransmite a informação para o sistema nervoso central.
Estímulo
Os quimiorreceptores periféricos do corpo carotídeo são principalmente sensíveis a diminuições na pressão parcial de oxigênio (P O 2 ). Isso contrasta com os quimiorreceptores centrais da medula oblonga, que são primariamente sensíveis às mudanças no pH e no PCO 2 (uma diminuição no pH e um aumento no PCO 2 ). Os quimiorreceptores do corpo carotídeo também são sensíveis ao pH e ao PCO 2 , mas apenas secundariamente. Mais especificamente, a sensibilidade dos quimiorreceptores do corpo carotídeo à redução do P O 2 é maior quando o pH diminui e o PCO 2 aumenta.
A taxa de impulso dos corpos carotídeos é particularmente sensível a mudanças na PO2 arterial na faixa de 60 a 30 mm Hg, uma faixa na qual a saturação da hemoglobina com oxigênio diminui rapidamente.
A saída dos corpos carotídeos é baixa em uma pressão parcial de oxigênio acima de cerca de 100 mmHg (13,3 k Pa ) (em pH fisiológico normal), mas abaixo de 60 mmHg a atividade das células do tipo I (glômicas) aumenta rapidamente devido a uma diminuição em saturação de hemoglobina-oxigênio abaixo de 90%.
Detecção
O mecanismo de detecção de reduções de P O 2 ainda não foi identificado, podendo haver múltiplos mecanismos e podem variar entre as espécies. Foi demonstrado que a detecção de hipóxia depende do aumento da geração de sulfeto de hidrogênio produzido pela cistationina gama-liase, visto que a detecção de hipóxia é reduzida em camundongos nos quais esta enzima é nocauteada ou farmacologicamente inibida. O processo de detecção envolve a interação da cistationina gama-liase com a hemeoxigenase-2 e a produção de monóxido de carbono . No entanto, alguns estudos mostram que a concentração fisiológica de sulfeto de hidrogênio pode não ser forte o suficiente para desencadear tais respostas.
Outras teorias sugerem que pode envolver sensores de oxigênio mitocondrial e os citocromos contendo heme que sofrem redução reversível de um elétron durante a fosforilação oxidativa. O heme se liga reversivelmente ao O 2 com uma afinidade semelhante à do corpo carotídeo, sugerindo que as proteínas contendo heme podem ter um papel no O 2 , potencialmente este poderia ser um dos complexos envolvidos na fosforilação oxidativa. Isso leva a aumentos nas espécies reativas de oxigênio e no Ca 2+ intracelular . No entanto, não se sabe se a hipóxia leva a um aumento ou diminuição das espécies reativas de oxigênio. O papel das espécies reativas de oxigênio na detecção de hipóxia também está em questão.
A enzima hemoxidase dependente de oxigênio também foi apresentada como um sensor de hipóxia. Na normóxia, a hemoxigenase gera monóxido de carbono (CO), CO ativa o canal de potássio ativado por cálcio de grande condutância, BK. As quedas de CO que ocorrem como consequência da hipóxia levariam ao fechamento desse canal de potássio e isso levaria à despolarização da membrana e conseqüente ativação do corpo carotídeo. Um papel para a proteína quinase ativada por AMP "sensor de energia" (AMPK) também foi proposto na detecção de hipóxia. Esta enzima é ativada durante os períodos de uso líquido de energia e estresse metabólico, incluindo hipóxia. A AMPK tem uma série de alvos e parece que, no corpo carotídeo, quando a AMPK é ativada por hipóxia, ela leva ao fechamento do canal de potássio a jusante de ambos os canais TASK e canais BK de O 2.
Um aumento de PCO 2 é detectado porque o CO 2 se difunde na célula, onde aumenta a concentração de ácido carbônico e, portanto, de prótons . O mecanismo preciso de detecção de CO 2 é desconhecido, no entanto, foi demonstrado que o CO 2 e o baixo pH inibem uma condutância de potássio semelhante a TASK, reduzindo a corrente de potássio. Isso leva à despolarização da membrana celular que leva à entrada de Ca 2+ , excitação das células glômicas e consequente liberação de neurotransmissores.
Arterial acidose (quer metabólica ou de alterada P CO 2 ) inibe transportadores ácido-base (por exemplo, Na + -H + ) que aumentar o pH intracelular , activa e transportadores (por exemplo, Cl - -HCO 3 - ) que diminuem a ele. Mudanças na concentração de prótons causadas pela acidose (ou o oposto da alcalose ) dentro da célula estimulam as mesmas vias envolvidas na detecção do PCO 2 .
Outro mecanismo é através dos canais de potássio sensíveis ao oxigênio. Uma queda no oxigênio dissolvido leva ao fechamento desses canais, o que resulta na despolarização. Isso leva à liberação do neurotransmissor dopamina no glossofaríngeo e aferente vago para a área vasomotora.
Potencial de acção
As células do tipo I (glômicas) na carótida (e nos corpos aórticos) são derivadas da neuroectoderme e, portanto, são eletricamente excitáveis. Uma diminuição na pressão parcial de oxigênio, um aumento na pressão parcial de dióxido de carbono e uma diminuição no pH arterial podem causar despolarização da membrana celular e afetam isso bloqueando as correntes de potássio . Essa redução no potencial de membrana abre canais de cálcio dependentes de voltagem, o que causa um aumento na concentração de cálcio intracelular. Isso causa exocitose de vesículas contendo uma variedade de neurotransmissores , incluindo acetilcolina , noradrenalina , dopamina , adenosina , ATP , substância P e metencefalina . Estes atuam em receptores nas fibras nervosas aferentes que se encontram em aposição à célula glômica para causar um potencial de ação.
Retransmissão
O feedback do corpo carotídeo é enviado aos centros cardiorrespiratórios na medula oblonga por meio dos ramos aferentes do nervo glossofaríngeo . As fibras eferentes dos quimiorreceptores do corpo aórtico são transmitidas pelo nervo vago . Esses centros, por sua vez, regulam a respiração e a pressão arterial, com a hipóxia causando um aumento na ventilação.
Significado clínico

Paraganglioma
Um paraganglioma é um tumor que pode envolver o corpo carotídeo e geralmente é benigno . Raramente, um neuroblastoma maligno pode originar-se do corpo carotídeo.
Referências
links externos
- Javier Villadiego, Reposo Ramírez-Lorca, Fernando Cala, José L Labandeira-García, Mariano Esteban, Juan J Toledo-Aral, José López-Barneo: A infecção do corpo carotídeo é responsável pela hipoxemia silenciosa em pacientes com COVID-19? . In: Function, Volume 2, Issue 1, 2021. Oxford Academic. Publicado: 23 de novembro de 2020. zqaa032 doi: 10.1093 / function / zqaa032 . Ao longo:
- Uma nova explicação assustadora para a falta de oxigenação do sangue em muitos pacientes com COVID-19 . Ativado: SciTechDaily. 29 de dezembro de 2020. Fonte: Universidade de Sevilha
- Uma explicação para a falta de oxigenação do sangue detectada em muitos pacientes com COVID-19 . Ligado: EurekAlert! 29 de dezembro de 2020. Fonte: Universidade de Sevilha
