ácido cloroso - Chlorous acid
| |

| |
| nomes | |
|---|---|
|
nome IUPAC
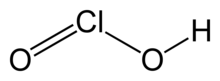
ácido cloroso
| |
| identificadores | |
|
Modelo 3D ( JSmol )
|
|
| Chebi | |
| ChemSpider | |
| KEGG | |
|
PubChem CID
|
|
| |
| |
| propriedades | |
| H Cl O 2 | |
| Massa molar | 68,46 g / mol |
| Acidez (p K um ) | 1,96 |
| Base conjugada | chlorite |
|
Excepto quando indicado de outra maneira, os dados são dados para materiais no seu estado normal (a 25 ° C [77 ° F], 100 kPa). | |
|
<Ver TFM> verificar ( o que é <Ver TFM> ?)
| |
| referências de Infobox | |
Ácido cloroso é um composto inorgânico com a fórmula HClO 2 . É um ácido fraco . Cloro tem estado de oxidação três neste ácido. A substância pura é instável, disproportionating de ácido hipocloroso (Cl estado de oxidação 1) e ácido clorídrico (Cl estado de oxidação 5):
- 2 HClO 2 → HClO + HClO 3
Embora o ácido é difícil de obter em substância pura, a base conjugada, clorito , derivado deste ácido é estável. Um exemplo de um sal de anião presente é o bem conhecido de clorito de sódio . Este e sais relacionados são por vezes usados na produção de dióxido de cloro .
Preparação
HClO 2 pode ser preparado através da reacção de bário ou cloreto de chumbo e diluir o ácido sulfúrico :
- Ba (ClO 2 ) 2 + H 2 SO 4 → BaSO 4 + 2 HClO 2
- Pb (ClO 2 ) 2 + H 2 SO 4 → PBSO 4 + 2 HClO 2
Estabilidade
ácido cloroso é um poderoso agente oxidante, ainda que a sua tendência para a desproporcionação neutraliza o seu potencial de oxidação.
O cloro é o único halogéneo para formar um ácido de fórmula isolável HXO 2 . Nem ácido bromous nem ácido iodous já foi isolado. Alguns sais de ácido bromous , bromites, são conhecidos, mas não há iodites .
Referências
![]() Mídia relacionadas com ácido cloroso no Wikimedia Commons
Mídia relacionadas com ácido cloroso no Wikimedia Commons
- ^ Um b Egon Wiberg, Arnold Frederick Holleman (2001) Inorganic Chemistry , Elsevier ISBN 0-12-352651-5
| Este inorgânico composto relacionados com o artigo é um esboço . Você pode ajudar a Wikipédia expandindo-o . |
