geometria de coordenação - Coordination geometry
O termo geometria de coordenação é utilizado num certo número de campos relacionados, de química e de estado sólido química / física.
Conteúdo
moléculas
A geometria de coordenação de um átomo é o padrão geométrico formado por átomos de ao redor do átomo central.
complexos de coordenação inorgânicos
No campo dos complexos de coordenação inorgânico é o padrão geométrico formado pelos átomos nos ligandos que estão ligados ao átomo central de uma molécula ou um complexo de coordenação . A disposição geométrica irá variar de acordo com o número e tipo de ligandos ligados ao centro metálico, e com a preferência coordenação do átomo central, tipicamente um metal em um complexo de coordenação . O número de átomos ligados, (isto é, o número de s-laços entre átomo central e ligandos) é denominado o número de coordenação . O padrão geométrico pode ser descrito como um poliedro , onde os vértices do poliedro são os centros dos átomos de coordenação nas ligandos.
A preferência de coordenação de um metal varia muitas vezes com o seu estado de oxidação. O número de ligações de coordenação ( número de coordenação ) pode variar de dois tão elevada como 20 em Th (η 5 -C 5 H 5 ) 4 .
Uma das geometrias de coordenação mais comuns é octaédrica , onde seis ligandos estão coordenados ao metal em uma distribuição simétrica, levando à formação de um octaedro se linhas foram desenhadas entre os ligandos. Outras geometrias de coordenação comuns são tetrahedral e planar quadrado .
Teoria do campo cristalino pode ser usado para explicar as estabilidades relativas de compostos de metais de transição de diferente geometria de coordenação, assim como a presença ou ausência de paramagnetismo , enquanto VSEPR podem ser usadas para complexos de elemento do grupo principal para prever geometria.
uso de cristalografia
Em uma estrutura de cristal a geometria de coordenação de um átomo é o padrão geométrico de átomos de coordenação onde a definição de átomos de coordenação depende do modelo de ligação utilizado. Por exemplo, na estrutura de rocha iónico sal cada átomo de sódio tem seis iões próximos de cloreto de vizinho em uma geometria octaédrica e cada cloreto tem similarmente seis próximos iões vizinho de sódio em uma geometria octaédrica. Em metais com a estrutura cúbica centrada no corpo (BCC) cada átomo tem oito vizinhos mais próximos em uma geometria cúbico. Em metais com a estrutura cúbica (FCC) de face centrada cada átomo tem doze vizinhos mais próximos de um cuboctahedral geometria.
Tabela de geometrias de coordenação
Uma tabela das geometrias de coordenação verificadas é mostrado a seguir, com exemplos de sua ocorrência em complexos encontrados como unidades discretas em compostos e esferas de coordenação ao redor de átomos em cristais (em que não há complexo discreto).
| Número de coordenação | Geometria | Exemplos de complexo discreto (finito) | Exemplos em cristais | |
|---|---|---|---|---|
| 2 | linear |
|
Ag (CN) 2 - em kag (CN) 2 | Ag em cianeto de prata , Au em AUI |
| 3 | planar trigonal |

|
HgI 3 - | O em TiO 2 estrutura rutilo |
| 4 | tetrahedral |

|
CoCl 4 2- | Zn e S em sulfureto de zinco , Si em dióxido de silício |
| 4 | planar quadrada |

|
AgF 4 - | CuO |
| 5 | trigonal bipiramidal |

|
SnCl 5 - | |
| 5 | piramidal quadrado |

|
InCl 5 2- na (NEt 4 ) 2 InCl 5 | |
| 6 | octaédrico |

|
Fe (H 2 O) 6 2+ | Na e Cl em NaCl |
| 6 | prismática trigonal |

|
W (CH 3 ) 6 | Como em NiAs , Mo em MoS 2 |
| 7 | bipiramidal pentagonal |

|
ZRF 7 3- em (NH 4 ) 3 ZRF 7 | Pa em PACL 5 |
| 7 | octahedral tampado |

|
MF 7 - | La em A-La 2 O 3 |
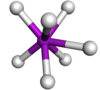
| 7 | tampado trigonal prismática |
|
TaF 7 2- em K 2 TaF 7 | |
| 8 | antiprismatic quadrado |

|
TaF 8 3- em Na 3 TaF 8 Zr (H 2 O) 8 4+ do aqua complexo |
Tório (IV) de iodeto de |
| 8 |
dodecaédrico (nota: enquanto este é o termo geralmente utilizado, o termo correcta é "bisdisphenoid" ou " disphenoid achatado ", como este é um poliedro deltaedro ) |

|
Mo (CN) 8 4- , em K 4 [Mo (CN) 8 ] .2H 2 O | Zr em K 2 ZRF 6 |
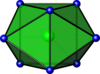
| 8 | bicapped trigonal prismática |
|
ZRF 8 4- | pUBR 3 |
| 8 | cúbico | Cloreto de césio , fluoreto de cálcio | ||
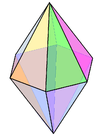
| 8 | bipiramidal hexagonal |
|
N em Li 3 N | |
| 8 | octahedral, trans-bicapped | Ni em arsenieto de níquel , NiAs; 6 Como vizinhos + 2 Ni capeamento | ||
| 8 | trigonal prismática, bicapped face triangular | Ca no café 2 O 4 | ||
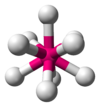
| 9 | tricapped trigonal prismática |
|
[ReH 9 ] 2- em nonahydridorhenate potássio Th (H 2 O) 9 4+ do aqua complexo |
SrCl 2 .6H 2 O, em Th RbTh 3 M 13 |
| 9 | antiprismatic quadrado tampado |

|
[Th (tropolonate) 4 (H 2 O)] | La no final 2 |
| 10 | antiprismatic quadrado bicapped | Th (C 2 O 4 ) 4 2- | ||
| 11 | Th em [Th IV (NO 3 ) 4 (H 2 O) 3 ] (NO 3 - é bidentado) | |||
| 12 | icosaedro |

|
Th em Th (NO 3 ) 6 2- iónica em Mg [Th (NO 3 ) 6 ] .8H 2 O | |
| 12 | cuboctahedron |

|
Zr IV (η 3 - (BH 4 ) 4 ) | átomos de metais de FCC , por exemplo, Ca |
| 12 | anticuboctahedron ( orthobicupola triangular ) |

|
átomos de metais HCP por exemplo Sc | |
| 14 | bicapped antiprismatic hexagonal | L (BH 4 ) 4 |
Nomeação de compostos inorgânicos
IUPAC introduziram o símbolo poliédrico como parte da sua nomenclatura da IUPAC de 2005 inorgânicos recomendações química para descrever a geometria em torno de um átomo de um composto.
IUCr propuseram um símbolo que é mostrado como um sobrescrito em parêntesis rectos na fórmula química. Por exemplo, CaF 2 seria Ca [8cb] F 2 [4t] , onde [8cb] significa coordenação cúbico e [4t] significa tetraédrica. Os símbolos equivalentes em IUPAC são CU -8 e T -4 respectivamente.
O símbolo IUPAC é aplicável para complexos de moléculas e que a proposta IUCr se aplica a sólidos cristalinos.
