Cloreto de cobre (I) - Copper(I) chloride
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Cloreto de cobre (I)
|
|
| Outros nomes
Cloreto cuproso
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 8127933 | |
| ChEBI | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard |
100.028.948 |
| Número EC | |
| 13676 | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| CuCl | |
| Massa molar | 98,999 g / mol |
| Aparência | pó branco, ligeiramente verde de impurezas oxidadas |
| Densidade | 4,14 g / cm 3 |
| Ponto de fusão | 423 ° C (793 ° F; 696 K) |
| Ponto de ebulição | 1.490 ° C (2.710 ° F; 1.760 K) (decompõe-se) |
| 0,047 g / L (20 ° C) | |
|
Produto de solubilidade ( K sp )
|
1,72 × 10 −7 |
| Solubilidade | insolúvel em etanol , acetona ; solúvel em HCl concentrado , NH 4 OH |
| Gap de banda | 3,25 eV (300 K, direto) |
| -40,0 · 10 −6 cm 3 / mol | |
|
Índice de refração ( n D )
|
1.930 |
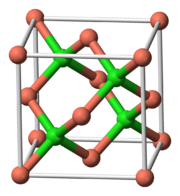
| Estrutura | |
| Zincblende , cF20 | |
| F 4 3m, No. 216 | |
|
a = 0,54202 nm
|
|
|
Volume da rede ( V )
|
0,1592 nm 3 |
|
Unidades de fórmula ( Z )
|
4 |
| Perigos | |
| Ficha de dados de segurança | JT Baker |
| Pictogramas GHS |
 
|
| Palavra-sinal GHS | Aviso |
| H302 , H400 , H410 | |
| P264 , P270 , P273 , P301 + 312 , P330 , P391 , P501 | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
140 mg / kg |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
TWA 1 mg / m 3 (como Cu) |
|
REL (recomendado)
|
TWA 1 mg / m 3 (como Cu) |
|
IDLH (perigo imediato)
|
TWA 100 mg / m 3 (como Cu) |
| Compostos relacionados | |
|
Outros ânions
|
Brometo de cobre (I) Iodeto de cobre (I) |
|
Outros cátions
|
Cloreto de cobre (II) Cloreto de prata (I) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O cloreto de cobre (I) , comumente chamado de cloreto cuproso , é o cloreto inferior do cobre , com a fórmula CuCl. A substância é um sólido branco moderadamente solúvel em água, mas muito solúvel em ácido clorídrico concentrado . Amostras impuras aparecem verdes devido à presença de cloreto de cobre (II) (CuCl 2 ).
História
O cloreto de cobre (I) foi preparado pela primeira vez por Robert Boyle em meados do século XVII a partir do cloreto de mercúrio (II) ("sublimado veneziano") e do metal de cobre:
- HgCl 2 + 2 Cu → 2 CuCl + Hg
Em 1799, JL Proust caracterizou os dois cloretos de cobre diferentes. Ele preparou o CuCl aquecendo o CuCl 2 em fogo vermelho na ausência de ar, fazendo com que perdesse metade de seu cloro combinado, seguido pela remoção do CuCl 2 residual por lavagem com água.
Uma solução ácida de CuCl foi usada anteriormente para análise do teor de monóxido de carbono em gases, por exemplo, no aparelho de gás de Hempel. Essa aplicação foi significativa durante o século XIX e início do século XX, quando o gás de carvão era amplamente usado para aquecimento e iluminação.
Síntese
O cloreto de cobre (I) é produzido industrialmente pela combinação direta de cobre metálico e cloro a 450–900 ° C:
O cloreto de cobre (I) também pode ser preparado reduzindo o cloreto de cobre (II) com dióxido de enxofre ou com ácido ascórbico ( vitamina C ) que atua como um açúcar redutor :
Muitos outros agentes redutores podem ser usados.
Propriedades
O cloreto de cobre (I) tem a estrutura cristalina de zincblenda cúbica em condições ambientais. Após o aquecimento a 408 ° C, a estrutura muda para hexagonal. Várias outras formas cristalinas de CuCl aparecem em altas pressões (vários GPa).
O cloreto de cobre (I) é um ácido de Lewis classificado como macio de acordo com o conceito Hard-Soft Acid-Base . Assim, forma uma série de complexos com bases de Lewis moles , como trifenilfosfina :
- CuCl + 1 P (C 6 H 5 ) 3 → 1/4 {CuCl [P (C 6 H 5 ) 3 ]} 4
- CuCl + 2 P (C 6 H 5 ) 3 → CuCl [P (C 6 H 5 ) 3 )] 2
- CuCl + 3 P (C 6 H 5 ) 3 → CuCl [P (C 6 H 5 ) 3 )] 3
Embora o CuCl seja insolúvel em água , ele se dissolve em soluções aquosas contendo moléculas doadoras adequadas. Forma complexos com íons haleto , por exemplo, formando H 3 O + CuCl 2 - em ácido clorídrico concentrado . O cloreto é deslocado por CN - e S 2 O 3 2− .
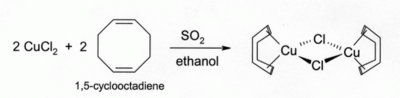
Soluções de CuCl em HCl ou NH 3 absorvem monóxido de carbono para formar complexos incolores, como o dímero com ponte de cloreto [CuCl (CO)] 2 . As mesmas soluções de ácido clorídrico também reagem com gás acetileno para formar [CuCl (C 2 H 2 )]. Soluções amoniacais de CuCl reagem com acetilenos para formar o explosivo acetileto de cobre (I) , Cu 2 C 2 . Os complexos de alceno podem ser preparados por redução de CuCl 2 por dióxido de enxofre na presença do alceno em solução de álcool . Complexos com dienos , como 1,5-ciclooctadieno, são particularmente estáveis:
Na ausência de outros ligantes, suas soluções aquosas são instáveis em relação à desproporção :
- 2 CuCl → Cu + CuCl 2
Em parte por esta razão, as amostras no ar assumem uma coloração verde.
Usos
O principal uso do cloreto de cobre (I) é como precursor do fungicida oxicloreto de cobre . Para este propósito, o cloreto de cobre (I) aquoso é gerado por comproporcionamento e, em seguida, oxidado pelo ar:
- Cu + CuCl 2 → 2 CuCl
- 4 CuCl + O 2 + 2 H 2 O → Cu 3 Cl 2 (OH) 4 + CuCl 2
O cloreto de cobre (I) catalisa uma variedade de reações orgânicas , como discutido acima. Sua afinidade pelo monóxido de carbono na presença de cloreto de alumínio é explorada no processo COPure SM .
Em síntese orgânica
CuCl é usado com monóxido de carbono , cloreto de alumínio e cloreto de hidrogênio na reação de Gatterman-Koch para formar benzaldeídos.
Na reação de Sandmeyer . O tratamento de um sal de arenodiazônio com CuCl leva a um cloreto de arila, por exemplo:
A reação tem amplo escopo e geralmente dá bons rendimentos.
Os primeiros investigadores observaram que os haletos de cobre (I) catalisam a adição de 1,4 de reagentes de Grignard às cetonas alfa, beta-insaturadas, levando ao desenvolvimento de reagentes organocuprato que são amplamente usados hoje em síntese orgânica :
Essa descoberta levou ao desenvolvimento da química de organocobre . Por exemplo, CuCl reage com metil - lítio (CH 3 Li) para formar " reagentes de Gilman ", como (CH 3 ) 2 CuLi, que encontram uso extensivo em síntese orgânica . Os reagentes de Grignard formam compostos organocobre semelhantes. Embora outros compostos de cobre (I) como o iodeto de cobre (I) sejam agora mais usados para esses tipos de reações, o cloreto de cobre (I) ainda é recomendado em alguns casos:
Aqui, Bu indica um grupo n- butil . Sem CuCl, o reagente de Grignard sozinho dá uma mistura de produtos de adição 1,2 e 1,4 (isto é, o butil adiciona no C mais próximo do C = O).
O cloreto de cobre (I) também é um intermediário formado a partir do cloreto de cobre (II) no processo Wacker .
Em química de polímeros
CuCl é usado como um catalisador na Polimerização Radical de Transferência Atômica (ATRP).
Nicho usa
O cloreto de cobre (I) também é usado em pirotecnia como um agente de coloração azul / verde. Em um teste de chama , os cloretos de cobre, como todos os compostos de cobre, emitem verde-azul.
Ocorrência natural
A forma natural de CuCl é a rara nantokita mineral .
Referências
links externos
- Inventário Nacional de Poluentes - Ficha técnica de cobre e compostos
- O processo COPure SM para purificação de CO utilizando um complexo de cloreto de cobre