Cloreto de cobre (II) - Copper(II) chloride
 Anidro
|
|
 Anidro
|
|
 Diidrato
|
|
| Nomes | |
|---|---|
| Outros nomes
Cloreto cúprico
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 8128168 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard |
100.028.373 |
| Número EC | |
| 9300 | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | 2802 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| CuCl 2 | |
| Massa molar | 134,45 g / mol (anidro) 170,48 g / mol (di-hidratado) |
| Aparência | sólido amarelo-marrom (anidro) sólido azul-esverdeado (di-hidratado) |
| Odor | inodoro |
| Densidade | 3,386 g / cm 3 (anidro) 2,51 g / cm 3 (di-hidratado) |
| Ponto de fusão | 498 ° C (928 ° F; 771 K) (anidro) 100 ° C (desidratação de diidrato) |
| Ponto de ebulição | 993 ° C (1.819 ° F; 1.266 K) (anidro, decompõe-se) |
| 70,6 g / 100 mL (0 ° C) 75,7 g / 100 mL (25 ° C) 107,9 g / 100 mL (100 ° C) |
|
| Solubilidade |
metanol: 68 g / 100 mL (15 ° C)
|
| + 1080 · 10 -6 cm 3 / mol | |
| Estrutura | |
| estrutura distorcida de CdI 2 | |
| Octaédrico | |
| Perigos | |
| Ficha de dados de segurança | Fisher Scientific |
| Pictogramas GHS |
   
|
| Palavra-sinal GHS | Perigo |
| H301 , H302 , H312 , H315 , H318 , H319 , H335 , H400 , H410 , H411 | |
| P261 , P264 , P270 , P271 , P273 , P280 , P301 + 310 , P301 + 312 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P310 , P312 , P321 , P322 , P330 , P332 + 313 , P337 + 313 , P362 , P363 , P391 , P403 + 233 , P405 , P501 | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
TWA 1 mg / m 3 (como Cu) |
|
REL (recomendado)
|
TWA 1 mg / m 3 (como Cu) |
|
IDLH (perigo imediato)
|
TWA 100 mg / m 3 (como Cu) |
| Compostos relacionados | |
|
Outros ânions
|
Fluoreto de cobre (II) Brometo de cobre (II) |
|
Outros cátions
|
Cloreto de cobre (I) Cloreto de prata Cloreto de ouro (III) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O cloreto de cobre (II) é o composto químico com a fórmula química CuCl 2 . A forma anidra é marrom amarelada, mas absorve lentamente a umidade para formar um diidrato verde-azulado .
Ambas as formas anidra e di-hidratada ocorrem naturalmente como os minerais muito raros tolbachita e eriochalcita , respectivamente.
Estrutura
O CuCl 2 anidro adota uma estrutura distorcida de iodeto de cádmio . Neste motivo, os centros de cobre são octaédricos . A maioria dos compostos de cobre (II) exibe distorções da geometria octaédrica idealizada devido ao efeito Jahn-Teller , que neste caso descreve a localização de um elétron-d em um orbital molecular que é fortemente anti-aderente em relação a um par de ligantes de cloreto. Em CuCl 2 · 2H 2 O, o cobre novamente adota uma geometria octaédrica altamente distorcida, os centros de Cu (II) sendo circundados por dois ligantes de água e quatro ligantes de cloreto, que se ligam assimetricamente a outros centros de Cu.
O cloreto de cobre (II) é paramagnético . De interesse histórico, CuCl 2 · 2H 2 O foi usado nas primeiras medições de ressonância paramagnética de elétrons por Yevgeny Zavoisky em 1944.
Propriedades e reações
A solução aquosa preparada com cloreto de cobre (II) contém uma variedade de complexos de cobre (II) dependendo da concentração, temperatura e presença de íons cloreto adicionais. Essas espécies incluem a cor azul de [Cu (H 2 O) 6 ] 2+ e a cor amarela ou vermelha dos complexos de haleto da fórmula [CuCl 2 + x ] x− .
Hidrólise
O hidróxido de cobre (II) precipita ao tratar soluções de cloreto de cobre (II) com base:
- CuCl 2 + 2 NaOH → Cu (OH) 2 + 2 NaCl

A hidrólise parcial dá trihidróxido de cloreto de dicobre , Cu 2 (OH) 3 Cl, um fungicida popular.
Redox
O cloreto de cobre (II) é um oxidante suave. Ele se decompõe em cloreto de cobre (I) e cloro gasoso próximo a 1000 ° C:
- 2 CuCl 2 → 2 CuCl + Cl 2
O cloreto de cobre (II) (CuCl 2 ) reage com vários metais para produzir cobre metálico ou cloreto de cobre (I) (CuCl) com a oxidação do outro metal. Para converter cloreto de cobre (II) em cloreto de cobre (I), pode ser conveniente reduzir uma solução aquosa com dióxido de enxofre como redutor:
- 2 CuCl 2 + SO 2 + 2 H 2 O → 2 CuCl + 2 HCl + H 2 SO 4
Complexos de coordenação
CuCl 2 reage com HCl ou outras fontes de cloreto para formar íons complexos: o CuCl 3 vermelho - (na realidade é um dímero, Cu 2 Cl 6 2− , um par de tetraedros que compartilham uma borda) e o CuCl verde ou amarelo 4 2− .
-
CuCl
2+ Cl-
⇌ CuCl-
3 -
CuCl
2+ 2 Cl-
⇌ CuCl2−
4
Alguns desses complexos podem ser cristalizados em solução aquosa e adotam uma ampla variedade de estruturas.
O cloreto de cobre (II) também forma uma variedade de complexos de coordenação com ligantes , como amônia , piridina e óxido de trifenilfosfina :
- CuCl 2 + 2 C 5 H 5 N → [CuCl 2 (C 5 H 5 N) 2 ] (tetragonal)
- CuCl 2 + 2 (C 6 H 5 ) 3 PO → [CuCl 2 ((C 6 H 5 ) 3 PO) 2 ] (tetraédrico)
No entanto, ligantes "suaves", como fosfinas (por exemplo, trifenilfosfina ), iodeto e cianeto , bem como algumas aminas terciárias, induzem a redução para dar complexos de cobre (I).
Preparação
O cloreto de cobre (II) é preparado comercialmente pela ação da cloração do cobre. O cobre no calor vermelho (300-400 ° C) combina diretamente com o gás cloro, dando cloreto de cobre (II) (fundido). A reação é muito exotérmica.
- Cu ( s ) + Cl 2 ( g ) → CuCl 2 ( l )
Também é comercialmente prático combinar óxido de cobre (II) com um excesso de cloreto de amônio em temperaturas semelhantes, produzindo cloreto de cobre, amônia e água:
- CuO + 2NH 4 Cl → CuCl 2 + 2NH 3 + H 2 O
Embora o metal de cobre em si não possa ser oxidado por ácido clorídrico , bases contendo cobre, como o hidróxido, óxido ou carbonato de cobre (II), podem reagir para formar CuCl 2 em uma reação ácido-base .
Uma vez preparada, uma solução de CuCl 2 pode ser purificada por cristalização . Um método padrão usa a solução misturada em ácido clorídrico diluído quente e faz com que os cristais se formem por resfriamento em um banho de cloreto de cálcio (CaCl 2 ) .
Existem meios indiretos e raramente usados de usar íons de cobre em solução para formar cloreto de cobre (II). A eletrólise de cloreto de sódio aquoso com eletrodos de cobre produz (entre outras coisas) uma espuma azul esverdeada que pode ser coletada e convertida em hidrato. Embora isso geralmente não seja feito devido à emissão de gás cloro tóxico e à prevalência do processo cloroalcal mais geral , a eletrólise converterá o metal cobre em íons de cobre na solução que forma o composto. Na verdade, qualquer solução de íons de cobre pode ser misturada com ácido clorídrico e transformada em cloreto de cobre removendo quaisquer outros íons.
Ocorrência natural
O cloreto de cobre (II) ocorre naturalmente como o muito raro mineral anidro tolbachita e o diidrato eriochalcita. Ambos são encontrados perto de fumarolas e em algumas minas de Cu. Mais comuns são os cloretos de oxihidróxido mistos como atacamita Cu 2 (OH) 3 Cl, surgindo entre as zonas de oxidação dos leitos de minério de Cu em clima árido (também conhecido por algumas escórias alteradas).
Usos
Co-catalisador no processo Wacker
Uma das principais aplicações industriais do cloreto de cobre (II) é como co-catalisador com cloreto de paládio (II) no processo Wacker . Neste processo, eteno (etileno) é convertido em etanal (acetaldeído) usando água e ar. Durante a reação, o PdCl 2 é reduzido a Pd , e o CuCl 2 serve para reoxidar este de volta a PdCl 2 . O ar pode então oxidar o CuCl resultante de volta a CuCl 2 , completando o ciclo.
- C 2 H 4 + PdCl 2 + H 2 O → CH 3 CHO + Pd + 2 HCl
- Pd + 2 CuCl 2 → 2 CuCl + PdCl 2
- 4 CuCl + 4 HCl + O 2 → 4 CuCl 2 + 2 H 2 O
O processo geral é:
- 2 C 2 H 4 + O 2 → 2 CH 3 CHO
Catalisador na produção de cloro
O cloreto de cobre (II) é usado como um catalisador em uma variedade de processos que produzem cloro por oxicloração . O processo Deacon ocorre a cerca de 400 a 450 ° C na presença de um cloreto de cobre:
- 4 HCl + O 2 → 2 Cl 2 + 2 H 2 O
O cloreto de cobre (II) catalisa a cloração na produção de cloreto de vinila e dicloroetano .
O cloreto de cobre (II) é usado no ciclo de cobre-cloro, no qual divide o vapor em um composto de oxigênio de cobre e cloreto de hidrogênio, sendo posteriormente recuperado no ciclo da eletrólise do cloreto de cobre (I).
Outras aplicações sintéticas orgânicas
O cloreto de cobre (II) tem algumas aplicações altamente especializadas na síntese de compostos orgânicos . Afeta a cloração de hidrocarbonetos aromáticos - isso geralmente é realizado na presença de óxido de alumínio . É capaz de clorar a posição alfa dos compostos de carbonila :
Esta reação é realizada em um solvente polar como a dimetilformamida (DMF), frequentemente na presença de cloreto de lítio , o que acelera a reação.
CuCl 2 , na presença de oxigênio , também pode oxidar fenóis . O produto principal pode ser direcionado para dar uma quinona ou um produto acoplado da dimerização oxidativa. O último processo fornece uma rota de alto rendimento para 1,1-binaftol :
Esses compostos são intermediários na síntese de BINAP e seus derivados.
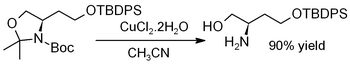
O cloreto de cobre (II) di-hidratado promove a hidrólise de acetonídeos , ou seja, para a desproteção para regenerar dióis ou aminoálcoois , como neste exemplo (onde TBDPS = terc- butildifenilsilil ):
CuCl 2 catalisa também o radical livre adição de cloretos de sulfonilo para alcenos ; a alfa-clorossulfona pode então sofrer eliminação com base para dar um produto de vinil sulfona .
Nicho usa
O cloreto de cobre (II) também é usado em pirotecnia como um agente de coloração azul / verde. Em um teste de chama , os cloretos de cobre, como todos os compostos de cobre, emitem verde-azul.
Em placas indicadoras de umidade (HICs), HICs de marrom a azul sem cobalto (base de cloreto de cobre (II)) podem ser encontrados no mercado. Em 1998, a Comunidade Europeia (CE) classificou itens contendo cloreto de cobalto (II) de 0,01 a 1% p / p como T (Tóxico), com a frase R correspondente de R49 (pode causar câncer se inalado). Como consequência, foram desenvolvidos novos cartões indicadores de umidade sem cobalto que contêm cobre.
Segurança
O cloreto de cobre (II) pode ser tóxico. Somente concentrações abaixo de 5 ppm são permitidas na água potável pela Agência de Proteção Ambiental dos EUA .
Referências
Leitura adicional
- Greenwood, Norman N .; Earnshaw, Alan (1997). Química dos Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- Lide, David R. (1990). Manual CRC de química e física: um livro de referência pronta de dados químicos e físicos . Boca Raton: CRC Press. ISBN 0-8493-0471-7.
- The Merck Index , 7ª edição, Merck & Co, Rahway, New Jersey, EUA, 1960.
- D. Nicholls, Complexes and First-Row Transition Elements , Macmillan Press, Londres, 1973.
- AF Wells, ' Structural Inorganic Chemistry , 5ª ed., Oxford University Press, Oxford, UK, 1984.
- J. March, Advanced Organic Chemistry , 4ª ed., P. 723, Wiley, New York, 1992.
- Fieser & Fieser Reagents for Organic Synthesis Volume 5, p158, Wiley, New York, 1975.
- DW Smith (1976). "Clorocupratos (II)". Revisões de Química de Coordenação . 21 (2–3): 93–158. doi : 10.1016 / S0010-8545 (00) 80445-2 .