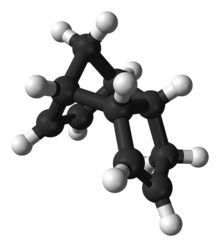
Diciclopentadieno - Dicyclopentadiene

|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Triciclo [5.2.1.0 2,6 ] deca-3,8-dieno
|
|
| Outros nomes
1,3-Diciclopentadieno, Biciclopentadieno, 3a, 4,7,7a-Tetrahidro-1 H -4,7-metanoindeno ( isômero endo : (3a R *, 4 S *, 7 R *, 7a S *) -, exo isômero: (3a S *, 4 S *, 7 R *, 7a R *) -)
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| Abreviações | DCPD |
| 1904092 | |
| ChemSpider | |
| ECHA InfoCard |
100.000.958 |
| Número EC | |
| KEGG | |
| Malha | Diciclopentadieno |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | ONU 2048 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 10 H 12 | |
| Massa molar | 132,20 g / mol |
| Aparência | Sólido cristalino incolor |
| Odor | desagradável, semelhante à cânfora |
| Densidade | 0,978 g / cm 3 |
| Ponto de fusão | 32,5 ° C (90,5 ° F; 305,6 K) |
| Ponto de ebulição | 170 ° C (338 ° F; 443 K) |
| 0,02% | |
| Solubilidade | muito solúvel em éter etílico , etanol solúvel em acetona , diclorometano , acetato de etila , n-hexano , tolueno |
| log P | 2,78 |
| Pressão de vapor | 180 Pa (20 ° C) |
| Perigos | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | 32 ° C (90 ° F; 305 K) |
| 503 ° C (937 ° F; 776 K) | |
| Limites explosivos | 0,8% -6,3% |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
Nenhum |
|
REL (recomendado)
|
TWA 5 ppm (30 mg / m 3 ) |
|
IDLH (perigo imediato)
|
WL |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
Diciclopentadieno , abreviado DCPD , é um composto químico com a fórmula C 10 H 12 . À temperatura ambiente, é um líquido límpido de cor amarelo claro com um odor acre. Sua densidade de energia é 10.975 Wh / l. O diciclopentadieno é coproduzido em grandes quantidades no steam cracking de nafta e gasóleo em etileno . O principal uso é em resinas , particularmente resinas de poliéster insaturado. Ele também é usado em tintas, adesivos e tintas.
Os sete principais fornecedores em todo o mundo juntos tinham uma capacidade anual em 2001 de 179 quilotoneladas (395 milhões de libras).
Síntese e estrutura
A dimerização espontânea de ciclopentadieno à temperatura ambiente para formar diciclopentadieno prossegue para cerca de 50% de conversão ao longo de 24 horas e produz o isômero endo em uma razão melhor que 99: 1 como o produto cineticamente favorecido (cerca de 150: 1 endo : exo a 80 ° C) . No entanto, o aquecimento prolongado resulta em isomerização para o isômero exo . O exo isômero puro foi primeiro preparado por eliminação mediada por base de hidroiodo- exo- diciclopentadieno. Termodinamicamente, o isômero exo é cerca de 0,7 kcal / mol mais estável do que o isômero endo .
Reações
Acima de 150 ° C, o diciclopentadieno sofre uma reação retro -Diels-Alder a uma taxa apreciável para produzir ciclopentadieno . A reação é reversível e à temperatura ambiente o ciclopentadieno dimeriza ao longo das horas para reformar o diciclopentadieno. O ciclopentadieno é um dieno útil nas reações de Diels-Alder, bem como um precursor de metalocenos na química organometálica . Não está disponível comercialmente como monômero, devido à rápida formação de diciclopentadieno; portanto, deve ser preparado "quebrando" o diciclopentadieno (aquecendo o dímero e isolando o monômero por destilação) pouco antes de ser necessário.
Os parâmetros termodinâmicos deste processo foram medidos. Em temperaturas acima de 125 ° C na fase de vapor, a dissociação em monômero de ciclopentadieno começa a se tornar termodinamicamente favorecida (a constante de dissociação K d = [ciclopentadieno] 2 / [diciclopentadieno]> 1 ). Por exemplo, os valores de K d a 149 ° C e 195 ° C foram encontrados como sendo 277 e 2200, respectivamente. Por extrapolação, K d é da ordem de 10–4 a 25 ° C, e a dissociação é desfavorecida. De acordo com os valores negativos de Δ H ° e Δ S ° para a reação de Diels-Alder, a dissociação do diciclopentadieno é mais termodinamicamente favorável em altas temperaturas. As medições da constante de equilíbrio implicam que Δ H ° = –18 kcal / mol e Δ S ° = –40 eu para a dimerização do ciclopentadieno.
A hidrogenação de diciclopentadieno dá endo- tetrahidridodiciclopentadieno ( dímero TH ), um combustível em aplicações militares. Na reação com cloreto de alumínio em temperatura elevada, este hidrocarboneto C 10 se reorganiza em adamantano .
O diciclopentadieno polimeriza . Os copolímeros são formados com etileno ou estireno . A " dupla ligação norborneno " participa. Usando a polimerização por metátese com abertura de anel, um homopolímero polidiciclopentadieno é formado.
A hidroformilação de DCP dá o dialdeído denominado dialdeído TCD (TCD = triciclodecano ). Este dialdeído pode ser oxidado ao ácido dicarboxílico e a um diol . Todos esses derivados têm alguma utilidade na ciência dos polímeros.
A hidrogenação de diciclopentadieno dá o derivado de C saturado 10 H 16 , o qual é submetido a rearranjo catalisado por ácido para adamantano .
Referências
- ^ Índice Merck , 11ª edição, 2744
- ^ a b c d e f g h Guia de bolso NIOSH para perigos químicos. "# 0204" . Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH).
- ^ Xu, Rui; Jocz, Jennifer N .; Wiest, Lisa K .; Sarngadharan, Sarath C .; Milina, Maria; Coleman, John S .; Iaccino, Larry L .; Pollet, Pamela; Sievers, Carsten; Liotta, Charles L. (05/09/2019). "Cinética de dimerização do ciclopentadieno na presença de alcenos e alcadienos C5". Pesquisa Química Industrial e de Engenharia . 58 (50): 22516–22525. doi : 10.1021 / acs.iecr.9b04018 . ISSN 0888-5885 .
- ^ Bartlett, Paul D .; Goldstein, Irving S. (1947-10-01). " exo- Diciclopentadieno". Journal of the American Chemical Society . 69 (10): 2553. doi : 10.1021 / ja01202a501 . ISSN 0002-7863 .
- ^ Narayan, Adithyaram; Wang, Beibei; Nava Medina, Ilse Belen; Mannan, M. Sam; Cheng, Zhengdong; Wang, Qingsheng (01/11/2016). "Predição de calor de formação para exo- Diciclopentadieno". Jornal de prevenção de perdas nas indústrias de processo . 44 : 433–439. doi : 10.1016 / j.jlp.2016.10.015 . ISSN 0950-4230 .
- ^ Wilson, Philip J .; Wells, Joseph H. (01/02/1944). "The Chemistry and Utilization of Cyclopentadiene". Revisões químicas . 34 (1): 1–50. doi : 10.1021 / cr60107a001 . ISSN 0009-2665 .
- ^ Lenz, Terry G .; Vaughan, John D. (01/02/1989). "Empregando cálculos de campo de força para prever constantes de equilíbrio e outras propriedades termodinâmicas para a dimerização de 1,3-ciclopentadieno". The Journal of Physical Chemistry . 93 (4): 1592–1596. doi : 10.1021 / j100341a081 . ISSN 0022-3654 .
- ^ Schleyer, Paul von R .; Donaldson, MM; Nicholas, RD; Cupas, C. (1973). "Adamantane" . Sínteses orgânicas .; Volume coletivo , 5 , p. 16
- ^ Li, Xiaofang; Hou, Zhaomin (2005). "Scandium-Catalyzed Copolymerization of Ethylene with Dicyclopentadiene and Terpolymerization of Ethylene, Dicyclopentadiene, and Styrene". Macromoléculas . 38 (16): 6767. bibcode : 2005MaMol..38.6767L . doi : 10.1021 / ma051323o .
- ^ Kohlpaintner, cristão; Schulte, Markus; Falbe, Jürgen; Lappe, Peter; Weber, Jürgen (2008). "Aldeídos, alifáticos". Enciclopédia de Química Industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a01_321.pub2 .
- ^ Hönicke, Dieter; Födisch, Ringo; Claus, Peter; Olson, Michael (2002). "Ciclopentadieno e ciclopenteno". Enciclopédia de Química Industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a08_227 .


