Dopamina beta-hidroxilase - Dopamine beta-hydroxylase
A dopamina beta-hidroxilase ( DBH ), também conhecida como dopamina beta-monooxigenase , é uma enzima ( EC 1.14.17.1 ) que em humanos é codificada pelo gene DBH . A dopamina beta-hidroxilase catalisa a conversão da dopamina em norepinefrina.
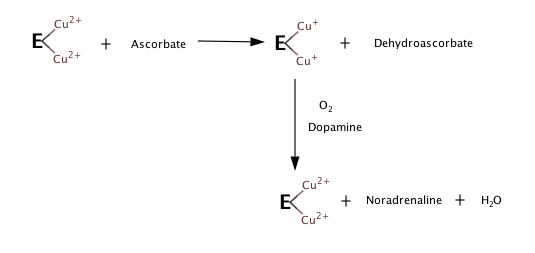
Os três substratos da enzima são dopamina , vitamina C (ascorbato) e O 2 . Os produtos são norepinefrina , desidroascorbato , e H 2 O .
DBH é uma oxigenase contendo cobre de 290 kDa que consiste em quatro subunidades idênticas e sua atividade requer ascorbato como cofator .
É a única enzima envolvida na síntese de neurotransmissores de pequenas moléculas ligados à membrana, tornando a norepinefrina o único transmissor conhecido sintetizado dentro das vesículas. É expresso em neurônios noradrenérgicos do sistema nervoso central (ou seja, locus coeruleus ) e sistemas nervosos periféricos (ou seja, gânglios simpáticos), bem como em células cromafins da medula adrenal .
Mecanismo de catálise
| dopamina beta-monooxigenase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| EC nº | 1.14.17.1 | ||||||||
| CAS no. | 9013-38-1 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologia Genética | AmiGO / QuickGO | ||||||||
| |||||||||
Com base nas observações do que acontece quando não há substrato, ou oxigênio, as etapas a seguir parecem constituir a reação de hidroxilação.
Embora os detalhes do mecanismo do DBH ainda não tenham sido confirmados, o DBH é homólogo a outra enzima, a peptidilglicina α-hidroxiladora monooxigenase (PHM). Como o DBH e o PHM compartilham estruturas semelhantes, é possível modelar o mecanismo de DBH com base no que se conhece sobre o mecanismo de PHM.
Especificidade do substrato
|
|
A dopamina beta-hidroxilase catalisa a hidroxilação não apenas da dopamina, mas também de outros derivados da feniletilamina, quando disponíveis. O requisito mínimo parece ser o esqueleto da feniletilamina : um anel de benzeno com uma cadeia lateral de dois carbonos que termina em um grupo amino.
Ensaios para atividade DBH em soro humano e líquido cefalorraquidiano
A atividade do DBH no soro humano pode ser estimada por método espectrofotométrico ou com o auxílio de cromatografia líquida de ultra alta performance com detector Photo Diode Array (UHPLC-PDA). Um ensaio sensível para a detecção da atividade DBH no líquido cefalorraquidiano usando cromatografia líquida de alta eficiência com detector eletroquímico (HPLC-ECD) também foi descrito anteriormente.
Expressão de loci de característica quantitativa (eQTLs) em loci DBH
Variantes genéticas, como polimorfismos de nucleotídeo único (SNPs) em loci DBH foram encontrados para estar associados com atividade DBH e são loci de traços quantitativos de expressão bem conhecidos . Variantes de alelos em dois SNPs reguladores, nomeadamente rs1611115 e rs1989787, mostraram afetar a transcrição deste gene. Mutações identificadas na deficiência de dopamina beta-hidroxilase e SNPs não sinônimos, como rs6271 neste gene, causaram secreção defeituosa da proteína do retículo endoplasmático.
Significado clínico
O DBH contribui principalmente para a biossíntese de catecolaminas e vestígios de aminas . Também participa do metabolismo dos xenobióticos relacionados a essas substâncias; por exemplo, a enzima DBH humana catalisa a beta-hidroxilação da anfetamina e para-hidroxianfetamina , produzindo norefedrina e para-hidroxinorefedrina, respectivamente.
DBH foi implicado como fator de correlação em condições associadas à tomada de decisão e drogas viciantes , por exemplo, alcoolismo e tabagismo, transtorno de déficit de atenção e hiperatividade , esquizofrenia e doença de Alzheimer . O DBH inadequado é denominado deficiência de dopamina beta-hidroxilase .
Os SNPs promotores proximais rs1989787 e rs1611115 foram encontrados para estar associados à cognição em indivíduos com Esquizofrenia . Além disso, esses SNPs (rs1989787; rs1611115) e uma variante distal do promotor 19bp Ins / Del (rs141116007) foram associados a pontuações da Escala de Movimento Involuntário Anormal em indivíduos com esquizofrenia positiva para discinesia tardia . Das três variantes, o promotor proximal SNP (rs1611115) foi associado aos escores da Escala de Síndrome Positiva e Negativa (PANSS) em indivíduos esquizofrênicos positivos para discinesia tardia .
Estrutura
Era difícil obter um cristal estável de dopamina beta-hidroxilase. Portanto, um modelo de homologia com base na sequência primária e comparação com PHM está disponível.

No entanto, uma estrutura de cristal também foi apresentada em 2016.
Regulação e inibição
Esta proteína pode usar o modelo de morfeína de regulação alostérica .
Inibidores
| HYD | HP | QCA | IQCA | BI | IAA | |
|---|---|---|---|---|---|---|
| Competitivo | Ascorbato | Ascorbato | Ascorbato | Ascorbato | Ascorbato | Ascorbato |
| Não-competitivo | Tiramina | Tiramina | ||||
| Misturado | Tiramina | Tiramina | Tiramina | Tiramina | ||
| Ascorbato é cofator; a tiramina é o substituto da dopamina, substrato homônimo do DBH | ||||||
O DBH é inibido pelo dissulfiram , tropolona e, mais seletivamente, pelo nepicastate .
DBH é reversivelmente inibido por l-2H-ftalazina hidrazona (hidralazina; HYD), 2-1H-piridinona hidrazona (2-hidrazinopiridina; HP), ácido 2-quinolina-carboxílico (QCA), ácido l-isoquinolinocarboxílico (IQCA), 2 , 2'-bi-lH-imidazol (2,2'-biimidazol; BI) e ácido IH-imidazol-4-acético (ácido imidazol-4-acético; IAA). HYD, QCA e IAA são alostéricos competitivos.
Nomenclatura
O nome sistemático desta classe de enzimas é 3,4-dihidroxifenetilamina, ascorbato: oxidoredutase de oxigênio (beta-hidroxilação) .
Outros nomes de uso comum incluem:
- dopamina beta-monooxigenase
- dopamina beta-hidroxilase
- dopamina beta-monooxigenase associada à membrana (MDBH)
- dopamina beta-monooxigenase solúvel (SDBH)
- dopamina-B-hidroxilase
- 3,4-dihidroxifenetilamina beta-oxidase
- 4- (2-aminoetil) pirocatecol beta-oxidase
- dopa beta-hidroxilase
- dopamina beta-oxidase
- dopamina hidroxilase
- fenilamina beta-hidroxilase
- (3,4-dihidroxifenetilamina) beta-mono-oxigenase
Referências
Leitura adicional
- Friedman S, Kaufman S (dezembro de 1965). "3,4-dihidroxifeniletilamina beta-hidroxilase. Propriedades físicas, conteúdo de cobre e papel do cobre na atividade catalítica" . The Journal of Biological Chemistry . 240 (12): 4763–73. doi : 10.1016 / S0021-9258 (18) 97021-3 . PMID 5846992 .
- Levin EY, Levenberg B, Kaufman S (1960). "A conversão enzimática de 3,4-dihidroxifeniletilamina em norepinefrina" . J. Biol. Chem . 235 (7): 2080–2086. doi : 10.1016 / S0021-9258 (18) 69366-4 . PMID 14416204 .
links externos
- Entrada GeneReviews / NIH / NCBI / UW na Deficiência de Dopamina Beta-Hidroxilase
- Dopamina + beta-hidroxilase nos títulos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)