Coeficientes de Einstein - Einstein coefficients
Os coeficientes de Einstein são quantidades matemáticas que medem a probabilidade de absorção ou emissão de luz por um átomo ou molécula. Os coeficientes de Einstein A estão relacionados à taxa de emissão espontânea de luz, e os coeficientes de Einstein B estão relacionados à absorção e emissão estimulada de luz.
Linhas espectrais
Na física , pensa-se em uma linha espectral de dois pontos de vista.
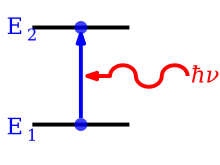
Uma linha de emissão é formada quando um átomo ou molécula faz uma transição de um determinado nível de energia discreto E 2 de um átomo, para um nível de energia mais baixo E 1 , emitindo um fóton de uma energia e comprimento de onda específicos. Um espectro de muitos desses fótons mostrará um pico de emissão no comprimento de onda associado a esses fótons.
Uma linha de absorção é formada quando um átomo ou molécula faz uma transição de um estado de energia discreta inferior, E 1 , para um estado de energia discreta superior, E 2 , com um fóton sendo absorvido no processo. Esses fótons absorvidos geralmente vêm da radiação contínua de fundo (o espectro completo da radiação eletromagnética) e um espectro mostrará uma queda na radiação contínua no comprimento de onda associado aos fótons absorvidos.
Os dois estados devem ser estados ligados em que o elétron está ligado ao átomo ou molécula, então a transição é algumas vezes referida como uma transição "ligada", em oposição a uma transição na qual o elétron é ejetado para fora do átomo completamente (transição "livre de limites") em um estado contínuo , deixando um átomo ionizado e gerando radiação contínua.
Um fóton com energia igual à diferença E 2 - E 1 entre os níveis de energia é liberado ou absorvido no processo. A frequência ν na qual a linha espectral ocorre está relacionada à energia do fóton pela condição de frequência de Bohr E 2 - E 1 = hν onde h denota a constante de Planck .
Coeficientes de emissão e absorção
Uma linha espectral atômica se refere a eventos de emissão e absorção em um gás em que é a densidade dos átomos no estado de energia superior para a linha e é a densidade dos átomos no estado de energia inferior para a linha.
A emissão da radiação da linha atômica na frequência ν pode ser descrita por um coeficiente de emissão com unidades de energia / (tempo x volume x ângulo sólido). ε dt dV dΩ é então a energia emitida por um elemento de volume no tempo em ângulo sólido . Para radiação de linha atômica,
onde é o coeficiente de Einstein para emissão espontânea, que é fixado pelas propriedades intrínsecas do átomo relevante para os dois níveis de energia relevantes.
A absorção da radiação da linha atômica pode ser descrita por um coeficiente de absorção com unidades de 1 / comprimento. A expressão κ 'dx fornece a fração da intensidade absorvida por um feixe de luz na frequência ν ao percorrer a distância dx . O coeficiente de absorção é dado por
onde e são os coeficientes de Einstein para absorção de fótons e emissão induzida, respectivamente. Como o coeficiente , eles também são fixados pelas propriedades intrínsecas do átomo relevante para os dois níveis de energia relevantes. Para a termodinâmica e para a aplicação da lei de Kirchhoff , é necessário que a absorção total seja expressa como a soma algébrica de dois componentes, descritos respectivamente por e , que podem ser considerados como absorção positiva e negativa, que são, respectivamente, o fóton direto. absorção, e o que é comumente chamado de emissão estimulada ou induzida.
As equações acima ignoraram a influência da forma da linha espectroscópica . Para serem precisas, as equações acima precisam ser multiplicadas pela forma da linha espectral (normalizada), caso em que as unidades serão alteradas para incluir um termo de 1 / Hz.
Em condições de equilíbrio termodinâmico, os densidades Número e , os coeficientes de Einstein, e a densidade de energia espectral fornecer informação suficiente para determinar as taxas de absorção e de emissão.
Condições de equilíbrio
As densidades Número e são definidas pelo estado físico do gás em que a linha espectral ocorre, incluindo o local de radiação espectral (ou, em algumas apresentações, o local de espectral radiante energia densidade). Quando esse estado é de equilíbrio termodinâmico estrito ou do chamado "equilíbrio termodinâmico local", então a distribuição dos estados atômicos de excitação (que inclui e ) determina as taxas de emissões e absorções atômicas para serem tais que a lei de Kirchhoff de igualdade de absortividade radiativa e emissividade se mantém. Em estrito equilíbrio termodinâmico, o campo de radiação é denominado radiação de corpo negro e é descrito pela lei de Planck . Para o equilíbrio termodinâmico local, o campo de radiação não precisa ser um campo de corpo negro, mas a taxa de colisões interatômicas deve exceder amplamente as taxas de absorção e emissão de quanta de luz, de modo que as colisões interatômicas dominam inteiramente a distribuição de estados de excitação atômica. Ocorrem circunstâncias em que o equilíbrio termodinâmico local não prevalece, porque os fortes efeitos radiativos superam a tendência à distribuição de Maxwell-Boltzmann das velocidades moleculares. Por exemplo, na atmosfera do Sol, a grande força da radiação domina. Na alta atmosfera da Terra, em altitudes acima de 100 km, a raridade das colisões intermoleculares é decisiva.
Nos casos de equilíbrio termodinâmico e de equilíbrio termodinâmico local , as densidades numéricas dos átomos, tanto excitadas como não excitadas, podem ser calculadas a partir da distribuição de Maxwell-Boltzmann , mas para outros casos (por exemplo, lasers ) o cálculo é mais complicado.
Coeficientes de Einstein
Em 1916, Albert Einstein propôs que existem três processos ocorrendo na formação de uma linha espectral atômica. Os três processos são chamados de emissão espontânea, emissão estimulada e absorção. A cada um está associado um coeficiente de Einstein, que é uma medida da probabilidade de ocorrência de um determinado processo. Einstein considerou o caso da radiação isotrópica de frequência ν e densidade de energia espectral ρ ( ν ) .
Várias formulações
Hilborn comparou várias formulações para derivações para os coeficientes de Einstein, por vários autores. Por exemplo, Herzberg trabalha com irradiância e número de onda; Yariv trabalha com energia por unidade de volume por unidade de intervalo de frequência, como é o caso na formulação mais recente (2008). Mihalas & Weibel-Mihalas trabalham com brilho e frequência; também Chandrasekhar; também Goody & Yung; Loudon usa frequência angular e brilho.
Emissão espontânea
A emissão espontânea é o processo pelo qual um elétron "espontaneamente" (isto é, sem qualquer influência externa) decai de um nível de energia superior para um inferior. O processo é descrito pelo coeficiente de Einstein A 21 ( s −1 ), que dá a probabilidade por unidade de tempo de um elétron no estado 2 com energia decair espontaneamente para o estado 1 com energia , emitindo um fóton com energia E 2 - E 1 = hν . Devido ao princípio da incerteza de energia-tempo , a transição realmente produz fótons dentro de uma faixa estreita de frequências chamada largura de linha espectral . Se for a densidade numérica de átomos no estado i , então a mudança na densidade numérica de átomos no estado 2 por unidade de tempo devido à emissão espontânea será
O mesmo processo resulta no aumento da população do estado 1:
Emissão estimulada
Emissão estimulada (também conhecida como emissão induzida) é o processo pelo qual um elétron é induzido a saltar de um nível de energia mais alto para um mais baixo pela presença de radiação eletromagnética na (ou próxima) à frequência da transição. Do ponto de vista termodinâmico, esse processo deve ser considerado uma absorção negativa. O processo é descrito pelo coeficiente de Einstein (m 3 J −1 s −2 ), que dá a probabilidade por unidade de tempo por unidade de radiância espectral do campo de radiação que um elétron no estado 2 com energia irá decair para o estado 1 com energia , emitindo um fóton com uma energia E 2 - E 1 = hν . A mudança na densidade do número de átomos no estado 1 por unidade de tempo devido à emissão induzida será
onde denota a radiância em uma largura de banda de 1 Hz do campo de radiação isotrópica na frequência da transição (ver lei de Planck ).
A emissão estimulada é um dos processos fundamentais que levaram ao desenvolvimento do laser . A radiação laser está, no entanto, muito longe do presente caso de radiação isotrópica.
Absorção de fóton
Absorção é o processo pelo qual um fóton é absorvido pelo átomo, fazendo com que um elétron salte de um nível de energia inferior para um superior. O processo é descrito pelo coeficiente de Einstein (m 3 J −1 s −2 ), que dá a probabilidade por unidade de tempo por unidade de radiância espectral do campo de radiação de que um elétron no estado 1 com energia absorva um fóton com energia E 2 - E 1 = hν e pule para o estado 2 com energia . A mudança na densidade do número de átomos no estado 1 por unidade de tempo devido à absorção será
Balanceamento detalhado
Os coeficientes de Einstein são probabilidades fixas por tempo associadas a cada átomo, e não dependem do estado do gás do qual os átomos fazem parte. Portanto, qualquer relação que possamos derivar entre os coeficientes em, digamos, equilíbrio termodinâmico será válida universalmente.
No equilíbrio termodinâmico, teremos um balanceamento simples, no qual a variação líquida no número de quaisquer átomos excitados é zero, sendo balanceado pela perda e ganho devido a todos os processos. Com relação às transições limitadas, teremos também um balanceamento detalhado , que afirma que a troca líquida entre quaisquer dois níveis será balanceada. Isso ocorre porque as probabilidades de transição não podem ser afetadas pela presença ou ausência de outros átomos excitados. O equilíbrio detalhado (válido apenas no equilíbrio) requer que a mudança no tempo do número de átomos no nível 1 devido aos três processos acima seja zero:
Junto com o equilíbrio detalhado, na temperatura T podemos usar nosso conhecimento da distribuição de energia de equilíbrio dos átomos, conforme declarado na distribuição de Maxwell-Boltzmann , e a distribuição de equilíbrio dos fótons, conforme declarado na lei de Planck da radiação do corpo negro para derivar relações universais entre os coeficientes de Einstein.
Da distribuição de Boltzmann temos para o número de espécies atômicas excitadas i :
onde n é a densidade numérica total da espécie atômica, excitada e não excitada, k é a constante de Boltzmann , T é a temperatura , é a degenerescência (também chamada de multiplicidade) do estado i e Z é a função de partição . Da lei de Planck da radiação de corpo negro na temperatura T temos para a radiância espectral (radiância é a energia por unidade de tempo por unidade de ângulo sólido por unidade de área projetada, quando integrada ao longo de um intervalo espectral apropriado) na frequência ν
Onde
onde está a velocidade da luz e é a constante de Planck .
Substituindo essas expressões na equação de equilíbrio detalhado e lembrando que E 2 - E 1 = hν resulta
separando para
A equação acima deve se manter em qualquer temperatura, então
e
Portanto, os três coeficientes de Einstein são inter-relacionados por
e
Quando essa relação é inserida na equação original, também se pode encontrar uma relação entre e , envolvendo a lei de Planck .
Forças do oscilador
A força do oscilador é definida pela seguinte relação com a seção transversal para absorção:
onde é a carga do elétron, é a massa do elétron e e são funções de distribuição normalizadas em frequência e frequência angular, respectivamente. Isso permite que todos os três coeficientes de Einstein sejam expressos em termos da força do oscilador único associada à linha espectral atômica particular:
Veja também
- Momento dipolo de transição
- Força do oscilador
- Distribuição Breit-Wigner
- Configuração eletronica
- Ressonância Fano
- Notação Siegbahn
- Espectroscopia atômica
- Radiação molecular , espectro contínuo emitido por moléculas
Referências
Bibliografia citada
- Bohr, N. (1913). "Sobre a constituição de átomos e moléculas" (PDF) . Revista Filosófica . 26 : 1-25. Bibcode : 1913PMag ... 26..476B . doi : 10.1080 / 14786441308634993 .
- Brillouin, L. (1970). Relatividade reexaminada . Academic Press . ISBN 978-0-12-134945-5.
- Chandrasekhar, S. (1950). Radiative Transfer , Oxford University Press, Oxford.
- Garrison, J. C., Chiao, R. Y. (2008). Quantum Optics , Oxford University Press, Oxford UK, ISBN 978-019-850-886-1 .
- Goody, R. M., Yung, Y. L. (1989). Atmospheric Radiation: Theoretical Basis , 2ª edição, Oxford University Press, Oxford, New York, 1989, ISBN 0-19-505134-3 .
- Heisenberg, W. (1925). "Über quantentheoretische Umdeutung kinematischer und mechanischer Beziehungen". Zeitschrift für Physik . 33 : 879–893. Bibcode : 1925ZPhy ... 33..879H . doi : 10.1007 / BF01328377 .Traduzido como "Reinterpretação teórica quântica das relações cinemáticas e mecânicas" em van der Waerden, BL (1967). Fontes de Mecânica Quântica . Publicação da Holanda do Norte . pp. 261–276.
- Herzberg, G. (1950). Molecular Spectroscopy and Molecular Structure , vol. 1, Diatomic Molecules , segunda edição, Van Nostrand, New York.
- Jammer, M. (1989). The Conceptual Development of Quantum Mechanics (segunda ed.). Tomash Publishers American Institute of Physics . ISBN 0-88318-617-9.
- Loudon, R. (1973/2000). The Quantum Theory of Light , (primeira edição 1973), terceira edição 2000, Oxford University Press, Oxford UK, ISBN 0-19-850177-3 .
- Mihalas, D., Weibel-Mihalas, B. (1984). Foundations of Radiation Hydrodynamics , Oxford University Press, New York ISBN 0-19-503437-6 .
- Sommerfeld, A. (1923). Estrutura Atômica e Linhas Espectrais . Brose, HL (trad.) (Da 3ª ed. Alemã). Methuen .
- Yariv, A. (1967/1989). Quantum Electronics , terceira edição, John Wiley & sons, New York, ISBN 0-471-60997-8 .
- Hubeny, Ivan; Mihalas, Dimitri (2015). Teoria das atmosferas estelares: uma introdução à análise espectroscópica quantitativa astrofísica de desequilíbrio . Princeton University Press. ISBN 9780691163291.
Outra leitura
- Condon, UE; Shortley, GH (1964). The Theory of Atomic Spectra . Cambridge University Press. ISBN 0-521-09209-4.
- Rybicki, GB; Lightman, AP (1985). Processos radiativos em astrofísica . John Wiley & Sons, Nova York. ISBN 0-471-82759-2.
- Shu, FH (1991). The Physics of Astrophysics . 1: Radiação. Livros de Ciências da Universidade, Mill Valley, CA. ISBN 0-935702-64-4.
- Robert C. Hilborn (2002). "Coeficientes de Einstein, seções transversais, valores de f, momentos de dipolo e tudo isso". arXiv : física / 0202029 .
- Taylor, MA; Vilchez, JM (2009). "Tutorial: soluções exatas para as populações do íon n-nível". Publicações da Astronomical Society of the Pacific . 121 (885): 1257–1266. arXiv : 0709.3473 . Bibcode : 2009PASP..121.1257T . doi : 10.1086 / 648121 .