Fluoração eletrofílica - Electrophilic fluorination
A fluoração eletrofílica é a combinação de um nucleófilo centrado no carbono com uma fonte eletrofílica de flúor para fornecer compostos organofluorados . Embora o flúor elementar e os reagentes que incorporam uma ligação oxigênio-flúor possam ser usados para esse propósito, eles foram amplamente substituídos por reagentes contendo uma ligação nitrogênio-flúor.
A fluoração eletrofílica oferece uma alternativa aos métodos de fluoração nucleofílicos que empregam fluoretos alcalinos ou de amônio e métodos que empregam fluoretos de enxofre para a preparação de compostos organofluorados. O desenvolvimento de reagentes de fluoração eletrofílicos sempre se concentrou na remoção da densidade do elétron do átomo ligado ao flúor; entretanto, compostos contendo ligações de nitrogênio-flúor provaram ser os agentes de fluoração eletrofílicos mais econômicos, estáveis e seguros. Os reagentes NF eletrofílicos são neutros ou catiônicos e podem possuir nitrogênio hibridizado sp 2 ou sp 3 . Embora o mecanismo preciso da fluoração eletrofílica não esteja claro, métodos altamente eficientes e estereosseletivos foram desenvolvidos.
Alguns agentes de fluoração comuns usados para síntese orgânica são N- fluor- o- benzenodisulfonimida (NFOBS), N- fluorobenzenossulfonimida (NFSI) e Selectfluor .
Mecanismo e estereoquímica
Mecanismo prevalecente
O mecanismo de fluoração eletrofílica permanece controverso. O que está em questão é se a reação prossegue por meio de um processo S N 2 ou de transferência de elétron único (SET). No suporte do mecanismo S N 2, os reagentes de aril Grignard e os aril - lítio dão rendimentos semelhantes de fluorobenzeno em combinação com N- fluoro- o- benzenodisulfonimida (NFOBS), embora as tendências desses reagentes para participarem nos processos SET difiram substancialmente. Além disso, as experiências de sondas radicais com éteres 5-hexenil e ciclopropil enol não deram quaisquer produtos rearranjados. Mais recentemente, estudos cinéticos sobre fluoração eletrofílica de uma série de derivados 1,3-dicarbonil por uma gama de reagentes NF sugeriram que o mecanismo S N 2 é mais provável através dos estudos de Eyring e Hammett .
Por outro lado, prevê-se que o tempo de vida dos radicais no processo SET seja quatro ordens de magnitude menor do que o limite de detecção mesmo da mais sensível das sondas radicais. Postulou-se que, após a transferência de elétrons, ocorre a recombinação imediata do radical flúor com o radical alquil.
Variantes estereosseletivas
As fluorações estereosseletivas podem ser diastereosseletivas ou enantiosseletivas. Os métodos diastereosseletivos têm se concentrado no uso de auxiliares quirais no substrato nucleofílico. Para fluorações de compostos de carbonila , oxazolidinonas quirais têm sido usadas com sucesso.
A adição de conjugado em tandem incorporando um nucleófilo quiral foi usada para sintetizar ésteres β-amino α-fluoro em forma quiral, não racêmica.
Os métodos enantiosseletivos empregam quantidades estequiométricas de agentes de fluoração quirais. Os sais de N- fluoroamónio dos alcalóides da cinchona representam o estado da arte para reacções deste tipo. Além disso, esses reagentes são facilmente sintetizados a partir do Selectfluor e dos alcalóides parentais.
Escopo e limitações
Reagentes de fluoração
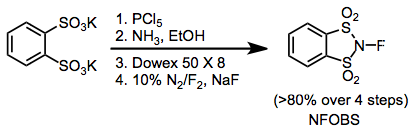
Os reagentes de fluoração NF eletrofílicos incorporam grupos de remoção de elétrons ligados ao nitrogênio para diminuir a densidade do elétron no flúor. Embora as N- fluorossulfonamidas sejam reagentes de fluoração razoavelmente fracos, as N- fluorosulfon imidas , como a N- fluorobenzenossulfonimida (NFSI), são muito eficazes e de uso comum. A N -fluoro-o-benzenodisulfonimida (NFOBS) é sintetizada a partir do ácido dissulfônico.
O uso de sais de nitrogênio catiônico aumenta as taxas e rendimentos de fluoração eletrofílica, porque o nitrogênio catiônico remove a densidade de elétrons do flúor. Os íons N-fluoropiridínio e íons imínio também podem ser usados como reagentes de fluoração eletrofílicos. Os contra-ânions desses sais, embora não estejam diretamente envolvidos na transferência de flúor para o substrato, influenciam a reatividade de maneiras sutis e podem ser ajustados usando uma variedade de métodos.
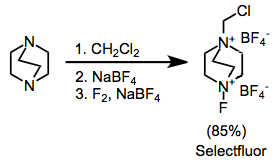
Os sais de amônio mais sinteticamente úteis são os íons DABCO bis (amônio) substituídos, incluindo Selectfluor . Estes podem ser facilmente sintetizados por alquilação seguida de fluoração. A versão difluoro, que à primeira vista pode parecer mais útil, fornece apenas um único átomo de flúor.
Reagentes de fluoração eletrofílicos mais especializados, como heterociclos neutros contendo ligações N-F, são úteis para a fluoração de uma gama limitada de substratos.
Substratos nucleofílicos
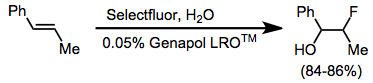
As fluorações simples de alcenos freqüentemente produzem misturas complexas de produtos. No entanto, a cofluoração na presença de um nucleófilo procede de forma limpa para dar alcoxifluoretos vicinais. Alcinos não são fluorados com reagentes NF. Um tensoativo aniônico foi usado para facilitar o contato entre o Selectfluor aquoso e o alceno.
A fluoração de compostos aromáticos ricos em elétrons dá fluoretos de arila. Os dois problemas mais comuns nesta classe de reações são baixas seletividades orto / para e desaromatização (o último é um problema particularmente significativo para fenóis).
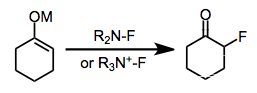
Éteres enol e glicais são nucleofílicos o suficiente para serem fluorados pelo Selectfluor. Semelhante a outros alquenos, a co-halogenação pode ser realizada por isolamento do aduto intermediário e reação com um nucleófilo ou deslocamento direto de DABCO in situ . Os enóis podem ser fluorados enantiosseletivamente (ver acima) na presença de um agente de fluoração quiral.
Os enolatos metálicos são compatíveis com muitos reagentes de fluoração, incluindo NFSI, NFOBS e sulfonamidas. No entanto, o reagente especializado 2-fluoro-3,3-dimetil-2,3-di-hidrobenzo [ d ] isotiazol 1,1-dióxido oferece consistentemente melhores rendimentos de compostos carbonilados monofluorados em reações com enolatos de lítio. Outros enolatos metálicos produziram grandes quantidades de produtos difluorados.
Comparação com outros métodos
Embora o uso de flúor molecular como fonte eletrofílica de flúor seja freqüentemente o método mais barato e direto, F 2 freqüentemente forma radicais e reage com ligações CH sem seletividade. Fontes de prótons ou ácidos de Lewis são necessários para suprimir a formação de radicais e, mesmo quando esses reagentes estão presentes, apenas certos substratos reagem com alta seletividade. O manuseio de F 2 gasoso requer equipamentos extremamente especializados e caros.
Os reagentes contendo ligações OF, como CF 3 OF, tendem a ser mais seletivos para monofluoração do que os reagentes NF. No entanto, as dificuldades associadas ao manuseio e seu poder oxidante extremo levaram à sua substituição por reagentes NF.
O di-, tetra- e hexafluoreto de xenônio são reagentes monofluorinantes seletivos. No entanto, sua instabilidade e alto custo os tornaram menos populares do que os agentes de fluoração nitrogenados.
Condições típicas
Embora as fluorações que empregam reagentes de NF não usem flúor molecular diretamente, elas são quase universalmente preparadas a partir de F 2 . O manuseio adequado de F 2 requer muito cuidado e aparelhos especiais. Os vasos de reação de poli (tetrafluoroetileno) ( PTFE , também conhecido como Teflon) são usados preferencialmente ao aço inoxidável ou vidro para reações envolvendo flúor molecular. As misturas de F 2 com N 2 ou He estão disponíveis comercialmente e ajudam a controlar a velocidade de entrega do flúor. As temperaturas devem ser mantidas baixas e a introdução do flúor lenta, para evitar reações de radicais livres.