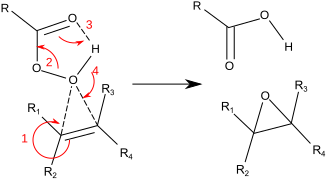Epóxido - Epoxide
Um epóxido é um éter cíclico com um anel de três átomos. Este anel se aproxima de um triângulo equilátero , o que o torna tenso e, portanto, altamente reativo, mais do que outros éteres. Eles são produzidos em grande escala para muitas aplicações. Em geral, os epóxidos de baixo peso molecular são incolores e apolares e frequentemente voláteis.
Nomenclatura
Um composto contendo o grupo funcional epóxido pode ser denominado epóxi, epóxido, oxirano e etoxilina. Os epóxidos simples são freqüentemente chamados de óxidos. Assim, o epóxido de etileno (C 2 H 4 ) é de óxido de etileno (C 2 H 4 O). Muitos compostos têm nomes triviais; por exemplo, o óxido de etileno é denominado "oxirano". Alguns nomes enfatizam a presença do grupo funcional epóxido , como no composto 1,2-epoxiheptano , que também pode ser denominado óxido de 1,2-hepteno .
Um polímero formado a partir de precursores de epóxido é denominado epóxi , mas esses materiais não contêm grupos epóxido (ou contêm apenas alguns grupos epóxido residuais que permanecem não reagidos na formação da resina).
Síntese
Os epóxidos dominantes industrialmente são o óxido de eteno e o óxido de propileno , que são produzidos respectivamente nas escalas de aproximadamente 15 e 3 milhões de toneladas / ano.
Oxidação heterogeneamente catalisada de alquenos
A epoxidação do etileno envolve sua reação com o oxigênio . De acordo com um mecanismo de reação sugerido em 1974, pelo menos uma molécula de etileno é totalmente oxidada para cada seis que são convertidas em óxido de etileno:
- 7 H 2 C = CH 2 + 6 O 2 → 6 C 2 H 4 O + 2 CO 2 + 2 H 2 O
A reação direta do oxigênio com os alcenos é útil apenas para este epóxido. Catalisadores de prata heterogêneos modificados são tipicamente empregados. Outros alquenos não reagem de maneira útil, mesmo o propileno , embora os catalisadores de Au com suporte de TS-1 possam realizar a epoxidação de propileno seletivamente.
Oxidação de olefina (alceno) usando peróxidos orgânicos e catalisadores de metal
Além do óxido de etileno, a maioria dos epóxidos são gerados tratando alcenos com reagentes contendo peróxido , que doam um único átomo de oxigênio. As considerações de segurança pesam sobre essas reações porque os peróxidos orgânicos são propensos à decomposição espontânea ou mesmo à combustão.
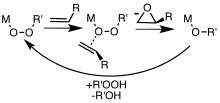
Complexos de metal são catalisadores úteis para epoxidações envolvendo peróxido de hidrogênio e hidroperóxidos de alquila. Os ácidos peroxicarboxílicos, que são mais eletrofílicos, convertem alcenos em epóxidos sem a intervenção de catalisadores metálicos. Em aplicações especializadas, outros reagentes contendo peróxidos são empregados, como o dimetildioxirano . Dependendo do mecanismo da reação e da geometria do material de partida alqueno, podem ser formados diastereômeros de epóxido cis e / ou trans . Além disso, se houver outros estereocentros presentes no material de partida, eles podem influenciar a estereoquímica da epoxidação. As epoxidações catalisadas por metal foram exploradas pela primeira vez usando hidroperóxido de terc-butila (TBHP). A associação de TBHP com o metal (M) gera o complexo peróxi de metal ativo contendo o grupo MOOR, que então transfere um centro O para o alceno.
Os peróxidos orgânicos são usados para a produção de óxido de propileno a partir do propileno. Os catalisadores também são necessários. Tanto o hidroperóxido de t-butila quanto o hidroperóxido de etilbenzeno podem ser usados como fontes de oxigênio.
Peroxidação de olefinas usando ácidos peroxicarboxílicos
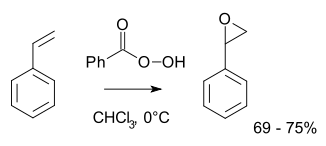
Mais tipicamente para operações de laboratório, a reação de Prilezhaev é empregada. Esta abordagem envolve a oxidação do alceno com um peroxiácido como o m-CPBA . Ilustrativo é a epoxidação de estireno com ácido perbenzoico em óxido de estireno :
A reação ocorre por meio do que é comumente conhecido como "Mecanismo de borboleta". O peróxido é visto como um eletrófilo e o alceno um nucleófilo . A reação é considerada combinada (os números no mecanismo abaixo são para simplificação). O mecanismo borboleta permite o posicionamento ideal do orbital da estrela sigma OO para que os elétrons do CC Pi ataquem. Como duas ligações são quebradas e formadas para o oxigênio do epóxido, este é formalmente um exemplo de um estado de transição coarctado .
Os hidroperóxidos também são empregados em epoxidações enantiosseletivas catalíticas , como a epoxidação de Sharpless e a epoxidação de Jacobsen . Junto com a epoxidação Shi , essas reações são úteis para a síntese enantiosseletiva de epóxidos quirais. Os reagentes de oxaziridina também podem ser usados para gerar epóxidos a partir de alcenos.
Epoxidações assimétricas catalisadas homogeneamente
Os óxidos de areno são intermediários na oxidação de arenos pelo citocromo P450 . Para arenos pró-quirais ( naftaleno , tolueno , benzoatos , benzopireno ), os epóxidos são freqüentemente obtidos em alta enantiosseletividade.
Os epóxidos quirais podem frequentemente ser derivados enantiosseletivamente de alcenos pró-quirais. Muitos complexos metálicos fornecem catalisadores ativos, mas os mais importantes envolvem titânio, vanádio e molibdênio.
A reação de epoxidação de Sharpless é uma das principais reações químicas enantiosseletivas . É usado para preparar 2,3-epoxialcoois a partir de álcoois alílicos primários e secundários .

Substituição intramolecular S N 2
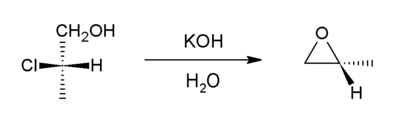
Este método envolve desidrohalogenação . É uma variante da síntese do éter Williamson . Nesse caso, um íon alcóxido desloca o cloreto intramolecularmente. Os compostos precursores são chamados de haloidrinas e podem ser gerados por meio da haloidratação de um alceno. Começando com o propileno clorohidrina , a maior parte do suprimento mundial de óxido de propileno surge por essa rota.
Uma reação de formação de epóxido intramolecular é uma das etapas principais na reação de Darzens .
Na reação de Johnson-Corey-Chaykovsky, os epóxidos são gerados a partir de grupos carbonila e iletos de sulfônio . Nesta reação, um sulfônio é o grupo de saída em vez do cloreto.
Epoxidação nucleofílica
As olefinas deficientes em elétrons, como enonas e derivados acrílicos, podem ser epoxidadas usando compostos de oxigênio nucleofílicos, como peróxidos. A reação é um mecanismo de duas etapas. Primeiro, o oxigênio realiza uma adição de conjugado nucleofílico para dar um carbânion estabilizado. Este carbanião então ataca o mesmo átomo de oxigênio, deslocando um grupo abandonante dele, para fechar o anel epóxido.
Biossíntese
Os epóxidos são incomuns na natureza. Eles surgem geralmente via oxigenação de alcenos pela ação do citocromo P450 . (mas veja também os ácidos Epoxyeicosatrienóicos de vida curta que agem como moléculas de sinalização. e Ácidos Epoxidocosapentaenóicos semelhantes , e Ácidos Epoxieicosatetraenóicos .)
Reações
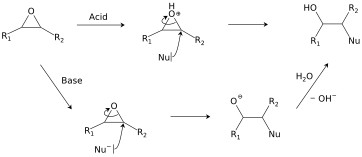
As reações de abertura do anel dominam a reatividade dos epóxidos.
Hidrólise e adição de nucleófilos
Álcoois, água, aminas, tióis e muitos outros reagentes são adicionados aos epóxidos. Essa reação é a base de duas aplicações comerciais, a formação de colas epóxi e a produção de glicóis. Sob condições ácidas, a adição nucleofílica é afetada por efeitos estéricos, como normalmente visto para reações S N 2, bem como a estabilidade do carbocátion emergente (como normalmente visto para reações S N 1). A hidrólise de um epóxido na presença de um catalisador ácido gera o glicol .
Polimerização e oligomerização
A polimerização de epóxidos dá poliéteres . Por exemplo, o óxido de etileno polimeriza para dar polietilenoglicol , também conhecido como óxido de polietileno. A reação de um álcool ou fenol com óxido de etileno, etoxilação , é amplamente utilizada para produzir surfactantes:
- ROH + n C 2 H 4 O → R (OC 2 H 4 ) n OH
Com os anidridos, os epóxidos dão poliésteres.
Desoxigenação
Os epóxidos podem ser desoxigenados usando reagentes oxofílicos . Esta reação pode ocorrer com perda ou retenção da configuração. A combinação de hexacloreto de tungstênio e n- butil-lítio dá o alceno .
Outras reações
- A redução de um epóxido com hidreto de alumínio e lítio ou hidreto de alumínio produz o álcool correspondente . Este processo de redução resulta da adição nucleofílica de hidreto (H - ).
- A clivagem redutiva de epóxidos dá β-litioalcóxidos.
- A redução com hexacloreto de tungstênio e n- butil-lítio gera o alceno
- Os epóxidos sofrem reações de expansão do anel, ilustradas pela inserção de dióxido de carbono para dar carbonatos cíclicos .
- Quando tratados com tioureia, os epóxidos se convertem em episulfeto, que são chamados de tiiranos .
Usos
O éter diglicidílico de bisfenol A é um componente do "epóxi" doméstico comum.
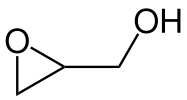
A estrutura química do epóxido glicidol , um intermediário químico comum.
As epotilonas são epóxidos de ocorrência natural.
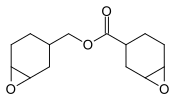
3,4-Epoxiciclohexilmetil-3 ', 4'-epoxiciclohexano carboxilato , precursor de revestimentos.
Epoxidado linolein , um importante componente de óleo de soja epoxidado (ESBO), um importante comercialmente plastificante .
O óxido de benzeno existe em equilíbrio com o isômero de oxepina.
O óxido de etileno é amplamente utilizado para gerar detergentes e surfactantes por etoxilação . Sua hidrólise fornece etilenoglicol . Também é usado para esterilizar instrumentos e materiais médicos.
A reação de epóxidos com aminas é a base para a formação de colas epóxi e materiais estruturais. Um endurecedor de amina típico é a trietilenotetramina (TETA).
Segurança
Os epóxidos são agentes alquilantes , tornando muitos deles altamente tóxicos.