Atresia esofágica - Esophageal atresia
| Atresia esofágica | |
|---|---|
| Outros nomes | Atresia esofágica |
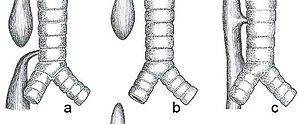 | |
| Tipos anatômicos comuns de atresia esofágica a) Atresia esofágica com fístula traqueoesofágica distal (86%), Gross C. b) Atresia esofágica isolada sem fístula traqueoesofágica (7%), Gross A. c) Fístula traqueoesofágica tipo H (4%), Gross E. | |
| Especialidade | Pediatria |
A atresia esofágica é uma condição médica congênita ( defeito de nascença ) que afeta o trato alimentar . Ele faz com que o esôfago termine em uma bolsa cega, em vez de se conectar normalmente ao estômago . Compreende uma variedade de defeitos anatômicos congênitos que são causados por um desenvolvimento embriológico anormal do esôfago. É caracterizada anatomicamente por uma obstrução congênita do esôfago com interrupção da continuidade da parede esofágica.
sinais e sintomas
Esse defeito de nascença surge na quarta semana fetal, quando a traqueia e o esôfago devem começar a se separar.
Pode estar associada a distúrbios do septo traqueoesofágico .
Complicações
Qualquer tentativa de alimentação pode causar pneumonia por aspiração, pois o leite se acumula na bolsa cega e transborda para a traqueia e os pulmões. Além disso, uma fístula entre a parte inferior do esôfago e a traqueia pode permitir que o ácido do estômago flua para os pulmões e cause danos. Por causa desses perigos, a condição deve ser tratada o mais rápido possível após o nascimento.
Defeitos de nascença associados
Outros defeitos congênitos podem coexistir, especialmente no coração , mas às vezes também no ânus, coluna vertebral ou rins. Isso é conhecido como associação VACTERL devido ao envolvimento da coluna vertebral, anorretal, cardíaca, traqueal, esofágica, renal e membros. Está associada a polidrâmnio no terceiro trimestre.
Diagnóstico
Essa condição pode ser visível, após cerca de 26 semanas, em um ultrassom . Na USG pré-natal, o achado de um estômago ausente ou pequeno no quadro de polidrâmnio foi considerado um sintoma potencial de atresia esofágica. No entanto, esses achados têm baixo valor preditivo positivo. O sinal da bolsa cervical superior é outro sinal que ajuda no diagnóstico pré-natal de atresia esofágica e pode ser detectado logo após o nascimento, pois o bebê afetado não conseguirá engolir sua própria saliva .
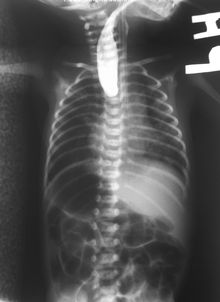
Na radiografia simples, um tubo de alimentação não será visto passando pelo esôfago e permanecerá enrolado na bolsa esofágica superior.
Classificação
Essa condição assume várias formas diferentes, geralmente envolvendo uma ou mais fístulas que conectam a traquéia ao esôfago ( fístula traqueoesofágica ).
| Bruto | Vogt | Ladd | Nome (s) | Descrição | Frequência |
|---|---|---|---|---|---|
| - | Tipo 1 | - | Agenesia esofágica | Ausência completa muito rara do esôfago, não incluída na classificação de Gross ou Ladd | N / D |
| Tipo A | Tipo 2 | eu | Atresia esofágica "Long Gap", "Pura" ou "Isolada" | Caracteriza-se pela presença de um “gap” entre as duas bolsas cegas esofágicas sem fístula. | 7% |
| Tipo B | Tipo 3A | II | Atresia esofágica com FTE proximal (fístula traqueoesofágica) | A bolsa esofágica superior se conecta anormalmente à traqueia. A bolsa esofágica inferior termina às cegas. | 2-3% |
| Tipo C | Tipo 3B | III, IV | Atresia esofágica com TEF distal (fístula traqueoesofágica) | A bolsa esofágica inferior se conecta anormalmente à traqueia. A bolsa esofágica superior termina às cegas. | 86% |
| Tipo D | Tipo 3C | V | Atresia esofágica com TEFs proximais e distais (duas fístulas traqueoesofágicas) | Tanto a bolsa esofágica superior quanto a inferior fazem uma conexão anormal com a traqueia em dois locais separados e isolados. | <1% |
| Tipo E | Tipo 4 | - | TEF (fístula traqueoesofágica) SOMENTE sem atresia esofágica, tipo H | Esôfago totalmente intacto e capaz de suas funções normais, entretanto, há uma conexão anormal entre o esôfago e a traquéia. Não incluído na classificação por Ladd | 4% |
Tratamento
Opções de tratamento
Os tratamentos para a doença variam de acordo com sua gravidade. O tratamento mais imediato e eficaz na maioria dos casos é um reparo cirúrgico para fechar a (s) fístula (s) e reconectar as duas extremidades do esôfago uma à outra. Embora isso geralmente seja feito por meio de uma incisão entre as costelas do lado direito do bebê, uma técnica com três pequenas incisões (toracoscopia) está sendo usada em alguns centros.
Em uma minoria de casos, o intervalo entre os segmentos superior e inferior do esôfago pode ser muito longo para ser preenchido. Nessas situações, as abordagens cirúrgicas tradicionais incluem gastrostomia seguida de pull-up gástrico, transposição do cólon e transposição do jejuno. A flexão gástrica tem sido a abordagem preferida em muitos centros especializados, incluindo Great Ormond Street (Londres) e Mott Children's Hospital (Ann Arbor). A gastrostomia, ou tubo G, permite a alimentação do tubo no estômago através da parede abdominal. Freqüentemente, também é feita uma esofagostomia cervical, para permitir que a saliva que é engolida escorra por um orifício no pescoço. Meses ou anos depois, o esôfago pode ser reparado, às vezes usando um segmento do intestino levado para o tórax, interpondo-se entre os segmentos superior e inferior do esôfago.
Em alguns desses chamados casos de gap longo, entretanto, um tratamento cirúrgico avançado desenvolvido por John Foker, MD, pode ser utilizado para alongar e, em seguida, unir os segmentos curtos do esôfago. Usando a técnica de Foker, os cirurgiões colocam suturas de tração nas minúsculas extremidades do esôfago e aumentam a tensão nessas suturas diariamente até que as extremidades estejam próximas o suficiente para serem costuradas. O resultado é um esôfago funcionando normalmente, virtualmente indistinguível de um bem formado congênito. Infelizmente, os resultados têm sido um tanto difíceis de replicar por outros cirurgiões e a necessidade de múltiplas operações diminuiu o entusiasmo por essa abordagem. O tratamento ideal em casos de atresia esofágica de longo gap permanece controverso.
O método de compressão magnética é outro método para reparar a atresia esofágica de longo gap. Este método não requer a substituição da seção ausente por enxertos do intestino ou de outras partes do corpo. O uso de força eletromagnética para atrair as extremidades superior e inferior do esôfago juntas foi tentado pela primeira vez na década de 1970, usando pelotas de aço atraídas entre si pela aplicação de eletroímãs externos no paciente. Na década de 2000, um novo refinamento foi desenvolvido pelo grupo de Mario Zaritzky e outros. O método mais recente usa ímãs permanentes e um balão.
- Os imãs são inseridos na bolsa superior pela boca ou nariz do bebê, e na inferior pelo orifício do tubo de gastrotomia (que teria que ser feito de qualquer maneira para alimentar o bebê, não necessitando, portanto, de nenhuma cirurgia adicional).
- A distância entre os ímãs é controlada por um balão na bolsa superior, entre a extremidade da bolsa e o ímã. Isso também controla a força entre os ímãs, portanto, não é forte o suficiente para causar danos.
- Depois que as extremidades do esôfago se esticam o suficiente para se tocar, o ímã superior é substituído por um sem balão e a atração magnética mais forte faz com que as extremidades se fundam ( anastomose ).
Em abril de 2015, Annalise Dapo se tornou a primeira paciente nos Estados Unidos a ter sua atresia esofágica corrigida com ímãs.
Complicações de tratamento
As complicações pós-operatórias podem incluir um vazamento no local de fechamento do esôfago. Às vezes, uma estenose, ou ponto tenso, se desenvolve no esôfago, dificultando a deglutição. A estenose esofágica geralmente pode ser dilatada com o uso de instrumentos médicos. Mais tarde na vida, a maioria das crianças com esse distúrbio terá alguns problemas para engolir, azia ou ambos. A dismotilidade esofágica ocorre em 75-100% dos pacientes. Após o reparo esofágico ( anastomose ), a flacidez relativa da antiga bolsa proximal (bolsa cega, acima) junto com a dismotilidade esofágica pode causar acúmulo de líquido durante a alimentação. Devido à proximidade, o balonamento da bolsa pode causar oclusão traqueal. Segue-se hipóxia severa ("crises de morte") e a intervenção médica pode freqüentemente ser necessária.
Traqueomalácia um amolecimento da traqueia, geralmente acima da carina ( carina da traqueia ), mas às vezes extensa também na árvore brônquica inferior - é outra possível complicação séria. Uma variedade de tratamentos para traqueomalácia associada à atresia esofágica estão disponíveis. Se não for grave, a condição pode ser tratada com expectativa, uma vez que a traqueia geralmente enrijece à medida que o bebê amadurece no primeiro ano de vida. Quando apenas a traqueia acima da carina está comprometida, uma das intervenções "mais simples" é a aortopexia em que a alça aórtica é fixada na parte posterior do esterno, aliviando mecanicamente a pressão da traqueia amolecida. Uma intervenção ainda mais simples é o implante de stent. No entanto, a proliferação de células epiteliais e a possível incorporação do stent na traqueia podem tornar a remoção subsequente perigosa.
A incidência de asma, bronquite, hiperresponsividade brônquica e infecções recorrentes em sobreviventes de atresia esofágica em adolescentes e adultos excede em muito a de seus pares saudáveis. Durante a primeira década de correção cirúrgica da IA, cerca de 20% dos pacientes sucumbiram à pneumonia . A partir daí, a pneumonia permaneceu como uma das principais complicações pulmonares e motivo de reinternações após o reparo da IA. Os fatores de risco de pneumonia nos primeiros cinco anos de vida incluem outras infecções respiratórias agudas e alto número de dilatações esofágicas.
Epidemiologia
Ocorre em aproximadamente 1 em 3.000 nascidos vivos .
A atresia congênita do esôfago (AE) representa uma falha do esôfago em se desenvolver como uma passagem contínua. Em vez disso, termina como uma bolsa cega. A fístula traqueoesofágica ( FTE ) representa uma abertura anormal entre a traqueia e o esôfago. EA e TEF podem ocorrer separadamente ou juntos. EA e TEF são diagnosticados na UTI no nascimento e tratados imediatamente.
Suspeita-se da presença de IA em lactentes com salivação excessiva (salivação) e em recém-nascidos com salivação frequentemente acompanhada de engasgo, tosse e espirros. Quando alimentados, esses bebês engolem normalmente, mas começam a tossir e lutar enquanto o líquido retorna pelo nariz e pela boca. O lactente pode ficar cianótico (ficar azulado devido à falta de oxigênio) e pode parar de respirar quando o excesso de fluido da bolsa cega é aspirado (sugado) para a traqueia. A cianose é decorrente do laringoespasmo (mecanismo de proteção que o organismo possui para evitar a aspiração para a traquéia). Com o tempo, desenvolverá dificuldade respiratória.
Se algum dos sinais / sintomas acima forem observados, um cateter é introduzido suavemente no esôfago para verificar a existência de resistência. Se houver resistência, outros estudos serão feitos para confirmar o diagnóstico. Um cateter pode ser inserido e aparecerá branco em um filme de raio-X regular para demonstrar o final da bolsa cega. Às vezes, uma pequena quantidade de bário (líquido semelhante a giz) é colocada pela boca para diagnosticar os problemas.
O tratamento de EA e TEF é uma cirurgia para reparar o defeito. Se houver suspeita de EA ou TEF, todas as alimentações orais são interrompidas e os fluidos intravenosos são iniciados. O bebê será posicionado para ajudar a drenar as secreções e diminuir a probabilidade de aspiração. Bebês com EA às vezes podem ter outros problemas. Serão feitos estudos para examinar o coração, a coluna e os rins. A cirurgia para reparar a IA é essencial, pois o bebê não será capaz de se alimentar e tem grande probabilidade de desenvolver pneumonia. Quando o bebê está em condições de cirurgia, uma incisão é feita na lateral do tórax. O esôfago geralmente pode ser costurado. Após a cirurgia, o bebê pode ficar hospitalizado por um período de tempo variável. O cuidado de cada bebê é individualizado. É muito comum em um recém-nascido com ânus imperfurado .
Referências
Leitura adicional
- Harmon CM, Coran AG (1998). "Anomalias Congênitas do Esôfago". Cirurgia Pediátrica (5ª ed.). St Louis, KY: Elsevier Science Health Science Division. ISBN 0-8151-6518-8 .
links externos
| Classificação | |
|---|---|
| Fontes externas |