Ester - Ester
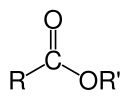
Um éster é um composto químico derivado de um ácido (orgânico ou inorgânico) em que pelo menos um grupo -OH hidroxila é substituído por um grupo -O- alquil ( alcoxi ), como na reação de substituição de um ácido carboxílico e um álcool . Os glicerídeos são ésteres de ácido graxo de glicerol ; eles são importantes em biologia, sendo uma das principais classes de lipídios e compreendendo a maior parte das gorduras animais e óleos vegetais.
Os ésteres geralmente têm um cheiro agradável; aqueles de baixo peso molecular são comumente usados como fragrâncias e são encontrados em óleos essenciais e feromônios . Eles atuam como solventes de alto grau para uma ampla gama de plásticos, plastificantes , resinas e lacas e são uma das maiores classes de lubrificantes sintéticos no mercado comercial. Os poliésteres são plásticos importantes , com monômeros ligados por porções de éster . Os fosfoésteres formam a espinha dorsal das moléculas de DNA . Os ésteres de nitrato , como a nitroglicerina , são conhecidos por suas propriedades explosivas.
Nomenclatura
Etimologia
A palavra éster foi cunhada em 1848 por um químico alemão Leopold Gmelin , provavelmente como uma contração do alemão Essigäther , " éter acético ".
Nomenclatura IUPAC
Os nomes dos ésteres são derivados do álcool original e do ácido original, onde o último pode ser orgânico ou inorgânico. Os ésteres derivados dos ácidos carboxílicos mais simples são comumente nomeados de acordo com os chamados " nomes triviais " mais tradicionais, por exemplo, como formato, acetato, propionato e butirato, em oposição à nomenclatura IUPAC metanoato, etanoato, propanoato e butanoato. Os ésteres derivados de ácidos carboxílicos mais complexos são, por outro lado, nomeados com mais frequência pelo nome sistemático IUPAC, com base no nome do ácido seguido do sufixo -oato . Por exemplo, o éster hexil octanoato, também conhecido pelo nome trivial de hexil caprilato , tem a fórmula CH 3 (CH 2 ) 6 CO 2 (CH 2 ) 5 CH 3 .
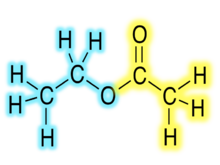
As fórmulas químicas dos ésteres orgânicos geralmente tomam a forma RCO 2 R ′, onde R e R ′ são as partes do hidrocarboneto do ácido carboxílico e do álcool, respectivamente. Por exemplo, acetato de butila (sistematicamente etanoato de butila), derivado de butanol e ácido acético (sistematicamente ácido etanóico) seria escrito CH 3 CO 2 C 4 H 9 . Apresentações alternativas são comuns, incluindo BuOAc e CH 3 COOC 4 H 9 .
Os ésteres cíclicos são chamados de lactonas , independentemente de serem derivados de um ácido orgânico ou inorgânico. Um exemplo de uma lactona orgânica é a γ-valerolactona .
Ortoesters
Uma classe incomum de ésteres orgânicos são os ortoésteres , que têm a fórmula RC (OR ′) 3 . O trietilortoformato (HC (OC 2 H 5 ) 3 ) é derivado, em termos de seu nome (mas não de sua síntese), do ácido ortofórmico (HC (OH) 3 ) e do etanol .
Ésteres inorgânicos
Os ésteres também podem ser derivados de ácidos inorgânicos.
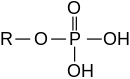
- O ácido fosfórico forma ésteres de fosfato , por exemplo, trifenilfosfato
- ácido sulfúrico forma ésteres de sulfato , por exemplo, dimetilsulfato
- o ácido nítrico forma ésteres de nitrato , por exemplo, nitrato de metila
- o ácido bórico forma boratos , por exemplo, trimetilborato .
- o ácido carbônico forma ésteres de carbonato , por exemplo, carbonato de etileno
Os ácidos inorgânicos que existem como tautômeros formam diversos ésteres
- o ácido fosforoso forma dois tipos de ésteres de fosfito , por exemplo, trietilfosfito (P (OEt) 3 ) e dietilfosfito (HP (O) (OEt) 2 ).
Os ácidos inorgânicos que são instáveis ou evasivos formam ésteres estáveis.
- ácido crômico , que nunca foi detectado, forma cromato de di-terc-butil
- ácido sulfuroso , que é raro, forma dimetilsulfito
Em princípio, todos os alcóxidos metálicos e metalóides , dos quais muitas centenas são conhecidos, poderiam ser classificados como ésteres dos ácidos hipotéticos.
Estrutura e ligação
Os ésteres contêm um centro carbonila , que dá origem aos ângulos 120 ° C – C – O e O – C – O. Ao contrário das amidas , os ésteres são grupos funcionais estruturalmente flexíveis porque a rotação em torno das ligações C – O – C tem uma barreira baixa. Sua flexibilidade e baixa polaridade se manifestam em suas propriedades físicas; eles tendem a ser menos rígidos (ponto de fusão mais baixo) e mais voláteis (ponto de ebulição mais baixo) do que as amidas correspondentes . O p K a dos alfa-hidrogênios em ésteres é cerca de 25.
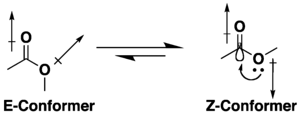
Muitos ésteres têm potencial para isomerismo conformacional , mas eles tendem a adotar uma conformação s- cis (ou Z) em vez da alternativa s- trans (ou E), devido a uma combinação de efeitos de hiperconjugação e minimização de dipolo . A preferência pela conformação Z é influenciada pela natureza dos substituintes e do solvente, se presentes. As lactonas com anéis pequenos estão restritas à conformação s- trans (isto é, E) devido à sua estrutura cíclica.
Propriedades físicas e caracterização
Os ésteres são mais polares do que os éteres, mas menos polares do que os álcoois. Eles participam de ligações de hidrogênio como aceitadores de ligações de hidrogênio, mas não podem atuar como doadores de ligações de hidrogênio, ao contrário de seus álcoois originais. Essa capacidade de participar de ligações de hidrogênio confere alguma solubilidade em água. Por causa de sua falta de capacidade de doação de ligações de hidrogênio, os ésteres não se autoassociam. Consequentemente, os ésteres são mais voláteis do que os ácidos carboxílicos de peso molecular semelhante.
Caracterização e análise
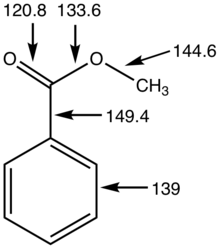
Os ésteres são geralmente identificados por cromatografia gasosa, aproveitando sua volatilidade. Os espectros de IR para os ésteres apresentam uma intensa banda bem definida no intervalo de 1730-1750 cm -1 atribuídos a v C = O . Este pico muda dependendo dos grupos funcionais ligados ao carbonil. Por exemplo, um anel de benzeno ou ligação dupla em conjugação com a carbonila fará com que o número de onda diminua cerca de 30 cm -1 .
Aplicações e ocorrência
Os ésteres são muito difundidos na natureza e amplamente utilizados na indústria. Na natureza, as gorduras são, em geral, triésteres derivados do glicerol e dos ácidos graxos . Os ésteres são responsáveis pelo aroma de muitas frutas, incluindo maçãs , durians , pêras , bananas , abacaxis e morangos . Vários bilhões de quilogramas de poliésteres são produzidos industrialmente anualmente, sendo produtos importantes o tereftalato de polietileno , ésteres de acrilato e acetato de celulose .
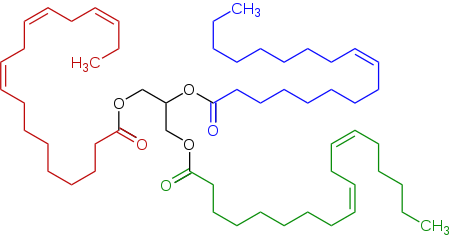 Triglicerídeo representativo encontrado em um óleo de linhaça, um triéster ( triglicerídeo ) derivado de ácido linoléico , ácido alfa-linolênico e ácido oleico .
Triglicerídeo representativo encontrado em um óleo de linhaça, um triéster ( triglicerídeo ) derivado de ácido linoléico , ácido alfa-linolênico e ácido oleico .
Preparação
Esterificação é o nome geral para uma reação química na qual dois reagentes (normalmente um álcool e um ácido) formam um éster como produto da reação . Os ésteres são comuns na química orgânica e em materiais biológicos e costumam ter um odor agradável e característico de frutas. Isso leva ao seu uso extensivo na indústria de fragrâncias e sabores . As ligações de ésteres também são encontradas em muitos polímeros .
Esterificação de ácidos carboxílicos com álcoois
A síntese clássica é a esterificação de Fischer , que envolve o tratamento de um ácido carboxílico com um álcool na presença de um agente desidratante :
- RCO 2 H + R′OH ⇌ RCO 2 R ′ + H 2 O
A constante de equilíbrio para tais reações é de cerca de 5 para ésteres típicos, por exemplo, acetato de etila. A reação é lenta na ausência de um catalisador. O ácido sulfúrico é um catalisador típico para essa reação. Muitos outros ácidos também são usados, como os ácidos sulfônicos poliméricos . Uma vez que a esterificação é altamente reversível, o rendimento do éster pode ser melhorado usando o princípio de Le Chatelier :
- Usar o álcool em grande excesso (ou seja, como solvente).
- Usando um agente desidratante: o ácido sulfúrico não apenas catalisa a reação, mas sequestra a água (um produto da reação). Outros agentes de secagem, como peneiras moleculares, também são eficazes.
- Remoção de água por meios físicos, como destilação como um azeótropo de baixo ponto de ebulição com tolueno , em conjunto com um aparelho Dean-Stark .
São conhecidos os reagentes que provocam a desidratação de misturas de álcoois e ácidos carboxílicos. Um exemplo é a esterificação de Steglich , que é um método de formação de ésteres em condições moderadas. O método é popular na síntese de peptídeos , onde os substratos são sensíveis a condições adversas, como altas temperaturas. DCC ( diciclohexilcarbodiimida ) é usado para ativar o ácido carboxílico para posterior reação. 4-Dimetilaminopiridina (DMAP) é usado como um catalisador de transferência de acila .
Outro método para a desidratação de misturas de álcoois e ácidos carboxílicos é a reação de Mitsunobu :
- RCO 2 H + R′OH + P (C 6 H 5 ) 3 + R 2 N 2 → RCO 2 R ′ + OP (C 6 H 5 ) 3 + R 2 N 2 H 2
Os ácidos carboxílicos podem ser esterificados usando diazometano :
- RCO 2 H + CH 2 N 2 → RCO 2 CH 3 + N 2
Usando este diazometano, misturas de ácidos carboxílicos podem ser convertidas em seus ésteres metílicos em rendimentos quase quantitativos, por exemplo, para análise por cromatografia gasosa . O método é útil em operações sintéticas orgânicas especializadas, mas é considerado muito perigoso e caro para aplicações em grande escala.
Esterificação de ácidos carboxílicos com epóxidos
Os ácidos carboxílicos são esterificados por tratamento com epóxidos, dando β-hidroxiésteres:
- RCO 2 H + RCHCH 2 O → RCO 2 CH 2 CH (OH) R
Esta reação é empregada na produção de resinas de resina de éster vinílico a partir de ácido acrílico .
Alcoólise de cloretos de acila e anidridos de ácido
Os álcoois reagem com cloretos de acila e anidridos de ácido para dar ésteres:
- RCOCl + R′OH → RCO 2 R ′ + HCl
- (RCO) 2 O + R′OH → RCO 2 R ′ + RCO 2 H
As reações são irreversíveis, simplificando o processamento . Uma vez que os cloretos de acila e os anidridos de ácido também reagem com a água, as condições anidras são preferidas. As acilações análogas de aminas para dar amidas são menos sensíveis porque aminas são nucleófilos mais fortes e reagem mais rapidamente do que a água. Este método é empregado apenas para procedimentos em escala de laboratório, pois é caro.
Alquilação de sais de carboxilato
Embora não sejam amplamente utilizados para esterificações, os sais de ânions carboxilato podem ser agentes alquilantes com halogenetos de alquila para dar ésteres. No caso de ser usado um cloreto de alquila , um sal iodeto pode catalisar a reação ( reação de Finkelstein ). O sal carboxilato é freqüentemente gerado in situ . Em casos difíceis, pode-se utilizar o carboxilato de prata, uma vez que o íon prata se coordena ao haleto auxiliando na sua saída e melhorando a velocidade da reação. Esta reação pode sofrer de problemas de disponibilidade de ânions e, portanto, pode se beneficiar da adição de catalisadores de transferência de fase ou solventes apróticos altamente polares , como DMF .
Transesterificação
A transesterificação , que envolve a transformação de um éster em outro, é amplamente praticada:
- RCO 2 R ′ + CH 3 OH → RCO 2 CH 3 + R′OH
Assim como a hidrólise, a transesterificação é catalisada por ácidos e bases. A reação é amplamente utilizada para degradar triglicerídeos , por exemplo, na produção de ésteres de ácidos graxos e álcoois. O poli (tereftalato de etileno) é produzido pela transesterificação de tereftalato de dimetila e etilenoglicol:
- (C 6 H 4 ) (CO 2 CH 3 ) 2 + 2 C 2 H 4 (OH) 2 → 1 ⁄ n {(C 6 H 4 ) (CO 2 ) 2 (C 2 H 4 )} n + 2 CH 3 OH
Um subconjunto da transesterificação é a alcoólise do diceteno . Esta reação fornece 2-cetoésteres.
- (CH 2 CO) 2 + ROH → CH 3 C (O) CH 2 CO 2 R
Carbonilação
Os alcenos sofrem " hidroesterificação " na presença de catalisadores de carbonila de metal . Os ésteres de ácido propanóico são produzidos comercialmente por este método:
- C 2 H 4 + ROH + CO → C 2 H 5 CO 2 R
Uma preparação de propionato de metila é um exemplo ilustrativo.
- C 2 H 4 + CO + MeOH → MeO 2 CCH 2 CH 3
A carbonilação do metanol produz formato de metila , que é a principal fonte comercial de ácido fórmico . A reação é catalisada por metóxido de sódio :
- CH 3 OH + CO → CH 3 O 2 CH
Adição de ácidos carboxílicos a alcenos e alcinos
Na presença de catalisadores à base de paládio , etileno, ácido acético e oxigênio reagem para dar acetato de vinila :
- C 2 H 4 + CH 3 CO 2 H + 1 ⁄ 2 O 2 → C 2 H 3 O 2 CCH 3 + H 2 O
Rotas diretas para este mesmo éster não são possíveis porque o álcool vinílico é instável.
Os ácidos carboxílicos também se agregam aos alcinos para dar os mesmos produtos.
O ácido silicotúngstico é usado para fabricar acetato de etila pela alquilação do ácido acético por etileno:
- C 2 H 4 + CH 3 CO 2 H → CH 3 CO 2 C 2 H 5
De aldeídos
A reação de Tishchenko envolve a desproporção de um aldeído na presença de uma base anidra para dar um éster. Os catalisadores são alcóxidos de alumínio ou alcóxidos de sódio. O benzaldeído reage com o benzilóxido de sódio (gerado a partir do sódio e do álcool benzílico ) para gerar o benzoato de benzila . O método é usado na produção de acetato de etila a partir do acetaldeído .
Outros métodos
- Reorganização Favorskii de α-halocetonas na presença de base
- Oxidação de Baeyer-Villiger de cetonas com peróxidos
- Reação de pinner de nitrilas com álcool
- Abstração nucleofílica de um complexo metal-acila
- Hidrólise de ortoésteres em ácido aquoso
- Celulólise via esterificação
- Ozonólise de alcenos usando um processamento na presença de ácido clorídrico e vários álcoois .
- Oxidação anódica de metil cetonas levando a ésteres metílicos.
- A interesterificação troca os grupos de ácidos graxos de diferentes ésteres.
Reações
Os ésteres reagem com os nucleófilos no carbono carbonílico. O carbonil é fracamente eletrofílico, mas é atacado por nucleófilos fortes (aminas, alcóxidos, fontes de hidretos, compostos de organolítio, etc.). As ligações C – H adjacentes à carbonila são fracamente ácidas, mas sofrem desprotonação com bases fortes. Este processo é o que geralmente inicia as reações de condensação. O oxigênio da carbonila nos ésteres é fracamente básico, menos que o oxigênio da carbonila nas amidas devido à doação por ressonância de um par de elétrons do nitrogênio nas amidas, mas forma adutos .
Hidrólise e saponificação
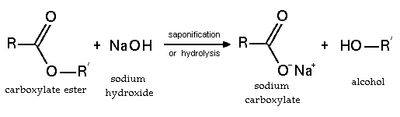
A esterificação é uma reação reversível. Os ésteres sofrem hidrólise em condições ácidas e básicas. Em condições ácidas, a reação é a reação reversa da esterificação de Fischer . Sob condições básicas, o hidróxido atua como um nucleófilo, enquanto um alcóxido é o grupo de saída. Essa reação, a saponificação , é a base da fabricação do sabão.
O grupo alcóxido também pode ser deslocado por nucleófilos mais fortes, como amônia ou aminas primárias ou secundárias para dar amidas : (reação de amonólise)
- RCO 2 R ′ + NH 2 R ″ → RCONHR ″ + R′OH
Essa reação geralmente não é reversível. Hidrazinas e hidroxilamina podem ser usadas no lugar das aminas. Os ésteres podem ser convertidos em isocianatos por meio de ácidos hidroxâmicos intermediários no rearranjo de Lossen .
Fontes de nucleófilos de carbono, por exemplo, reagentes de Grignard e compostos de organolítio, adicionam-se prontamente ao carbonil.
Redução
Comparados às cetonas e aldeídos, os ésteres são relativamente resistentes à redução . A introdução da hidrogenação catalítica no início do século 20 foi um grande avanço; os ésteres de ácidos graxos são hidrogenados em álcoois graxos .
- RCO 2 R ′ + 2 H 2 → RCH 2 OH + R′OH
Um catalisador típico é a cromita de cobre . Antes do desenvolvimento da hidrogenação catalítica , os ésteres foram reduzidos em grande escala usando a redução de Bouveault-Blanc . Este método, em grande parte obsoleto, usa sódio na presença de fontes de prótons.
Especialmente para sínteses químicas finas, o hidreto de alumínio e lítio é usado para reduzir os ésteres a dois álcoois primários. O reagente relacionado boro-hidreto de sódio é lento nesta reação. O DIBAH reduz os ésteres a aldeídos.
A redução direta para dar o éter correspondente é difícil porque o hemiacetal intermediário tende a se decompor para dar um álcool e um aldeído (que é rapidamente reduzido para dar um segundo álcool). A reação pode ser realizada usando trietilsilano com uma variedade de ácidos de Lewis.
Quanto aos aldeídos , os átomos de hidrogênio no carbono adjacente ("α a") o grupo carboxila em ésteres são suficientemente ácidos para sofrer desprotonação, o que por sua vez leva a uma variedade de reações úteis. A desprotonação requer bases relativamente fortes, como alcóxidos . A desprotonação dá um enolato nucleofílico , que pode reagir posteriormente, por exemplo, a condensação de Claisen e seu equivalente intramolecular, a condensação de Dieckmann . Esta conversão é explorada na síntese do éster malônico , em que o diéster do ácido malônico reage com um eletrófilo (por exemplo, haleto de alquila ) e é subsequentemente descarboxilado. Outra variação é a alquilação Fráter – Seebach .
Outras reações
- Os ésteres fenílicos reagem às hidroxiarilcetonas no rearranjo de Fries .
- Ésteres específicos são funcionalizados com um grupo α-hidroxila no rearranjo de Chan .
- Os ésteres com átomos de hidrogênio β podem ser convertidos em alquenos na pirólise do éster .
- Uma conversão direta de ésteres em nitrilos .
Protegendo grupos
Como classe, os ésteres servem como grupos de proteção para os ácidos carboxílicos . Proteger um ácido carboxílico é útil na síntese de peptídeos, para prevenir auto-reações dos aminoácidos bifuncionais . Os ésteres metílicos e etílicos estão comumente disponíveis para muitos aminoácidos; o éster t- butílico tende a ser mais caro. No entanto, os ésteres t- butílicos são particularmente úteis porque, sob condições fortemente ácidas, os ésteres t- butílicos são eliminados para dar o ácido carboxílico e o isobutileno , simplificando o processamento.
Lista de odorantes de éster
Muitos ésteres têm odores característicos de frutas e muitos ocorrem naturalmente nos óleos essenciais das plantas. Isso também levou ao seu uso comum em aromas e fragrâncias artificiais que visam imitar esses odores.
Veja também
- Lista de ésteres
- Amida , um análogo de éster com oxigênio substituído por nitrogênio
- Éster de cianato
- Oligoester
- Poliolester
- Tioéster , um análogo de éster com oxigênio substituído por enxofre
- Transesterificação
- Éter lipídico