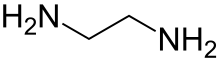
Etilenodiamina - Ethylenediamine
|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Etano-1,2-diamina |
|||
| Outros nomes
Edamina, 1,2-diaminoetano, 'en' quando um ligante
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| Abreviações | en | ||
| 605263 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100,003,154 |
||
| Número EC | |||
| 1098 | |||
| KEGG | |||
| Malha | etilenodiamina | ||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 1604 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 2 H 8 N 2 | |||
| Massa molar | 60,100 g · mol −1 | ||
| Aparência | Líquido incolor | ||
| Odor | Amoniacal | ||
| Densidade | 0,90 g / cm 3 | ||
| Ponto de fusão | 8 ° C (46 ° F; 281 K) | ||
| Ponto de ebulição | 116 ° C (241 ° F; 389 K) | ||
| miscível | |||
| log P | -2,057 | ||
| Pressão de vapor | 1,3 kPa (a 20 ° C) | ||
|
Constante da lei de Henry ( k H ) |
5,8 mol Pa −1 kg −1 | ||
|
Índice de refração ( n D )
|
1,4565 | ||
| Termoquímica | |||
|
Capacidade de calor ( C )
|
172,59 JK −1 mol −1 | ||
|
Entropia molar padrão ( S |
202,42 JK −1 mol −1 | ||
| −63,55-−62,47 kJ mol −1 | |||
| −1,8678–−1,8668 MJ mol −1 | |||
| Perigos | |||
| Pictogramas GHS |
   
|
||
| Palavra-sinal GHS | Perigo | ||
| H226 , H311 , H302 , H332 , H314 , H334 , H317 , H412 | |||
| P405 , P102 , P260 , P280 , P305 + 351 + 338 , P101 , P308 + 313 , P273 , P501 | |||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | 34 ° C (93 ° F; 307 K) | ||
| 385 ° C (725 ° F; 658 K) | |||
| Limites explosivos | 2,7-16% | ||
| Dose ou concentração letal (LD, LC): | |||
|
LD 50 ( dose mediana )
|
500 mg / kg (oral, rato) 470 mg / kg (oral, porquinho da índia) 1160 mg / kg (oral, rato) |
||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
TWA 10 ppm (25 mg / m 3 ) | ||
|
REL (recomendado)
|
TWA 10 ppm (25 mg / m 3 ) | ||
|
IDLH (perigo imediato)
|
1000 ppm | ||
| Compostos relacionados | |||
|
Alcanaminas relacionadas
|
1,2-diaminopropano , 1,3-diaminopropano | ||
|
Compostos relacionados
|
Etilamina , Etilenodinitramina | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Etilenodiamina (abreviado como en quando um ligando ) é o composto orgânico com a fórmula C 2 H 4 (NH 2 ) 2 . Este líquido incolor com um odor semelhante ao da amônia é uma amina básica . É um bloco de construção amplamente utilizado em síntese química, com aproximadamente 500.000 toneladas produzidas em 1998. A etilenodiamina reage prontamente com a umidade do ar úmido para produzir uma névoa corrosiva, tóxica e irritante, à qual mesmo exposições curtas podem causar sérios danos à saúde (ver segurança). A etilenodiamina é o primeiro membro das chamadas aminas de polietileno .
Síntese
A etilenodiamina é produzida industrialmente pelo tratamento de 1,2-dicloroetano com amônia sob pressão a 180 ° C em um meio aquoso:
Nesta reação é gerado cloreto de hidrogênio , que forma um sal com a amina. A amina é liberada pela adição de hidróxido de sódio e pode então ser recuperada por retificação . A dietilenotriamina (DETA) e a trietilenotetramina (TETA) são formadas como subprodutos.
Outra rota industrial para a etilenodiamina envolve a reação de etanolamina e amônia:
Este processo envolve a passagem dos reagentes gasosos sobre um leito de catalisadores heterogêneos de níquel .
Pode ser produzido em laboratório pela reação de etilenoglicol e ureia .
A etilenodiamina pode ser purificada por tratamento com hidróxido de sódio para remover a água seguido de destilação.
Formulários
A etilenodiamina é usada em grandes quantidades para a produção de muitos produtos químicos industriais. Ele forma derivados com ácidos carboxílicos (incluindo ácidos graxos ), nitrilos , álcoois (em temperaturas elevadas), agentes alquilantes, dissulfeto de carbono e aldeídos e cetonas . Devido à sua natureza bifuncional, tendo duas aminas, forma prontamente heterociclos como as imidazolidinas .
Precursor de agentes quelantes, drogas e agroquímicos
Um derivado mais proeminente da etilenodiamina é o agente quelante EDTA , que é derivado da etilenodiamina por meio de uma síntese de Strecker envolvendo cianeto e formaldeído . Hidroxietiletilenodiamina é outro agente quelante comercialmente significativo. Numerosos compostos bioativos e drogas contêm a ligação N-CH 2 -CH 2 -N, incluindo alguns anti-histamínicos . Os sais de etilenobisditiocarbamato são fungicidas comercialmente significativos sob as marcas Maneb , Mancozeb, Zineb e Metiram. Alguns fungicidas contendo imidazolina são derivados da etilenodiamina.
Ingrediente farmacêutico
Etilenodiamina é um ingrediente na comum broncodilatador droga aminofilina , onde serve para solubilizar o ingrediente activo teofilina . A etilenodiamina também tem sido usada em preparações dermatológicas, mas foi removida de algumas por causar dermatite de contato. Quando usado como excipiente farmacêutico, após administração oral sua biodisponibilidade é de cerca de 0,34, devido a um efeito substancial de primeira passagem . Menos de 20% são eliminados por excreção renal .
Os anti - histamínicos derivados da etilenodiamina são os mais antigos das cinco classes de anti-histamínicos de primeira geração , começando com piperoxan também conhecido como benodain, descoberto em 1933 no Instituto Pasteur na França, e também incluindo mepiramina , tripelenamina e antazolina . As outras classes são derivados de etanolamina, alquilamina , piperazina e outros (principalmente compostos tricíclicos e tetracíclicos relacionados a fenotiazinas , antidepressivos tricíclicos , bem como a família ciproheptadina - fenindamina )
Papel em polímeros
A etilenodiamina, por conter dois grupos amina, é um precursor amplamente utilizado de vários polímeros. Os condensados derivados do formaldeído são plastificantes. É amplamente utilizado na produção de fibras de poliuretano. A classe PAMAM de dendrímeros são derivados da etilenodiamina.
Tetraacetiletilenodiamina
O ativador de branqueamento tetraacetiletilenodiamina é gerado a partir da etilenodiamina. O derivado N , N- etilenobis (estearamida) (EBS) é um agente desmoldante comercialmente significativo e um surfactante na gasolina e óleo de motor.
Outras aplicações
- como solvente , é miscível com solventes polares e é usado para solubilizar proteínas como albuminas e caseína . Também é usado em certos banhos de galvanoplastia .
- como inibidor de corrosão em tintas e refrigerantes .
- O di- hidroiodeto de etilenodiamina (EDDI) é adicionado à alimentação animal como fonte de iodeto.
- produtos químicos para revelação de fotografia colorida , aglutinantes , adesivos , amaciantes de roupas , agentes de cura para epóxis e tinturas .
- como um composto para sensibilizar o nitrometano a um explosivo. Esta mistura foi usada no Picatinny Arsenal durante a Segunda Guerra Mundial, dando à mistura de nitrometano e etilenodiamina o apelido de PLX , ou Picatinny Liquid Explosive.
Química de coordenação
A etilenodiamina é um ligante quelante bidentado bem conhecido para compostos de coordenação , com os dois átomos de nitrogênio doando seus pares de elétrons quando a etilenodiamina atua como um ligante. Freqüentemente, é abreviado como "en" em química inorgânica. O complexo [Co (etilenodiamina) 3 ] 3+ é um complexo tris-quelato quiral arquetípico . Os ligantes salen , alguns dos quais são usados na catálise, são derivados da condensação de salicilaldeídos e etilenodiamina.
Ligantes relacionados
Derivados relacionados de etilenodiamina incluem ácido etilenodiaminotetracético (EDTA) , tetrametiletilenodiamina (TMEDA) e tetraetiletilenodiamina (TEEDA). Análogos quirais de etilenodiamina incluem 1,2-diaminopropano e trans- diaminociclohexano .
Segurança
A etilenodiamina, como a amônia e outras aminas de baixo peso molecular, é irritante para a pele e as vias respiratórias. A menos que firmemente contido, a etilenodiamina líquida liberará vapores tóxicos e irritantes em seu entorno, especialmente quando aquecido. Os vapores reagem com a umidade do ar úmido para formar uma névoa branca característica, que é extremamente irritante para a pele, olhos, pulmões e membranas mucosas.
Referências
links externos
![]() Mídia relacionada à etilenodiamina no Wikimedia Commons
Mídia relacionada à etilenodiamina no Wikimedia Commons



