Ferrochelatase - Ferrochelatase
| Ferrochelatase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Ferrochelatase humana
| |||||||||
| Identificadores | |||||||||
| EC nº | 4.99.1.1 | ||||||||
| CAS no. | 9012-93-5 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologia Genética | AmiGO / QuickGO | ||||||||
| |||||||||
| Ferrochelatase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | Ferrochelatase | ||||||||
| Pfam | PF00762 | ||||||||
| InterPro | IPR001015 | ||||||||
| PRÓSITO | PDOC00462 | ||||||||
| SCOP2 | 1ak1 / SCOPe / SUPFAM | ||||||||
| Superfamília OPM | 129 | ||||||||
| Proteína OPM | 1hrk | ||||||||
| |||||||||
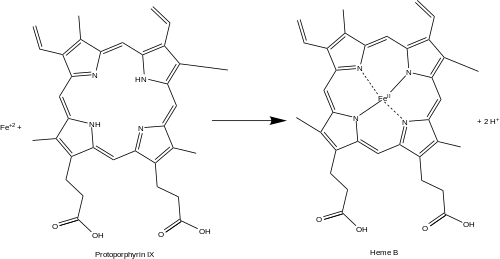
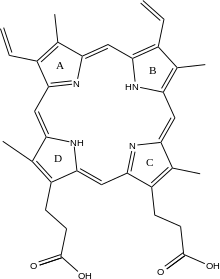
Ferrochelatase (ou protoporfirina ferrochelatase) é uma enzima que é codificada pelo gene FECH em humanos. Ferroquelatase catalisa o passo oitavo e terminal na biossíntese de heme , a conversão de protoporf irina IX em heme B . Catalisa a reação:
- protoporfirina + Fe +2 ⇌ heme B + 2 H +
Função

A ferroquelatase catalisa a inserção de ferro ferroso na protoporfirina IX na via de biossíntese do heme para formar o heme B. A enzima está localizada no lado voltado para a matriz da membrana mitocondrial interna. Ferroquelatase é o mais conhecido membro de uma família de enzimas que adicionam divalentes de metal catiões para estruturas de tetrapirrole. Por exemplo, a quelatase de magnésio adiciona magnésio à protoporfirina IX na primeira etapa da biossíntese de bacterioclorofila .
Heme B é um cofator essencial em muitas proteínas e enzimas. Em particular, o heme b desempenha um papel fundamental como transportador de oxigênio na hemoglobina nos glóbulos vermelhos e na mioglobina nas células musculares . Além disso, o heme B é encontrado no citocromo b , um componente chave na Q-citocromo c oxidoredutase (complexo III) na fosforilação oxidativa .
Estrutura
A ferrochelatase humana é um homodímero composto por duas cadeias polipeptídicas de 359 aminoácidos. Tem um peso molecular total de 85,07 kDa. Cada subunidade é composta por cinco regiões: uma sequência de localização mitocondrial , o domínio N terminal, dois domínios dobrados e uma extensão C terminal. Os resíduos 1–62 formam um domínio de localização mitocondrial que é clivado na modificação pós-tradução . Os domínios dobrados contêm um total de 17 hélices α e 8 folhas β . A extensão do terminal C contém três dos quatro resíduos de cisteína (Cys403, Cys406, Cys411) que coordenam o cluster catalítico ferro-enxofre (2Fe-2S) . A quarta cisteína de coordenação reside no domínio N-terminal (Cys196).
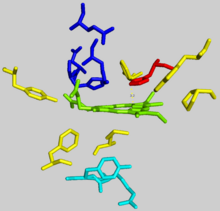
O bolso ativo da ferrocheltase consiste em dois "lábios" hidrofóbicos e um interior hidrofílico. Os lábios hidrofóbicos, consistindo nos resíduos altamente conservados 300–311, estão voltados para a membrana mitocondrial interna e facilitam a passagem do substrato protoporfirina IX fracamente solúvel e do produto heme através da membrana. O interior da bolsa do sítio ativo contém uma superfície ácida altamente conservada que facilita a extração de prótons da protoporfirina. Os resíduos de histidina e aspartato a cerca de 20 angstroms do centro do sítio ativo no lado da matriz mitocondrial da ligação do metal coordenada da enzima.
Mecanismo
O mecanismo de metalação da protoporfirina humana permanece sob investigação. Muitos pesquisadores levantaram a hipótese de que a distorção do macrociclo da porfirina é a chave para a catálise. Os pesquisadores que estudam a ferrochelatase Bacillus subtilis propõem um mecanismo para a inserção do ferro na protoporfirina em que a enzima agarra firmemente os anéis B, C e D enquanto dobra o anel A 36 o . Normalmente planar, essa distorção expõe o único par de elétrons no nitrogênio no anel A ao íon Fe + 2 . A investigação subsequente revelou uma distorção de 100 o na protoporfirina ligada à ferrochelatase humana. Um resíduo de histidina altamente conservado (His183 em B. subtilis , His263 em humanos) é essencial para determinar o tipo de distorção, além de atuar como aceptor inicial de prótons da protoporfirina. Os resíduos aniônicos formam uma via que facilita o movimento do próton para longe da histidina catalítica. A frataxina chaperona o ferro para o lado da matriz da ferrochelatase, onde os resíduos de aspartato e histidina em ambas as proteínas coordenam a transferência de ferro para a ferrochelatase. Dois resíduos de arginina e tirosina no sítio ativo (Arg164, Tyr165) podem realizar a metalação final.
Significado clínico
Defeitos na ferrochelatase criam um acúmulo de protoporfirina IX, causando protoporfiria eritropoiética (EPP). A doença pode resultar de uma variedade de mutações na FECH, a maioria das quais se comporta de maneira autossômica dominante com baixa penetrância clínica. Clinicamente, os pacientes com PPE apresentam uma variedade de sintomas, desde assintomáticos a sofrendo de fotossensibilidade extremamente dolorosa . Em menos de 5% dos casos, o acúmulo de protoporfirina no fígado resulta em colestase (bloqueio do fluxo biliar do fígado para o intestino delgado) e insuficiência hepática terminal .
Em casos de envenenamento por chumbo , o chumbo inibe a atividade da ferrochelatase, em parte resultando em porfiria.
Interações
A ferroquelatase interage com várias outras enzimas envolvidas na biossíntese, catabolismo e transporte do heme , incluindo protoporfirinogênio oxidase , 5-aminolevulinato sintase , ABCB10 , ABCB7 , succinil-CoA sintetase e mitoferrin-1. Vários estudos sugeriram a existência de um complexo oligomérico que permite a canalização do substrato e a coordenação do metabolismo geral do ferro e da porfirina em toda a célula. A N-metilmesoporfirina (N-MeMP) é um inibidor competitivo com a protoporfirina IX e é considerada um análogo do estado de transição. Como tal, o N-MeMP foi usado extensivamente como um ligante estabilizador para a determinação da estrutura da cristalografia de raios-x . A frataxina atua como a chaperona Fe +2 e complexas com a ferrochelatase em seu lado da matriz mitocondrial. A ferroquelatase também pode inserir outros íons metálicos divalentes na protoporfirina. Alguns íons, como Zn +2 , Ni e Co, formam outras metaloporfirinas, enquanto íons de metais mais pesados, como Mn , Pb , Hg e Cd, inibem a liberação do produto após a metalização.
Veja também
Referências
Leitura adicional
- Cox TM (junho de 1997). "Protoporfiria eritropoiética". Journal of Inherited Metabolic Disease . 20 (2): 258–69. doi : 10.1023 / A: 1005317124985 . PMID 9211198 . S2CID 12493042 .
- Brenner DA, Didier JM, Frasier F, Christensen SR, Evans GA, Dailey HA (junho de 1992). "Um defeito molecular na protoporfiria humana" . American Journal of Human Genetics . 50 (6): 1203–10. PMC 1682545 . PMID 1376018 .
- Nakahashi Y, Fujita H, Taketani S, Ishida N, Kappas A, Sassa S (janeiro de 1992). "O defeito molecular da ferrochelatase em um paciente com protoporfiria eritropoiética" . Anais da Academia Nacional de Ciências dos Estados Unidos da América . 89 (1): 281–5. Bibcode : 1992PNAS ... 89..281N . doi : 10.1073 / pnas.89.1.281 . PMC 48220 . PMID 1729699 .
- Lamoril J, Boulechfar S, de Verneuil H, Grandchamp B, Nordmann Y, Deybach JC (dezembro de 1991). "Protoporfiria eritropoiética humana: duas mutações pontuais no gene da ferrochelatase". Comunicações de pesquisa bioquímica e biofísica . 181 (2): 594–9. doi : 10.1016 / 0006-291X (91) 91231-Z . PMID 1755842 .
- Nakahashi Y, Taketani S, Okuda M, Inoue K, Tokunaga R (dezembro de 1990). "Molecular cloning and sequence analysis of cDNA encoding human ferrochelatase". Comunicações de pesquisa bioquímica e biofísica . 173 (2): 748–55. doi : 10.1016 / S0006-291X (05) 80099-3 . PMID 2260980 .
- Rossi E, Attwood PV, Garcia-Webb P, Costin KA (maio de 1990). "Inibição da atividade da ferrochelatase de linfócitos humanos pela hemina". Biochimica et Biophysica Acta (BBA) - Estrutura de Proteínas e Enzimologia Molecular . 1038 (3): 375–81. doi : 10.1016 / 0167-4838 (90) 90251-A . PMID 2340297 .
- Polson RJ, Lim CK, Rolles K., Calne RY, Williams R (setembro de 1988). "O efeito do transplante de fígado em um menino de 13 anos com protoporfiria eritropoiética". Transplante . 46 (3): 386–9. doi : 10.1097 / 00007890-198809000-00010 . PMID 3047929 .
- Bonkovsky HL, Schned AR (janeiro de 1986). "Insuficiência hepática fatal na protoporfiria. Sinergismo entre o excesso de etanol e o defeito genético". Gastroenterology . 90 (1): 191–201. doi : 10.1016 / 0016-5085 (86) 90093-4 . PMID 3940245 .
- Prasad AR, Dailey HA (agosto de 1995). "Efeito da localização celular na função da ferrochelatase" . The Journal of Biological Chemistry . 270 (31): 18198–200. doi : 10.1074 / jbc.270.31.18198 . PMID 7629135 .
- Sarkany RP, Alexander GJ, Cox TM (junho de 1994). "Herança recessiva de protoporfiria eritropoiética com insuficiência hepática". Lancet . 343 (8910): 1394–6. doi : 10.1016 / S0140-6736 (94) 92525-9 . PMID 7910885 . S2CID 42243172 .
- Tugores A, Magness ST, Brenner DA (dezembro de 1994). "Um único promotor dirige a expressão preferencial de manutenção e eritróide do gene da ferrochelatase humana" . The Journal of Biological Chemistry . 269 (49): 30789–97. doi : 10.1016 / S0021-9258 (18) 47351-6 . PMID 7983009 .
- Dailey HA, Sellers VM, Dailey TA (janeiro de 1994). "Ferrochelatase de mamífero. Expressão e caracterização de ferrochelatases protoporfíricas normais e duas humanas" . The Journal of Biological Chemistry . 269 (1): 390–5. doi : 10.1016 / S0021-9258 (17) 42362-3 . PMID 8276824 .
- Wang X, Poh-Fitzpatrick M, Carriero D, Ostasiewicz L, Chen T, Taketani S, Piomelli S (abril de 1993). "Uma nova mutação em protoporfiria eritropoiética: um mRNA de ferrochelatase aberrante causado por salto de exon durante o splicing de RNA". Biochimica et Biophysica Acta (BBA) - Molecular Basis of Disease . 1181 (2): 198–200. doi : 10.1016 / 0925-4439 (93) 90112-e . PMID 8481408 .
- Nakahashi Y, Miyazaki H, Kadota Y, Naitoh Y, Inoue K, Yamamoto M, Hayashi N, Taketani S (maio de 1993). "Defeito molecular na protoporfiria eritropoiética humana com insuficiência hepática fatal". Genética Humana . 91 (4): 303–6. doi : 10.1007 / BF00217346 . PMID 8500787 . S2CID 5844599 .
- Imoto S, Tanizawa Y, Sato Y, Kaku K, Oka Y (julho de 1996). "Uma nova mutação no gene da ferrochelatase associada à protoporfiria eritropoiética". British Journal of Hematology . 94 (1): 191–7. doi : 10.1046 / j.1365-2141.1996.d01-1771.x . PMID 8757534 . S2CID 27290533 .
- Crouse BR, Sellers VM, Finnegan MG, Dailey HA, Johnson MK (dezembro de 1996). "Mutagênese dirigida ao local e caracterização espectroscópica da ferrochelatase humana: identificação de resíduos que coordenam o cluster [2Fe-2S]". Bioquímica . 35 (50): 16222–9. doi : 10.1021 / bi9620114 . PMID 8973195 .
links externos
- Orientação UMich de Proteínas em Proteína de Membranas / pdbid-1hrk
- Ferrochelatase nos cabeçalhos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)