Volatilidade de flúor - Fluoride volatility
A volatilidade do flúor é a tendência das moléculas altamente fluoradas a vaporizarem em temperaturas comparativamente baixas. Heptafluoretos , hexafluoretos e pentafluoretos têm pontos de ebulição muito mais baixos do que os fluoretos de menor valência . A maioria dos difluoretos e trifluoretos têm altos pontos de ebulição, enquanto a maioria dos tetrafluoretos e monofluoretos ficam entre os dois. O termo "volatilidade de fluoreto" é um jargão usado particularmente no contexto da separação de radionuclídeos .
Volatilidade e valência
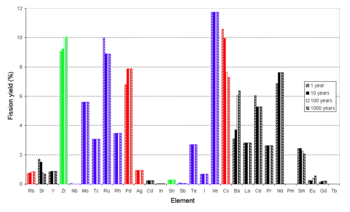
As valências para a maioria dos elementos são baseadas no mais alto flúor conhecido.
Grosso modo, a volatilidade do fluoreto pode ser usada para remover elementos com valência 5 ou maior: urânio , neptúnio , plutônio , metalóides ( telúrio , antimônio ), não metais ( selênio ), halogênios ( iodo , bromo ) e os metais de transição intermediários ( nióbio , molibdênio , tecnécio , rutênio e possivelmente ródio ). Esta fração inclui os actinídeos mais facilmente reutilizáveis como combustível nuclear em um reator térmico e os dois produtos de fissão de longa duração mais adequados para descarte por transmutação, Tc-99 e I-129 , bem como Se-79 .
Gases nobres ( xenônio , criptônio ) são voláteis mesmo sem fluoretação e não se condensam, exceto em temperaturas muito mais baixas.
Deixados para trás estão os metais alcalinos ( césio , rubídio ), metais alcalino-terrosos ( estrôncio , bário ), lantanídeos , os actinídeos restantes ( amerício , cúrio ), metais de transição restantes ( ítrio , zircônio , paládio , prata ) e metais pós-transição ( estanho , índio , cádmio ). Esta fração contém os produtos de fissão que são riscos de radiação em uma escala de décadas ( Cs-137 , Sr-90 , Sm-151 ), os quatro produtos de fissão de longa vida restantes Cs-135 , Zr-93 , Pd-107 , Sn -126 dos quais apenas o último emite radiação forte, a maioria dos venenos de nêutrons e os actinídeos superiores ( amerício , cúrio , califórnio ) que são riscos de radiação em uma escala de centenas ou milhares de anos e são difíceis de trabalhar por causa da gama radiação, mas são fissionáveis em um reator rápido .
Métodos de reprocessamento
Os óxidos de urânio reagem com o flúor para formar hexafluoreto de urânio gasoso , a maior parte do plutônio reage para formar hexafluoreto de plutônio gasoso, a maioria dos produtos de fissão (especialmente elementos eletropositivos: lantanídeos , estrôncio , bário , ítrio , césio ) formam fluoretos não voláteis. Poucos metais nos produtos de fissão (os metais de transição nióbio , rutênio , tecnécio , molibdênio e iodo halógeno ) formam fluoretos voláteis (ponto de ebulição <200 ° C) que acompanham os hexafluoretos de urânio e plutônio, juntamente com gases inertes . A destilação é então usada para separar o hexafluoreto de urânio da mistura.
Os produtos de fissão alcalina não volátil e actinídeos menores são mais adequados para processamento posterior com métodos não aquosos de processamento eletroquímico "seco" ( piroquímico ) . Os fluoretos de lantanídeos são difíceis de dissolver no ácido nítrico usado para métodos de reprocessamento aquoso, como PUREX , DIAMEX e SANEX , que usam extração com solvente . A volatilidade do flúor é apenas um dos vários processos piroquímicos projetados para reprocessar o combustível nuclear usado.
O instituto de investigação nuclear rez em rez na República Checa testado doseadores de parafuso que alimentados óxido de urânio chão (simulando pastilhas de combustível usado) num fluorinator onde as partículas foram queimados em gás de flúor a forma hexafluoreto de urânio .
A Hitachi desenvolveu uma tecnologia, chamada FLUOREX, que combina a volatilidade do flúor, para extrair urânio, com a extração mais tradicional por solvente (PUREX), para extrair plutônio e outros transurânicos]. O ciclo de combustível baseado em FLUOREX deve ser usado com o reator de água de moderação reduzida .
Tabela de propriedades relevantes
|
Fluoreto |
Z |
Ebulição ° C |
Derretendo ° C |
Meia - vida chave |
Produção |
|---|---|---|---|---|---|
| SeF 6 | 34 | -46,6 | -50,8 | 79 Se: 65ky | 0,04% |
| TeF 6 | 52 | -39 | -38 | 127m Te: 109d | |
| IF 7 | 53 | 4,8 (1 atm) | 6,5 ( triponto ) | 129 I: 15,7 meu | 0,54% |
| MoF 6 | 42 | 34 | 17,4 | 99 Mo: 2,75d | |
| PuF 6 | 94 | 62 | 52 | 239 Pu : 24ky | |
| TcF 6 | 43 | 55,3 | 37,4 | 99 Tc : 213ky | 6,1% |
| NpF 6 | 93 | 55,18 | 54,4 | 237 Np : 2,14 meu | |
| UF 6 | 92 | 56,5 (subl) | 64,8 | 233 U : 160ky | |
| RuF 6 | 44 | 54 | 106 Ru: 374d | ||
| RhF 6 | 45 | 70 | 103 Rh: estável | ||
| ReF 7 | 75 | 73,72 | 48,3 | Não FP | |
| BrF 5 | 35 | 40,25 | -61,30 | 81 Br: estável | |
| IF 5 | 53 | 97,85 | 9,43 | 129 I: 15,7 meu | 0,54% |
| XeF 2 | 54 | 114,25 ( subl ) | 129,03 ( tripoint ) | ||
| SbF 5 | 51 | 141 | 8,3 | 125 Sb: 2,76y | |
| RuOF 4 | 44 | 184 | 115 | 106 Ru: 374d | |
| RuF 5 | 44 | 227 | 86,5 | 106 Ru: 374d | |
| NbF 5 | 41 | 234 | 79 | 95 Nb: 35d | baixo |
| PdF 4 | 46 | 107 Pd: 6,5 meu | |||
| SnF 4 | 50 | 750 (subl) | 705 |
121m1 Sn: 44y 126 Sn: 230ky |
0,013% ? |
| ZrF 4 | 40 | 905 | 932 (triponto) | 93 Zr: 1,5 my | 6,35% |
| AgF | 47 | 1159 | 435 | 109 Ag: estável | |
| CsF | 55 | 1251 | 682 |
137 Cs : 30,2y 135 Cs: 2,3my |
6,19% 6,54% |
| BeF 2 | 4 | 1327 | 552 | ||
| RbF | 37 | 1410 | 795 | ||
| UF 4 | 92 | 1417 | 1036 | 233 U : 160ky | |
| FLiBe | 1430 | 459 | estábulo | ||
| FLiNaK | 1570 | 454 | estábulo | ||
| LiF | 3 | 1676 | 848 | estábulo | |
| KF | 19 | 1502 | 858 | 40 K: 1,25Gy | |
| NaF | 11 | 1704 | 993 | estábulo | |
| ThF 4 | 90 | 1680 | 1110 | ||
| CdF 2 | 48 | 1748 | 1110 | 113m Cd: 14,1y | |
| YF 3 | 39 | 2230 | 1150 | 91 Y: 58.51d | |
| InF 3 | 49 | > 1200 | 1170 | ||
| BaF 2 | 56 | 2260 | 1368 | 140 Ba: 12,75d | |
| TbF 3 | 65 | 2280 | 1172 | ||
| GdF 3 | 64 | 1231 | 159 Gd: 18,5h | ||
| PmF 3 | 61 | 1338 | 147 Pm: 2,62y | ||
| EuF 3 | 63 | 2280 | 1390 | 155 Eu: 4,76y | |
| NdF 3 | 60 | 2300 | 1374 | 147 Nd: 11d | |
| PrF 3 | 59 | 1395 | 143 Pr: 13,57d | ||
| CeF 3 | 58 | 2327 | 1430 | 144 Ce: 285d | |
| SmF 3 | 62 | 2427 | 1306 | 151 Sm : 90y | 0,419% ? |
| SrF 2 | 38 | 2460 | 1477 | 90 Sr : 29.1y | 5,8% |
| LaF 3 | 57 | 1493 | 140 La: 1,68d |
Veja também
Notas
- Principais fluoretos ausentes:
- PrF 4 (porque se decompõe a 90 ° C)
- TbF 4 (porque se decompõe a 300 ° C)
- CeF 4 (porque se decompõe a 600 ° C)
- Sem fluoretos estáveis: Kr, Xe, Pd
Referências
links externos
- Estudo de processos eletroquímicos para separação de actinídeos e lantanídeos em meios de fluoreto fundido ( PDF )
- "Separação e purificação de UF 6 de fluoretos voláteis por retificação" (PDF) . Arquivado do original (PDF) em 13 de janeiro de 2005.
- Destilação de baixa pressão de uma porção do sal carreador de combustível do Experimento de Reator de Sal Fundido (PDF)
- Uso do Processo de Volatilidade de Fluoreto para Extrair Tecnécio do Combustível Nuclear Usado Transmutado (PDF)
- Uma revisão por pares da estratégia para caracterizar contaminação por transurânicos e tecnécio em cilindros caudas de hexafluoreto de urânio empobrecido (PDF)
- CONSTANTES FÍSICOS DE COMPOSTOS INORGÂNICOS (PDF)
