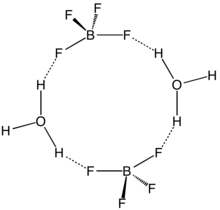
Ácido fluorobórico - Fluoroboric acid

|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Ácido tetrafluorobórico |
|
| Outros nomes
ácido tetrafluorobórico, tetrafluoroboranuida de oxônio, tetrafluoridoborato de oxônio (1-)
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.037.165 |
| Número EC | |
| 21702 | |
| Malha | Fluorobórico + ácido |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | 1775 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| B F 4 H | |
| Massa molar | 87,81 g · mol −1 |
| Aparência | Líquido incolor |
| Ponto de fusão | −90 ° C (−130 ° F; 183 K) |
| Ponto de ebulição | 130 ° C (266 ° F; 403 K) |
| Acidez (p K a ) | ~ 1.8 (solução MeCN) |
| Perigos | |
| Ficha de dados de segurança | MSDS externo |
|
|
|
| Frases R (desatualizado) | R34 |
| Frases S (desatualizado) | (S1 / 2) , S26 , S27 , S45 |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Compostos relacionados
|
Fluoreto de hidrogénio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O ácido fluorobórico ou ácido tetrafluorobórico (arcaicamente, ácido fluobórico ) é um composto inorgânico com a fórmula química [H + ] [BF 4 - ], onde H + representa o próton solvatado. O solvente pode ser qualquer entidade básica de Lewis adequada. Por exemplo, na água, pode ser representado por H
3OBF
4(tetrafluoroborato de oxônio), embora de forma mais realista, várias moléculas de água solvatam o próton: [H (H 2 O) n + ] [BF 4 - ]. O solvato de éter etílico também está disponível comercialmente: [H (Et 2 O) n + ] [BF 4 - ], onde n é mais provavelmente 2. Ao contrário de ácidos fortes como H 2 SO 4 ou HClO 4 , a substância pura não solvatada não existem (veja abaixo).
É produzido principalmente como precursor de outros sais de fluoroborato. É um ácido forte . O ácido fluorobórico é corrosivo e ataca a pele. Ele está disponível comercialmente como uma solução em água e outros solventes , como éter dietílico . É um ácido forte com uma base conjugada não oxidante e de coordenação fraca . É estruturalmente semelhante ao ácido perclórico , mas não apresenta os perigos associados aos oxidantes .
Estrutura e produção
HBF 4 puro foi descrito como um "composto inexistente", visto que se espera que um próton suficientemente 'nu' abstraia um fluoreto do íon tetrafluoroborato para dar fluoreto de hidrogênio e trifluoreto de boro : [H + ] [BF 4 - ] → HF + BF 3 . (O mesmo vale para os superácidos que são conhecidos pelas fórmulas simples HPF 6 e HSbF 6. ) No entanto, uma solução de BF 3 em HF é altamente ácida, tendo uma especiação aproximada de [H 2 F + ] [BF 4 - ] e uma função de acidez de Hammett de –16.6 a 7 mol% BF 3 , facilmente qualificado como um superácido. Embora o HBF 4 sem solvente não tenha sido isolado, seus solvatos estão bem caracterizados. Estes sais consistem em solvente protonado como um cátion, por exemplo, H 3 O + e H
5O+
2, e o BF tetraédrico-
4ânion. O ânion e os cátions são fortemente ligados por hidrogênio.
Soluções aquosas de HBF 4 são produzidas dissolvendo ácido bórico em ácido fluorídrico aquoso . Três equivalentes de HF reagem para dar o trifluoreto de boro intermediário e o quarto dá ácido fluorobórico:
- B (OH) 3 + 4 HF → H 3 O + + BF-
4+ 2 H 2 O
As soluções anidras podem ser preparadas por tratamento de ácido fluorobórico aquoso com anidrido acético .
Acidez
A acidez do ácido fluorobórico é complicada pelo fato de que o nome se refere a várias espécies diferentes H (OEt 2 ) + BF-
4, H 3 O + BF-
4e HF . BF 3 - cada um com uma acidez diferente. A fase aquosa pKa um é citado como -0,44. Titulação de NBu+
4BF-
4em solução de acetonitrila indica que HBF 4 , isto é, HF . BF 3 , tem um pK a de 1,6 nesse solvente. Sua acidez é, portanto, comparável à do ácido fluorossulfônico .
Formulários
O ácido fluorobórico é o principal precursor dos sais de fluoroborato , que são tipicamente preparados tratando os óxidos de metal com ácido fluorobórico. Os sais inorgânicos são intermediários na fabricação de materiais retardadores de chama e fritas de envidraçamento e na geração eletrolítica de boro . O HBF 4 também é usado em corrosão de alumínio e decapagem ácida.
Química orgânica
HBF 4 é usado como um catalisador para alquilações e polimerizações . Em reações de proteção de carboidratos, o ácido fluorobórico etéreo é um catalisador eficiente e de baixo custo para reações de transacetalação e isopropilidenação. As soluções de acetonitrila clivam os acetais e alguns éteres . Muitos cátions reativos foram obtidos usando ácido fluorobórico , por exemplo, tetrafluoroborato de tropílio ( C
7H+
7BF-
4), trifenilmetil tetrafluoroborato ( Ph
3C+
BF-
4), tetrafluoroborato de trietiloxônio ( Et
3O+
BF-
4), e tetrafluoroborato de benzenediazônio ( PhN+
2BF-
4)
Galvanoplastia
Soluções de HBF 4 são utilizadas na galvanoplastia de estanho e ligas de estanho. Nesta aplicação, o ácido metanossulfônico está substituindo o uso de HBF 4 .
Segurança
O HBF 4 é tóxico e ataca a pele e os olhos. Ele ataca o vidro. Ele hidrolisa, liberando fluoreto de hidrogênio volátil e corrosivo .
Outros ácidos fluorobóricos
Uma série de ácidos fluorobóricos é conhecida em soluções aquosas. A série pode ser apresentada da seguinte forma:
- H [B (OH) 4 ]
- H [BF (OH) 3 ]
- H [BF 2 (OH) 2 ]
- H [BF 3 (OH)]
- H [BF 4 ]
Veja também
Referências
Leitura adicional
- Albert, R .; Dax, K .; Pleschko, R .; Stütz, AE (1985). "Ácido tetrafluorobórico, um catalisador eficiente nas reações de proteção e desproteção de carboidratos". Carbohydrate Research . 137 : 282–290. doi : 10.1016 / 0008-6215 (85) 85171-5 .
- Bandgar, BP; Patil, AV; Chavan, OS (2006). "Ácido fluorobórico com suporte de sílica como um catalisador novo, eficiente e reutilizável para a síntese de 1,5-benzodiazepinas em condições livres de solvente". Journal of Molecular Catalysis A: Chemical . 256 (1–2): 99–105. doi : 10.1016 / j.molcata.2006.04.024 .
- Heintz, RA; Smith, JA; Szalay, PS; Weisgerber, A .; Dunbar, KR (2002). Cátions de acetonitrila de metal de transição homoléptica com ânions tetrafluoroborato ou trifluorometanossulfonato . Sínteses inorgânicas. 33 . pp. 75–83. doi : 10.1002 / 0471224502 . ISBN 9780471208259.
- Housecroft, CE; Sharpe, AG (2004). Inorganic Chemistry (2ª ed.). Prentice Hall. p. 307. ISBN 978-0-13-039913-7.
- Meller, A. (1988). "Boro". Gmelin Handbook of Inorganic Chemistry . 3 . Nova York: Springer-Verlag. pp. 301–310.
- Perry, DL; Phillips, SL (1995). Handbook of Inorganic Compounds (1ª ed.). Boca Raton: CRC Press. p. 1203. ISBN 9780849386718.
- Wamser, CA (1948). "Hydrolysis of Fluoboric Acid in Aqueous Solution". Journal of the American Chemical Society . 70 (3): 1209–1215. doi : 10.1021 / ja01183a101 .
- Wilke-Dörfurt, E .; Balz, G. (1927). "Zur Kenntnis der Borfluorwasserstoffsäure und ihrer Salze". Zeitschrift für Anorganische und Allgemeine Chemie . 159 (1): 197–225. doi : 10.1002 / zaac.19271590118 .
links externos
- "Fluoroboric Acid ICSC: 1040" . INCHEM.