Fulvalene - Fulvalene
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
[1,1′-Bi (ciclopentilideno)] - 2,2 ′, 4,4′-tetraeno |
|
| Outros nomes
Biciclopentiliden-2,4,2 ′, 4′-tetraeno
1,1′-Bi [ciclopentadienilideno] Pentafulvaleno Biciclopentadienilideno [5,5 ′] Biciclopentadienilideno |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
|
PubChem CID
|
|
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 10 H 8 | |
| Massa molar | 128,174 g · mol −1 |
| Densidade | 1,129 g / ml |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
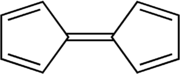
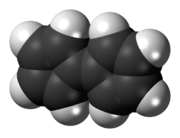
Fulvaleno ( biciclopentadienilideno ) é o membro da família fulvaleno com a fórmula molecular C 10 H 8 . É de interesse teórico como um dos hidrocarbonetos conjugados não benzenoides mais simples . O fulvaleno é um isômero instável dos compostos aromáticos benzenoides mais comuns, naftaleno e azuleno . Fulvalene consiste em dois anéis de 5 membros, cada um com duas ligações duplas , unidas por uma quinta ligação dupla. Possui simetria D 2h .
História
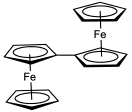
Uma tentativa anterior de síntese de fulvaleno em 1951 por Pauson e Kealy resultou na descoberta acidental de ferroceno . Sua síntese foi relatada pela primeira vez em 1958 por EA Matzner, trabalhando com William von Eggers Doering . Neste método, o ânion ciclopentadienil é acoplado ao iodo ao dihidrofulvaleno. A desprotonação dupla do diidrofulvaleno com n- butil-lítio dá o derivado dilítio, que se oxida com o oxigênio. O fulvaleno foi espectroscopicamente observado a −196 ° C (77 K) a partir da fotólise do diazociclopentadieno , que induz a dimerização de carbenos derivados do ciclopentadieno . O composto foi isolado em 1986. Descobriu-se que não era aromático. Acima de −50 ° C (223 K), ele se dimeriza por uma reação de Diels-Alder .
Derivados
Perclorofulvaleno (C 4 Cl 4 C) 2 é bastante estável em contraste com o próprio fulvaleno.
Veja também
- Fulvenos , (CH = CH) 2 C = CH 2 e derivados substituídos
- Tetratiafulvaleno , C 2 H 2 S 2 C = CS 2 C 2 H 2
