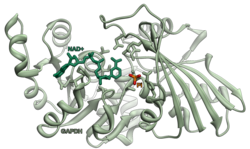
Gliceraldeído 3-fosfato desidrogenase - Glyceraldehyde 3-phosphate dehydrogenase
| Gliceraldeído 3-fosfato desidrogenase, domínio de ligação de NAD | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 determinantes da termoestabilidade da enzima observada na estrutura molecular de thermus aquaticus d-gliceraldeído-3-fosfato desidrogenase com resolução de 2,5 angstroms
| |||||||||
| Identificadores | |||||||||
| Símbolo | Gp_dh_N | ||||||||
| Pfam | PF00044 | ||||||||
| Clã Pfam | CL0063 | ||||||||
| InterPro | IPR020828 | ||||||||
| PRÓSITO | PDOC00069 | ||||||||
| SCOP2 | 1gd1 / SCOPe / SUPFAM | ||||||||
| |||||||||
| Gliceraldeído 3-fosfato desidrogenase, domínio C-terminal | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 estrutura cristalina da gliceraldeído-3-fosfato desidrogenase de pyrococcus horikoshii ot3
| |||||||||
| Identificadores | |||||||||
| Símbolo | Gp_dh_C | ||||||||
| Pfam | PF02800 | ||||||||
| Clã Pfam | CL0139 | ||||||||
| InterPro | IPR020829 | ||||||||
| PRÓSITO | PDOC00069 | ||||||||
| SCOP2 | 1gd1 / SCOPe / SUPFAM | ||||||||
| |||||||||
Gliceraldeído 3-fosfato desidrogenase (abreviado GAPDH ) ( EC 1.2.1.12 ) é uma enzima de cerca de 37 kDa que catalisa a sexta etapa da glicólise e, portanto, serve para quebrar a glicose para obter energia e moléculas de carbono. Além dessa função metabólica estabelecida há muito tempo, GAPDH foi recentemente implicado em vários processos não metabólicos, incluindo ativação da transcrição , início da apoptose , transporte de vesículas de ER para Golgi e transporte axonal rápido ou axoplasmático . No esperma, uma isoenzima GAPDHS específica do testículo é expressa.
Estrutura
Em condições celulares normais, o GAPDH citoplasmático existe principalmente como um tetrâmero . Esta forma é composta por quatro subunidades idênticas de 37 kDa contendo um único grupo tiol catalítico cada e crítico para a função catalítica da enzima. O GAPDH nuclear aumentou o ponto isoelétrico (pI) de pH 8,3-8,7. Digno de nota, o resíduo de cisteína C152 no sítio ativo da enzima é necessário para a indução da apoptose por estresse oxidativo . Notavelmente, as modificações pós-tradução de GAPDH citoplasmático contribuem para suas funções fora da glicólise.
GAPDH é codificado por um único gene que produz um único transcrito de mRNA com 8 variantes de splice, embora exista uma isoforma como um gene separado que é expresso apenas em espermatozóides .
Reação
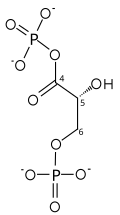
| gliceraldeído 3-fosfato | gliceraldeído fosfato desidrogenase | D - glicerato 1,3-bisfosfato | |

|
|
||
| NAD + + P i | NADH + H + | ||

|
|||
| NAD + + P i | NADH + H + | ||
Composto C00118 no banco de dados KEGG Pathway. Enzyme 1.2.1.12 em KEGG Pathway Database. Reaction R01063 no banco de dados KEGG Pathway. Composto C00236 no banco de dados KEGG Pathway.
Conversão de duas etapas de G3P
A primeira reação é a oxidação do gliceraldeído 3-fosfato (G3P) na posição 1 (no diagrama é mostrado como o 4º carbono da glicólise), em que um aldeído é convertido em um ácido carboxílico (ΔG ° '= - 50 kJ / mol (−12kcal / mol)) e NAD + é simultaneamente reduzido endergonicamente para NADH.
A energia libertada por esta altamente exergônicas unidades da reacção de oxidação a endergônica segunda reacção (? G ° '= + 50 kJ / mol (+ 12kcal / mol)), em que uma molécula de inorgânica de fosfato é transferido para a GAP intermediário para formar um produto com alto potencial de transferência de fosforil: 1,3-bisfosfoglicerato (1,3-BPG).
Este é um exemplo de fosforilação acoplada à oxidação, e a reação geral é um tanto endergônica (ΔG ° '= + 6,3 kJ / mol (+1,5)). O acoplamento de energia aqui é possibilitado pelo GAPDH.
Mecanismo
GAPDH usa catálise covalente e catálise de base geral para diminuir a energia de ativação muito grande da segunda etapa (fosforilação) desta reação.
1: Oxidação
Primeiro, um resíduo de cisteína no sítio ativo de GAPDH ataca o grupo carbonila de GAP, criando um intermediário hemitioacetal (catálise covalente).
O hemitioacetal é desprotonado por um resíduo de histidina no sítio ativo da enzima (catálise de base geral). A desprotonação estimula a reforma do grupo carbonila no intermediário tioéster subsequente e a ejeção de um íon hidreto .
Em seguida, uma molécula adjacente de NAD + fortemente ligada aceita o íon hidreto , formando NADH enquanto o hemitioacetal é oxidado a um tioéster .
Esta espécie de tioéster é muito mais alta em energia (menos estável) do que as espécies de ácido carboxílico que resultariam se GAP fosse oxidado na ausência de GAPDH (a espécie de ácido carboxílico é tão baixa em energia que a barreira de energia para a segunda etapa da reação (fosforilação) seria muito alta, e a reação, portanto, muito lenta e desfavorável para um organismo vivo).
2: Fosforilação
O NADH deixa o sítio ativo e é substituído por outra molécula de NAD + , cuja carga positiva estabiliza o oxigênio carbonil carregado negativamente no estado de transição da etapa seguinte e final. Finalmente, uma molécula de fosfato inorgânico ataca o tioéster e forma um intermediário tetraédrico, que então entra em colapso para liberar 1,3-bisfosfoglicerato e o grupo tiol do resíduo de cisteína da enzima.
Regulamento
Esta proteína pode usar o modelo de morfeína de regulação alostérica .
Função
Metabólico
Como seu nome indica, gliceraldeído 3-fosfato desidrogenase (GAPDH) catalisa a conversão de gliceraldeído 3-fosfato em D - glicerato 1,3-bifosfato . Esta é a 6ª etapa na quebra glicolítica da glicose, uma importante via de fornecimento de energia e molécula de carbono que ocorre no citosol das células eucarióticas. A conversão ocorre em duas etapas acopladas. A primeira é favorável e permite que a segunda etapa desfavorável ocorra.
Transcrição e apoptose
O próprio GAPDH pode ativar a transcrição . O complexo coativador transcricional OCA-S contém GAPDH e lactato desidrogenase , duas proteínas que antes só se pensava estar envolvidas no metabolismo . GAPDH se move entre o citosol e o núcleo e pode, assim, ligar o estado metabólico à transcrição do gene.
Em 2005, Hara et al. mostrou que GAPDH inicia apoptose . Esta não é uma terceira função, mas pode ser vista como uma atividade mediada pela ligação de GAPDH ao DNA como na ativação da transcrição, discutida acima. O estudo demonstrou que o GAPDH é S-nitrosilado pelo NO em resposta ao estresse celular, o que faz com que ele se ligue à proteína SIAH1 , uma ubiquitina ligase . O complexo se move para o núcleo onde o Siah1 tem como alvo as proteínas nucleares para degradação , iniciando assim o desligamento controlado da célula. Em um estudo subsequente, o grupo demonstrou que o deprenil , que tem sido usado clinicamente para tratar a doença de Parkinson , reduz fortemente a ação apoptótica de GAPDH ao prevenir sua S-nitrosilação e pode, portanto, ser usado como medicamento.
Interruptor metabólico
GAPDH atua como um interruptor metabólico reversível sob estresse oxidativo. Quando as células são expostas a oxidantes , elas precisam de quantidades excessivas do cofator antioxidante NADPH . No citosol, o NADPH é reduzido a partir do NADP + por várias enzimas, três delas catalisam as primeiras etapas da via das pentoses fosfato . Os tratamentos com oxidantes causam uma inativação de GAPDH. Esta inativação redireciona temporariamente o fluxo metabólico da glicólise para a Via das Pentoses Fosfato, permitindo que a célula gere mais NADPH. Em condições de estresse, o NADPH é necessário para alguns sistemas antioxidantes, incluindo a glutaredoxina e a tioredoxina , além de ser essencial para a reciclagem da glutationa .
ER para transporte de Golgi
O GAPDH também parece estar envolvido no transporte de vesículas do retículo endoplasmático (RE) para o aparelho de Golgi, que faz parte da rota de transporte das proteínas secretadas. Verificou-se que GAPDH é recrutado por rab2 para os aglomerados vesiculotubulares do ER, onde ajuda a formar vesículas COP 1 . GAPDH é ativado via fosforilação de tirosina por Src .
Funções adicionais
GAPDH, como muitas outras enzimas, tem várias funções. Além de catalisar a 6ª etapa da glicólise , evidências recentes implicam o GAPDH em outros processos celulares. GAPDH foi descrito por exibir multifuncionalidade de ordem superior no contexto da manutenção da homeostase do ferro celular, especificamente como uma proteína chaperona para heme lábil dentro das células. Isso foi uma surpresa para os pesquisadores, mas faz sentido evolucionário reutilizar e adaptar as proteínas existentes, em vez de desenvolver uma nova proteína do zero.
Use como controle de carregamento
Como o gene GAPDH é frequentemente expresso de forma estável e constitutiva em níveis elevados na maioria dos tecidos e células, ele é considerado um gene doméstico . Por esse motivo, GAPDH é comumente usado por pesquisadores biológicos como um controle de carregamento para western blot e como um controle para qPCR . No entanto, os pesquisadores relataram regulação diferente de GAPDH sob condições específicas. Por exemplo, o fator de transcrição MZF-1 demonstrou regular o gene GAPDH. A hipóxia também regula positivamente o GAPDH. Portanto, o uso de GAPDH como controle de carregamento deve ser considerado com cuidado.
Distribuição celular
Todas as etapas da glicólise ocorrem no citosol, assim como a reação catalisada por GAPDH. Nos glóbulos vermelhos , o GAPDH e várias outras enzimas glicolíticas se agrupam em complexos no interior da membrana celular . O processo parece ser regulado por fosforilação e oxigenação. Espera-se que aproximar várias enzimas glicolíticas umas das outras aumente muito a velocidade geral de degradação da glicose. Estudos recentes também revelaram que o GAPDH é expresso de uma forma dependente de ferro no exterior da membrana celular a, onde desempenha um papel na manutenção da homeostase celular do ferro.
Significado clínico
Câncer
O GAPDH é superexpresso em vários cânceres humanos, como o melanoma cutâneo , e sua expressão está positivamente correlacionada com a progressão do tumor. Suas funções glicolíticas e antiapoptóticas contribuem para a proliferação e proteção das células tumorais, promovendo a tumorigênese . Notavelmente, o GAPDH protege contra o encurtamento do telômero induzido por drogas quimioterápicas que estimulam o esfingolipídeo ceramida . Enquanto isso, condições como o estresse oxidativo prejudicam a função de GAPDH, levando ao envelhecimento celular e à morte. Além disso, a depleção de GAPDH conseguiu induzir a senescência nas células tumorais, apresentando assim uma nova estratégia terapêutica para o controle do crescimento tumoral.
Neurodegeneração
GAPDH tem sido implicado em várias doenças e distúrbios neurodegenerativos, principalmente por meio de interações com outras proteínas específicas para essa doença ou distúrbio. Essas interações podem afetar não apenas o metabolismo energético, mas também outras funções GAPDH. Por exemplo, as interações de GAPDH com a proteína precursora de beta-amiloide (betaAPP) podem interferir em sua função em relação ao citoesqueleto ou transporte de membrana, enquanto as interações com huntingtina podem interferir em sua função em relação à apoptose, transporte de tRNA nuclear , replicação de DNA e reparo de DNA . Além disso, a translocação nuclear de GAPDH foi relatada na doença de Parkinson (DP), e vários medicamentos anti-apoptóticos para DP, como a rasagilina , funcionam prevenindo a translocação nuclear de GAPDH. É proposto que o hipometabolismo pode contribuir para a DP, mas os mecanismos exatos subjacentes ao envolvimento de GAPDH na doença neurodegenerativa ainda precisam ser esclarecidos. O SNP rs3741916 no 5 ' UTR do gene GAPDH pode estar associado ao início tardio da doença de Alzheimer .
Interações
Parceiros de ligação de proteína
GAPDH participa de uma série de funções biológicas por meio de suas interações proteína-proteína com:
- tubulina para facilitar o agrupamento de microtúbulos;
- actina para facilitar a polimerização da actina;
- VDAC1 para induzir a permeabilização da membrana mitocondrial (MMP) e apoptose;
- Receptor de inositol 1,4,5-trifosfato para regular a sinalização intracelular de Ca2 + ;
- Oct-1 para formar o complexo coativador OCA-S, que é necessário para a síntese de histona H2B durante a fase S do ciclo celular ;
- p22 para ajudar na organização dos microtúbulos ;
- Rab2 para facilitar o transporte do retículo endoplasmático (RE) - golgi ;
- Transferrina na superfície de diversas células e no fluido extracelular;
- Lactato desidrogenase ;
- Lactoferrina;
- Endonuclease apurínica / apirimidínica ( APE1 ), convertendo assim APE1 oxidado em sua forma reduzida, para reiniciar sua atividade endonuclease ;
- Proteína de leucemia promielocítica (PML) de um modo dependente de RNA ;
- Rheb para sequestrar a GTPase durante condições de baixa glicose;
- Siah1 para formar um complexo que se transloca para o núcleo, onde ubiquitina e degrada proteínas nucleares durante condições de estresse nitrosativo;
- O competidor de GAPDH da proteína Siah aumenta a vida (GOSPEL) para bloquear a interação de GAPDH com Siah1 e, assim, a morte celular em resposta ao estresse oxidativo;
- proteína de ligação p300 / CREB (CBP), que acetila GAPDH e, por sua vez, aumenta a acetilação de alvos apoptóticos adicionais;
- Ca2 + / proteína quinase dependente de calmodulina específica do músculo esquelético;
- Akt ;
- Proteína precursora de beta-amilóide (betaAPP);
- Huntingtin .
- GAPDH pode se autoassociar em oligômeros / agregados homotípicos
Parceiros de ligação de ácido nucleico
GAPDH se liga a RNA e DNA de fita simples e uma série de parceiros de ligação de ácido nucleico foram identificados:
- tRNA ,
- RNA viral da hepatite A ,
- RNA viral da hepatite B ,
- RNA viral da hepatite C ,
- HPIV3,
- mRNA de linfocina ,
- MRNA de IFN-γ ,
- MRNA de JEV , e
- DNA telomérico .
Inibidores
Mapa de caminho interativo
Clique nos genes, proteínas e metabólitos abaixo para acessar os respectivos artigos.
Referências
Leitura adicional
- Voet D, Voet JG (2010). Bioquímica . Nova York: Wiley. ISBN 978-0-470-57095-1.
- Stryer L, Berg JM, Tymoczko JL (2002). Biochemistry, Fifth Edition & Lecture Notebook . São Francisco: WH Freeman. ISBN 978-0-7167-9804-0.
- diagrama do mecanismo de reação GAPDH de Lodish MCB na estante NCBI
- diagrama semelhante da estante de livros Alberts The Cell at NCBI
links externos
- PDBe-KB fornece uma visão geral de todas as informações de estrutura disponíveis no PDB para Gliceraldeído-3-fosfato desidrogenase humano