Hexose - Hexose
Em química , uma hexose é um monossacarídeo (açúcar simples) com seis átomos de carbono. A fórmula química para todas as hexoses é C 6 H 12 O 6 e seu peso molecular é 180,156 g / mol.
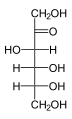
As hexoses existem em duas formas, de cadeia aberta ou cíclica, que se convertem facilmente uma na outra em soluções aquosas. A forma de cadeia aberta de uma hexose, que geralmente é favorecida em soluções, tem a estrutura geral H– (CHOH) n −1 –C (= O) - (CHOH) 4− n –H, onde n é 1, 2 , ou 3. Nomeadamente, cinco dos carbonos têm um grupo funcional hidroxilo (-OH) cada, ligado por uma ligação simples , e um tem um grupo oxo (= O), formando um grupo carbonilo (C = O). As ligações restantes dos átomos de carbono são satisfeitas por sete átomos de hidrogênio . Os carbonos são comumente numerados de 1 a 6, começando na extremidade mais próxima do carbonil.
Hexoses são extremamente importantes em bioquímica , tanto como moléculas isoladas (como glicose e frutose ) e como blocos de construção de outros compostos, como amido , celulose e glicosídeos . As hexoses podem formar dihexose (como a sacarose ) por uma reação de condensação que faz a ligação 1,6- glicosídica .
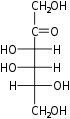
Quando a carbonila está na posição 1, formando um grupo formila (–CH = O), o açúcar é denominado aldohexose , um caso especial de aldose . Caso contrário, se a posição carbonila for 2 ou 3, o açúcar é um derivado de uma cetona e é chamado de cetohexose , um caso especial de cetose ; especificamente, uma n- cetohexose . No entanto, as 3-cetohexoses não foram observadas na natureza e são difíceis de sintetizar; portanto, o termo "cetohexose" geralmente significa 2-cetohexose.
Na forma linear, existem 16 aldohexoses e oito 2-cetohexoses, estereoisômeros que diferem na posição espacial dos grupos hidroxila. Essas espécies ocorrem em pares de isômeros ópticos . Cada par tem um nome convencional (como "glicose" ou "frutose"), e os dois membros são rotulados " D- " ou " L- ", dependendo se a hidroxila na posição 5, na projeção Fischer da molécula, está à direita ou à esquerda do eixo, respectivamente. Esses rótulos são independentes da atividade óptica dos isômeros. Em geral, apenas um dos dois enantiômeros ocorre naturalmente (por exemplo, D- glicose) e pode ser metabolizado por animais ou fermentado por leveduras .
O termo "hexose" às vezes é assumido como incluindo desoxihexoses , como fucose e ramnose : compostos com a fórmula geral C
6H
12O
6- y que pode ser descrito como derivado de hexoses pela substituição de um ou mais grupos hidroxila por átomos de hidrogênio.
Classificação
Aldohexoses
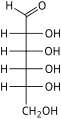
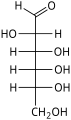
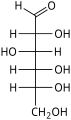
As aldohexoses são uma subclasse das hexoses que, na forma linear, possuem a carbonila no carbono 1, formando um derivado aldeído com estrutura H – C (= O) - (CHOH) 5 –H. O exemplo mais importante é a glicose .
Na forma linear, uma aldohexose tem quatro centros quirais , que dão 16 estereoisômeros de aldohexose possíveis (2 4 ), compreendendo 8 pares de enantiômeros . As formas lineares das oito D -aldohexoses, na projeção de Fischer , são
Destes D -isômeros, todos exceto D -altrose ocorrem em organismos vivos, mas apenas três são comuns: D- glicose, D- galactose e D- manose. Os isômeros L geralmente estão ausentes em organismos vivos; no entanto, a L -altrose foi isolada de cepas da bactéria Butyrivibrio fibrisolvens .
Diz-se que o químico Emil Fischer desenvolveu o seguinte dispositivo mnemônico para lembrar a ordem dada acima, que corresponde às configurações sobre os centros quirais quando ordenados como cadeias binárias de 3 bits:
- Todas as alt ruists gl Adly ma ke gu m i n gal lon ta NKS.
referindo-se a todos ose, altr ose, gl ucose, ma nnose, gu perder, eu doses, gal actose, ta perder.
Quando desenhadas nesta ordem, as projeções de Fischer das D -aldohexoses podem ser identificadas com os números binários de 3 dígitos de 0 a 7, a saber 000, 001, 010, 011, 100, 101, 110, 111. Os três bits , da esquerda para a direita, indique a posição das hidroxilas nos carbonos 4, 3 e 2, respectivamente: para a direita se o valor do bit for 0 e para a esquerda se o valor for 1.
Os diagramas de Fischer das oito L -aldohexoses são as imagens espelhadas dos isômeros D correspondentes ; com todos os hydoxyls revertidos, incluindo aquele no carbono 5.
Cetohexoses
Uma cetohexose é uma hexose contendo cetona. Biologicamente, o exemplo mais importante é a frutose .
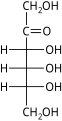
Na forma linear, as 2-cetohexoses possuem três centros quirais e, portanto, oito estereoisômeros possíveis (2 3 ), compreendendo quatro pares de enantiômeros. Os quatro isômeros D são:
As formas L correspondentes têm os hidroxilos nos carbonos 3, 4 e 5 invertidos. Abaixo estão uma representação dos oito isômeros em um estilo alternativo:
3-cetohexoses
Em teoria, as cetohexoses incluem também as 3-cetohexoses, que possuem a carbonila na posição 3; ou seja, H– (CHOH) 2 –C (= O) - (CHOH) 3 –H. No entanto, esses compostos não são conhecidos por ocorrer na natureza e são difíceis de sintetizar.
Em 1897, um produto não fermentável obtido por tratamento de frutose com bases , em particular hidróxido de chumbo (II) , recebeu o nome de glutose , um portmanteau de glicose e frutose , e foi considerado uma 3-cetohexose. No entanto, estudos posteriores mostraram que a substância era uma mistura de vários outros compostos.
A síntese unívoca e isolamento de um 3-cetohexose, xilo -3-hexulose , através de um percurso bastante complexo, foi relatada pela primeira vez em 1961 por G. Yuen e J. Sugihara .
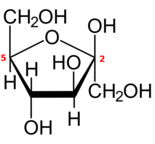
Formas cíclicas
Como a maioria dos monossacarídeos com cinco ou mais carbonos, cada aldohexose ou 2-cetohexose também existe em uma ou mais formas cíclicas (de cadeia fechada), derivadas da forma de cadeia aberta por um rearranjo interno entre o grupo carbonila e um dos grupos hidroxila .
A reação transforma o grupo = O em uma hidroxila, e a hidroxila em uma ponte de éter (–O–) entre os dois átomos de carbono, criando assim um anel com um átomo de oxigênio e quatro ou cinco carbonos.
Se o ciclo tem cinco átomos de carbono (seis átomos no total), a forma fechada é chamada de piranose , em homenagem ao éter cíclico tetra-hidropirano , que tem o mesmo anel. Se o ciclo tiver quatro átomos de carbono (cinco no total), a forma é chamada de furanose, em homenagem ao composto tetra-hidrofurano . A numeração convencional dos carbonos na forma fechada é a mesma que na forma de cadeia aberta.
Se o açúcar for uma aldohexose, com a carbonila na posição 1, a reação pode envolver a hidroxila no carbono 4 ou carbono 5, criando um hemiacetal com anel de cinco ou seis membros, respectivamente. Se o açúcar for uma 2-cetohexose, ele só pode envolver a hidroxila no carbono 5 e criará um hemicetal com um anel de cinco membros.
O fechamento transforma o carbono carboxílico em um centro quiral , que pode ter qualquer uma das duas configurações, dependendo da posição da nova hidroxila. Portanto, cada hexose na forma linear pode produzir duas formas fechadas distintas, identificadas pelos prefixos "α" e "β".
Sabe-se desde 1926 que as hexoses no estado sólido cristalino assumem a forma cíclica. As formas "α" e "β", que não são enantiômeros, geralmente cristalizam separadamente como espécies distintas. Por exemplo, a D- glicose forma um cristal α que tem rotação específica de + 112 ° e ponto de fusão de 146 ° C, bem como um cristal β que tem rotação específica de + 19 ° e ponto de fusão de 150 ° C.
A forma linear não cristaliza e existe apenas em pequenas quantidades em soluções aquosas, onde está em equilíbrio com as formas fechadas. No entanto, desempenha um papel essencial como estágio intermediário entre essas formas fechadas.
Em particular, as formas "α" e "β" podem ser convertidas uma na outra, retornando à forma de cadeia aberta e, em seguida, fechando na configuração oposta. Este processo é denominado mutarotação .
Propriedades quimicas
Embora todas as hexoses tenham estruturas semelhantes e compartilhem algumas propriedades gerais, cada par de enantiômero tem sua própria química. A frutose é solúvel em água, álcool e éter. Os dois enantiômeros de cada par geralmente têm propriedades biológicas muito diferentes.
2-cetohexoses são estáveis ao longo de uma gama larga de pH, e com um p primário K um de 10,28, só desprotonar a um pH elevado, de modo que são ligeiramente menos estáveis que aldohexoses em solução.
Ocorrência natural e usos
A aldohexose mais importante na bioquímica é a D - glicose , que é o principal "combustível" para o metabolismo de muitos organismos vivos.
As 2-cetohexoses psicose , frutose e tagatose ocorrem naturalmente como os isômeros D , enquanto a sorbose ocorre naturalmente como o isômero L.
D- Sorbose é comumente usada na síntese comercial de ácido ascórbico. D- Tagatose é uma rara cetohexose natural encontrada em pequenas quantidades nos alimentos. D - A frutose é responsável pelo sabor doce de muitas frutas e é um alicerce da sacarose , o açúcar comum.
Desoxihexoses
O termo "hexose" pode às vezes ser usado para incluir as desoxialdohexoses, que têm um ou mais hidroxilas (-OH) substituídos por átomos de hidrogênio (-H). É chamada de hexose-mãe, com o prefixo " x- desoxi-", o x indicando o carbono com a hidroxila afetada. Alguns exemplos de interesse biológico são
- L- Fucose(6-desoxi- L -galactose)
- L- Ramnose(6-desoxi- L- manose)
- D- quinovose(6-desoxi- D- glicose), encontrada como parte dosulfolipídeo sulfoquinovosil diacilglicerol(SQDG)
- L- Pneumose(6-desoxi- L -talose)
Veja também
Referências
links externos
-
 Mídia relacionada a Aldohexoses no Wikimedia Commons
Mídia relacionada a Aldohexoses no Wikimedia Commons -
 Mídia relacionada a cetohexoses no Wikimedia Commons
Mídia relacionada a cetohexoses no Wikimedia Commons