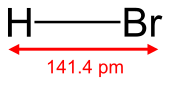
Brometo de hidrogênio - Hydrogen bromide
|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Brometo de hidrogênio |
|||
|
Nome IUPAC sistemático
Bromane |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 3587158 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100.030.090 |
||
| Número EC | |||
| KEGG | |||
| Malha | Hidrobromo + Ácido | ||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 1048 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| HBr | |||
| Massa molar | 80,91 g / mol | ||
| Aparência | Gás incolor | ||
| Odor | Acre | ||
| Densidade | 3,307 g / mL (25 ° C) | ||
| Ponto de fusão | −86,9 ° C (−124,4 ° F; 186,2 K) | ||
| Ponto de ebulição | −66,8 ° C (−88,2 ° F; 206,3 K) | ||
| 221 g / 100 mL (0 ° C) 204 g / 100 mL (15 ° C) 193 g / 100 mL (20 ° C) 130 g / 100 mL (100 ° C) |
|||
| Solubilidade | Solúvel em álcool , solventes orgânicos | ||
| Pressão de vapor | 2,308 MPa (a 21 ° C) | ||
| Acidez (p K a ) | −8,8 (± 0,8); ~ −9 | ||
| Basicidade (p K b ) | ~ 23 | ||
| Ácido conjugado | Bromonium | ||
| Base conjugada | Brometo | ||
|
Índice de refração ( n D )
|
1,325 | ||
| Estrutura | |||
| Linear | |||
| 820 mD | |||
| Termoquímica | |||
|
Capacidade de calor ( C )
|
350,7 mJ / (K · g) | ||
|
Entropia molar padrão ( S |
198,696–198,704 J / (K · mol) | ||
| −36,45 ...− 36,13 kJ / mol | |||
| Perigos | |||
| Ficha de dados de segurança |
Hazard.com |
||
| Pictogramas GHS |
 
|
||
| Palavra-sinal GHS | Perigo | ||
| H314 , H335 | |||
| P261 , P280 , P305 + 351 + 338 , P310 | |||
| NFPA 704 (diamante de fogo) | |||
| Dose ou concentração letal (LD, LC): | |||
|
LC 50 ( concentração média )
|
2858 ppm (rato, 1 h ) 814 ppm (camundongo, 1 h) |
||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
TWA 3 ppm (10 mg / m 3 ) | ||
|
REL (recomendado)
|
TWA 3 ppm (10 mg / m 3 ) | ||
|
IDLH (perigo imediato)
|
30 ppm | ||
| Compostos relacionados | |||
|
Compostos relacionados
|
Fluoreto de hidrogênio Cloreto de hidrogênio Iodeto de hidrogênio Hidrogênio astatida |
||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
O brometo de hidrogênio é o composto inorgânico com a fórmula HBr. É um halogeneto de hidrogênio que consiste em hidrogênio e bromo. Um gás incolor, que se dissolve em água, formando ácido bromídrico , que é saturado com 68,85% de HBr em peso à temperatura ambiente. Soluções aquosas com 47,6% de HBr em massa formam uma mistura azeotrópica de ebulição constante que ferve a 124,3 ° C. A fervura de soluções menos concentradas libera H 2 O até que a composição da mistura em ebulição constante seja alcançada.
O brometo de hidrogênio e sua solução aquosa são reagentes comumente usados na preparação de compostos de brometo.
Reações
Química orgânica
O brometo de hidrogênio e o ácido bromídrico são reagentes importantes na produção de compostos organobromáticos . Em uma reação de radical livre , o HBr adiciona aos alquenos:
- RCH = CH 2 + HBr → R − CHBr − CH 3
Os brometos de alquila resultantes são agentes alquilantes úteis , por exemplo, como precursores de derivados de aminas graxas. Adições de radicais livres relacionadas a cloreto de alila e estireno dão 1-bromo-3-cloropropano e feniletilbrometo , respectivamente.
O brometo de hidrogênio reage com diclorometano para dar bromoclorometano e dibromometano , sequencialmente:
- HBr + CH 2 Cl 2 → HCl + CH 2 BrCl
- HBr + CH 2 BrCl → HCl + CH 2 Br 2
Essas reações de metátese ilustram o consumo do ácido mais forte (HBr) e a liberação do ácido mais fraco (HCl).
O brometo de alila é preparado pelo tratamento de álcool alílico com HBr:
- CH 2 = CHCH 2 OH + HBr → CH 2 = CHCH 2 Br + H 2 O
HBr é adicionado a alcinos para produzir bromoalcenos. A estereoquímica desse tipo de adição é geralmente anti :
- RC≡CH + HBr → RC (Br) = CH 2
Além disso, o HBr adiciona epóxidos e lactonas , resultando na abertura do anel.
Com a trifenilfosfina , o HBr dá brometo de trifenilfosfônio , uma "fonte" sólida de HBr.
- P (C 6 H 5 ) 3 + HBr → [HP (C 6 H 5 ) 3 ] + Br -
Química Inorgânica
Brometo de vanádio (III) e brometo de molibdênio (IV) foram preparados por tratamento dos cloretos superiores com HBr. Essas reações ocorrem por meio de reações redox:
- 2 VCl 4 + 8 HBr → 2 VBr 3 + 8 HCl + Br 2
Preparação industrial
O brometo de hidrogênio (junto com o ácido bromídrico) é produzido pela combinação de hidrogênio e bromo a temperaturas entre 200 e 400 ° C. A reação é normalmente catalisada por platina ou amianto .
Síntese de Laboratório
O HBr pode ser preparado por destilação de uma solução de brometo de sódio ou brometo de potássio com ácido fosfórico ou ácido sulfúrico :
- KBr + H 2 SO 4 → KHSO 4 + HBr
O ácido sulfúrico concentrado é menos eficaz porque oxida o HBr a bromo :
- 2 HBr + H 2 SO 4 → Br 2 + SO 2 + 2 H 2 O
O ácido pode ser preparado por:
- reação de bromo com água e enxofre :
- 2 Br 2 + S + 2 H 2 O → 4 HBr + SO 2
- bromação de tetralina :
- C 10 H 12 + 4 Br 2 → C 10 H 8 Br 4 + 4 HBr
- redução de bromo com ácido fosforoso:
- Br 2 + H 3 PO 3 + H 2 O → H 3 PO 4 + 2 HBr
O brometo de hidrogênio anidro também pode ser produzido em pequena escala por termólise de brometo de trifenilfosfônio em xileno em refluxo .
O brometo de hidrogênio preparado pelos métodos acima pode ser contaminado com Br 2 , que pode ser removido passando o gás através de uma solução de fenol à temperatura ambiente em tetraclorometano ou outro solvente adequado (produzindo 2,4,6-tribromofenol e gerando mais HBr em processo) ou através de aparas de cobre ou gaze de cobre em alta temperatura.
Segurança
O HBr é altamente corrosivo e irritante para inalação.
Referências
- ^ "Ácido bromídrico - Resumo do composto" . Composto PubChem . EUA: National Center for Biotechnology Information. 16 de setembro de 2004. Identificação e registros relacionados . Página visitada em 10 de novembro de 2011 .
- ^ Lide, David R., ed. (2006). CRC Handbook of Chemistry and Physics (87ª ed.). Boca Raton, FL: CRC Press . ISBN 0-8493-0487-3.
- ^ Trummal, Aleksander; Lipping, Lauri; Kaljurand, Ivari; Koppel, Ilmar A; Leito, Ivo (2016). "Acidez de Ácidos Fortes em Água e Dimetil Sulfóxido". O Journal of Physical Chemistry Uma . 120 (20): 3663–9. Bibcode : 2016JPCA..120.3663T . doi : 10.1021 / acs.jpca.6b02253 . PMID 27115918 .
- ^ Perrin, DD Constantes de dissociação de ácidos inorgânicos e bases em solução aquosa. Butterworths, Londres, 1969.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed . Houghton Mifflin Company. ISBN 978-0-618-94690-7.
- ^ a b c Guia de bolso de NIOSH aos perigos químicos. "# 0331" . Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH).
- ^ "Brometo de hidrogênio" . Concentrações imediatamente perigosas para a vida ou para a saúde (IDLH) . Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH).
- ^ Dagani, MJ; Barda, HJ; Benya, TJ; Sanders, DC "Bromine Compounds". Enciclopédia de Química Industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a04_405 .CS1 maint: vários nomes: lista de autores ( link )
- ^ a b c Greenwood, NN; Earnshaw, A. Chemistry of the Elements; Butterworth-Heineman: Oxford, Grã-Bretanha; 1997; pp. 809–812.
- ^ Vollhardt, KPC; Schore, NE Organic Chemistry: Structure and Function; 4ª Ed .; WH Freeman and Company: New York, NY; 2003
- ^ a b Hercouet, A .; LeCorre, M. (1988) Trifenilfosfônio brometo: Uma fonte conveniente e quantitativa de brometo de hidrogênio gasoso. Synthesis, 157-158.
- ^ Calderazzo, Fausto; Maichle-Mössmer, Cäcilie; Pampaloni, Guido; Strähle, Joachim (1993). "Low-Temperature Syntheses of Vanadium (III) and Molybdenum (IV) Bromides by Halide Exchange". J. Chem. Soc., Dalton Trans. (5): 655–658. doi : 10.1039 / DT9930000655 .
- ^ a b Ruhoff, JR; Burnett, RE; Reid, EE "Hydrogen Bromide (Anhydrous)" Organic Syntheses, Vol. 15, pág. 35 (Coll. Vol. 2, p. 338).
- ^ a b c M. Schmeisser "Cloro, Bromo, Iodo" em Handbook of Preparative Inorganic Chemistry, 2a Ed. Editado por G. Brauer, Academic Press, 1963, NY. Vol. 1. p. 282.


