Hipobromito - Hypobromite
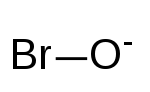
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
hipobromito
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| 1040 | |
|
PubChem CID
|
|
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| BrO - | |
| Massa molar | 95,904 g / mol |
| Ácido conjugado | Ácido hipobromoso |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O íon hipobromito , também chamado de água alcalina de bromo , é BrO - . O bromo está no estado de oxidação +1 . O hipobromito é o composto de bromo análogo aos hipocloritos encontrados em alvejantes comuns e em células do sistema imunológico. De muitas maneiras, o hipobromito funciona da mesma maneira que o hipoclorito e também é usado como germicida e antiparasitário em aplicações industriais e no sistema imunológico.
Preparação
Os sais de hipobromito são formados no tratamento do bromo com bases aquosas, tais como hidróxido de sódio ou potássio. A 20 ° C a reação é rápida.
- Br 2 + 2 OH - (aq) → Br - + BrO - + H 2 O
Nesta reação, o bromo é desproporcional (alguns sofrem redução e alguns oxidação) do estado de oxidação 0 (Br 2 ) para o estado de oxidação -1 (Br - ) e estado de oxidação +1 (BrO - ). O hipobromito de sódio pode ser isolado como um sólido laranja.
Uma reação secundária, onde o hipobromito espontaneamente se desproporciona em brometo (estado de oxidação do bromo -1) e bromato (estado de oxidação do bromo +5) ocorre rapidamente a 20 ° C e lentamente a 0 ° C.
- 3 BrO - → 2 Br - + BrO -
3
Portanto, na reação 2, a formação e as proporções dos produtos do estado de oxidação do bromo -1, +1 e +5 podem ser controladas pela temperatura. O hipobromito não é termodinamicamente estável em qualquer pH (consulte o diagrama de Pourbaix para o bromo em http://www.eosremediation.com/download/Chemistry/Chemical%20Properties/Eh_pH_Diagrams.pdf ), mas é cineticamente bloqueado em direção a uma desproporção adicional em bromato brometo acima do pKa de HBrO.
Essas reações do bromo são análogas às do cloro formando hipoclorito e clorato . A reação 1 de cloro correspondente (para formar ClO - ) é rápida a 20 ° C e a reação 2 (para formar ClO -
3 ) é lento a 20 ° C e rápido a 70 ° C.
Compostos
Um hipobromito é um composto que contém esse ânion. Os exemplos incluem hipobromito de sódio e hipobromito de potássio.
Na natureza e na indústria
O brometo da dieta, naturalmente presente no sangue, é utilizado pelos eosinófilos , leucócitos da classe dos granulócitos, especializados no tratamento de parasitas multicelulares. Essas células reagem o brometo com o peróxido para gerar hipobromito pela ação da eosinófila peroxidase , uma enzima haloperoxidase que usa preferencialmente brometo em vez de cloreto para esse fim.
Sais de brometo simples (como o brometo de sódio) às vezes também são usados em banheiras de hidromassagem e spas como agentes germicidas leves, usando a ação de um agente oxidante adicionado (como o peróxido de hidrogênio) para gerar hipobromito in situ , de maneira semelhante à ação de peroxidase em brometo em eosinófilos.
Hipobromito foi proposto para ser um intermediário reativo no rearranjo de Hofmann .
Veja também
Outros ânions de bromo:
| Estado de oxidação do bromo | -1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Nome | brometo | hipobromito | bromite | bromato | perbromato |
| Fórmula | Br - | BrO - |
Mano - 2 |
Mano - 3 |
Mano - 4 |
| Estrutura |

|
|
|
|

|
