Ácido hipofluoroso - Hypofluorous acid
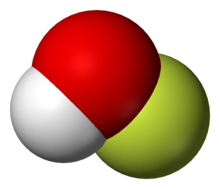
 Estrutura da fase gasosa
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Ácido hipofluoroso
|
|
| Outros nomes
Hidrogênio hipofluorito
Hidrogênio fluorato (-I) Fluórico (-I) ácido Hidrogênio monofluoroxigenado (0) fluoreto de hidroxila |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| HOF | |
| Massa molar | 36,0057 g mol −1 |
| Aparência | líquido amarelo claro acima de −117 ° C sólido branco abaixo de −117 ° C |
| Ponto de fusão | −117 ° C (−179 ° F; 156 K) |
| Ponto de ebulição |
decompõe-se a 0 ° C |
| Estrutura | |
| C s | |
| Perigos | |
| Riscos principais | oxidante forte, corrosivo |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Outros cátions
|
hipofluorito de lítio |
|
Compostos relacionados
|
ácido hipocloroso nitroxil hidrogênio cianeto formaldeído |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O ácido hipofluoro , fórmula química H O F , é o único oxiácido conhecido do flúor e o único oxoácido conhecido no qual o átomo principal ganha elétrons do oxigênio para criar um estado de oxidação negativo. O estado de oxidação do oxigênio em hipofluoritos é 0. Ele também é o único ácido hipohaloso que pode ser isolado como um sólido . HOF é um intermediário na oxidação da água pelo flúor , que produz fluoreto de hidrogênio , difluoreto de oxigênio , peróxido de hidrogênio , ozônio e oxigênio . HOF é explosivo em temperatura ambiente, formando HF e O 2 :
- 2 HOF → 2 HF + O 2
Foi isolado na forma pura passando o gás F 2 sobre o gelo a −40 ° C, recolhendo o gás HOF e condensando-o:
- F 2 + H 2 O → HOF + HF
O composto foi caracterizado na fase sólida por cristalografia de raios-X como uma molécula curvada com um ângulo de 101 °. Os comprimentos de ligação O – F e O – H são 144,2 e 96,4 picômetros , respectivamente. A estrutura sólida consiste em cadeias com ligações O – H ··· O. A estrutura também foi analisada na fase gasosa, um estado em que o ângulo de ligação H – O – F é ligeiramente mais estreito (97,2 °).
O ácido hipofluoro em acetonitrila (gerado in situ pela passagem de flúor gasoso através da acetonitrila "úmida" ) é comumente conhecido como reagente de Rozen .
Hipofluoritos
Os hipofluoritos são formalmente derivados de OF - , que é a base conjugada do ácido hipofluoroso. Um exemplo é o hipofluorito trifluorometil (CF 3 OF).
Veja também
- Ácido hipocloroso , um composto relacionado que é mais importante tecnologicamente, mas não foi obtido na forma pura.

