Ácido hipofosfórico - Hypophosphoric acid
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Ácido hipodifosfórico
|
|
| Outros nomes
Ácido difosfórico
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| H 4 P 2 O 6 | |
| Massa molar | 161,98 g / mol |
| Aparência | Sólido branco (di-hidratado) |
| Ponto de fusão | 54 ° C (129 ° F; 327 K) |
| Base conjugada | Hipofosfato |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
| Referências da Infobox | |
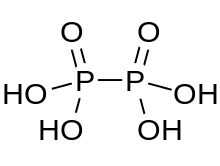
O ácido hipofosfórico é um ácido mineral com a fórmula H 4 P 2 O 6 , com fósforo em um estado de oxidação formal de +4. No estado sólido, está presente como o di-hidrato, H 4 P 2 O 6 · 2H 2 O. No ácido hipofosfórico, os átomos de fósforo são idênticos e unidos diretamente por uma ligação P − P. Ácido Isohypophosphoric é um isómero estrutural de ácido hipofosfórico em que um fósforo tem um hidrogénio directedly ligado a ele e que átomo de fósforo está ligado ao outro por uma ponte de oxigénio para dar um ácido fosforoso / ácido fosfórico misto de anidrido . Os dois átomos de fósforo estão nos estados de oxidação +3 e +5, respectivamente.
Preparação e reações
O ácido hipofosfórico pode ser preparado pela reação do fósforo vermelho com o clorito de sódio à temperatura ambiente.
- 2 P + 2 NaClO 2 + 2 H 2 O → Na 2 H 2 P 2 O 6 + 2 HCl
Uma mistura de ácido hipofosfórico, ácido fosfórico (H 3 PO 3 ) e ácido fosfórico (H 3 PO 4 ) é produzida quando o fósforo branco oxida no ar quando parcialmente imerso em água.
O sal tetrassódico Na 4 P 2 O 6 · 10H 2 O cristaliza a pH 10 e o sal dissódico, Na 2 H 2 PO 6 · 6H 2 O a pH 5,2. O sal dissódico pode ser passado através de uma coluna de troca iônica para formar o di-hidrato ácido, H 4 P 2 O 6 · 2H 2 O.
O ácido anidro pode ser formado por desidratação a vácuo sobre P 4 O 10 ou pela reação de H 2 S em hipofosfato de chumbo, Pb 2 P 2 O 6 .
O ácido hipofosfórico é tetraprótico com constantes de dissociação p K a1 = 2,2, p K a2 = 2,8, p K a3 = 7,3 ep K a4 = 10,0.
Em repouso, o ácido anidro sofre rearranjo e desproporcionamento para formar uma mistura de ácido iso-hipofosfórico, HPO (OH) -O-PO 2 (OH); ácido pirofosfórico H 2 P 2 O 7 e ácido pirofosforoso.
O ácido hipofosfórico é instável em ácido clorídrico quente , em HCl 4 M ele hidrolisa para dar H 3 PO 3 + H 3 PO 4 .
Estrutura
O ácido hipofosforado contém íons oxônio e é melhor formulado [H 3 O + ] 2 [H 2 P 2 O 6 ] 2− . O ácido é isoestrutural com o sal de diamônio que contém o ânion [HOPO 2 PO 2 OH] 2− com um comprimento de ligação P − P de 219 pm.
O ânion HOPO 2 PO 2 OH 2− em Na 2 H 2 P 2 O 6 · 6H 2 O tem uma estrutura simétrica e escalonada do tipo etano com uma ligação P − P de comprimento 219 pm. Cada átomo de fósforo tem duas ligações P-O com comprimento de 151 pm e um comprimento de ligação P-OH de 159 pm.
Sais de hipofosfato
Muitos sais de hipofosfato são conhecidos, por exemplo, K 4 P 2 O 6 · 8H 2 O, Ca 2 P 2 O 6 · 2H 2 O, K 3 HP 2 O 6 · 3H 2 O, K 2 H 2 P 2 O 6 · 2H 2 O, KH 3 P 2 O 6 .
Ao permanecer no ar, os hipofosfatos tendem a se oxidar em pirofosfatos contendo o P
2O4−
7íon onde P tem um estado de oxidação formal de +5. Os hipofosfatos são estáveis aos hidróxidos alcalinos. No hidróxido de sódio fundido , eles se convertem rapidamente no ortofosfato contendo PO3−
4.
Polihipofosfatos
Os poli-hipofosfatos são conhecidos contendo ânions lineares, por exemplo Na 5 P 3 O 8 contendo O (PO
2) 3 O 5− com uma cadeia P − P − P e Na 6 P 4 O 10 · 2H 2 O contendo O (PO
2) 4 O 6− , com uma cadeia P − P − P − P. O ânion cíclico (PO
2)6−
6, (hipohexametafosfato) em que cada átomo de fósforo tem um estado de oxidação de +3 é formado quando uma suspensão de fósforo vermelho em KOH é oxidada com bromo.
Veja também
- Ácido ditionico , o equivalente de enxofre.
