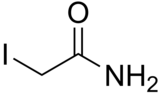
Iodoacetamida - Iodoacetamide
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
2-Iodoacetamida |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100,005,119 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 2 H 4 I N O | |
| Massa molar | 184,964 g · mol −1 |
| Aparência | cristais brancos (coloração amarela indica a presença de iodo) |
| Ponto de fusão | 94 ° C (201 ° F; 367 K) |
| Perigos | |
| Ficha de dados de segurança | MSDS 1 , MSDS 2 |
| NFPA 704 (diamante de fogo) | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
2-Iodoacetamida é um agente alquilante usado para fins de mapeamento de peptídeos . Suas ações são semelhantes às do iodoacetato . É comumente usado para se ligar covalentemente ao grupo tiol da cisteína, de modo que a proteína não pode formar ligações dissulfeto . Também usado em estudos de ubiquitina como um inibidor das enzimas deubiquitinase (DUBs) porque alquila os resíduos de cisteína no sítio ativo de DUB.
Inibidor de peptidase
A iodoacetamida é um inibidor irreversível de todas as cisteína peptidases, com o mecanismo de inibição ocorrendo a partir da alquilação do resíduo de cisteína catalítica (ver esquema). Em comparação com seu derivado ácido, o iodoacetato, a iodoacetamida reage substancialmente mais rápido. Esta observação parece contraditória com a reatividade química padrão, no entanto, a presença de uma interação favorável entre o íon imidazólio positivo da histidina catalítica e o grupo carboxila carregado negativamente do iodoacetato é a razão para o aumento da atividade relativa da iodoacetamida.
Espectrometria de massa de proteína
É comumente usado durante a preparação da amostra para sequenciamento de novo (peptídeo) com espectrometria de massa de proteína , mas críticos recentes sugerem evitar o uso dele


