Proteína ferro-enxofre - Iron–sulfur protein
Proteínas ferro-enxofre (ou proteínas ferro-enxofre na grafia britânica ) são proteínas caracterizadas pela presença de aglomerados de ferro-enxofre contendo centros di-, tri- e tetra -ferro ligados por sulfeto em estados de oxidação variáveis . Aglomerados de ferro-enxofre são encontrados em uma variedade de metaloproteínas , como as ferredoxinas , bem como NADH desidrogenase , hidrogenases , coenzima Q - citocromo c redutase , succinato - coenzima Q redutase e nitrogenase. Os aglomerados de ferro-enxofre são mais conhecidos por seu papel nas reações de oxidação-redução do transporte de elétrons em mitocôndrias e cloroplastos . Tanto o Complexo I quanto o Complexo II de fosforilação oxidativa possuem múltiplos aglomerados de Fe-S. Eles têm muitas outras funções, incluindo catálise, conforme ilustrado pela aconitase , geração de radicais conforme ilustrado por enzimas dependentes de SAM e como doadores de enxofre na biossíntese de ácido lipóico e biotina . Além disso, algumas proteínas Fe-S regulam a expressão gênica. As proteínas Fe – S são vulneráveis ao ataque do óxido nítrico biogênico , formando complexos dinitrosil de ferro . Na maioria das proteínas Fe – S, os ligantes terminais do Fe são tiolato , mas existem exceções.
A prevalência dessas proteínas nas vias metabólicas da maioria dos organismos leva alguns cientistas a teorizar que os compostos ferro-enxofre tiveram um papel significativo na origem da vida na teoria mundial ferro-enxofre .
Motivos estruturais
Em quase todas as proteínas Fe-S, os centros de Fe são tetraédricos e os ligantes terminais são centros de enxofre tiolato de resíduos de cisteína. Os grupos de sulfeto são dois ou três coordenados. Três tipos distintos de aglomerados de Fe – S com essas características são os mais comuns.
Clusters 2Fe-2S
O sistema polimetálicos mais simples, o [Fe 2 S 2 ] aglomerado, é constituído por dois iões de ferro em ponte através de dois iões sulfureto e coordenados por quatro cisteinilo ligandos (em Fe 2 S 2 ferredoxinas ) ou por duas cisteínas e duas histidinas (em proteínas de Rieske ) As proteínas oxidadas contêm dois íons Fe 3+ , enquanto as proteínas reduzidas contêm um íon Fe 3+ e um Fe 2+ . Essas espécies existem em dois estados de oxidação, (Fe III ) 2 e Fe III Fe II . O domínio de enxofre de ferro CDGSH também está associado a aglomerados 2Fe-2S.
Clusters 4Fe-4S
Um motivo comum apresenta quatro íons de ferro e quatro íons de sulfeto colocados nos vértices de um aglomerado do tipo cubano . Os centros de Fe são normalmente ainda coordenados por ligantes de cisteinila. As proteínas de transferência de elétrons [Fe 4 S 4 ] ([Fe 4 S 4 ] ferredoxinas ) podem ser subdivididas em ferredoxinas de baixo potencial (tipo bacteriano) e alto potencial (HiPIP) . As ferredoxinas de baixo e alto potencial estão relacionadas pelo seguinte esquema redox:
No HiPIP, o cluster se desloca entre [2Fe 3+ , 2Fe 2+ ] (Fe 4 S 4 2+ ) e [3Fe 3+ , Fe 2+ ] (Fe 4 S 4 3+ ). Os potenciais para este par redox variam de 0,4 a 0,1 V. Nas ferredoxinas bacterianas, o par de estados de oxidação são [Fe 3+ , 3Fe 2+ ] (Fe 4 S 4 + ) e [2Fe 3+ , 2Fe 2+ ] (Fe 4 S 4 2+ ). Os potenciais para este par redox variam de -0,3 a -0,7 V. As duas famílias de aglomerados 4Fe-4S compartilham o estado de oxidação Fe 4 S 4 2+ . A diferença nos pares redox é atribuída ao grau de ligação de hidrogênio, que modifica fortemente a basicidade dos ligantes tiolato de cisteína. Outro par redox, que é ainda mais redutor do que as ferredoxinas bacterianas, está implicado na nitrogenase .
Alguns aglomerados 4Fe-4S ligam substratos e, portanto, são classificados como cofatores enzimáticos. Na aconitase , o cluster Fe – S liga o aconitato no centro de Fe que não possui um ligante tiolato. O cluster não sofre redox, mas serve como um catalisador de ácido de Lewis para converter citrato em isocitrato . Em enzimas SAM radicais , o cluster se liga e reduz a S-adenosilmetionina para gerar um radical, que está envolvido em muitas biossínteses.
Clusters 3Fe-4S
As proteínas também são conhecidas por conter centros [Fe 3 S 4 ], que apresentam um ferro a menos do que os núcleos mais comuns [Fe 4 S 4 ]. Três íons de sulfeto ligam dois íons de ferro cada, enquanto o quarto sulfeto faz a ponte de três íons de ferro. Seus estados de oxidação formal podem variar de [Fe 3 S 4 ] + (forma totalmente Fe 3+ ) a [Fe 3 S 4 ] 2− (forma totalmente Fe 2+ ). Em uma série de proteínas ferro-enxofre, o cluster [Fe 4 S 4 ] pode ser reversivelmente convertido por oxidação e perda de um íon de ferro em um cluster [Fe 3 S 4 ]. Por exemplo, a forma inativa da aconitase possui um [Fe 3 S 4 ] e é ativada pela adição de Fe 2+ e redutor.
Outros clusters Fe – S
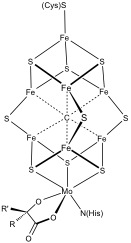
Sistemas polimetálicos mais complexos são comuns. Os exemplos incluem os agrupamentos 8Fe e 7Fe na nitrogenase . A monóxido de carbono desidrogenase e a [FeFe] - hidrogenase também apresentam aglomerados incomuns de Fe-S. Um agrupamento especial coordenado por 6 cisteína [Fe 4 S 3 ] foi encontrado em hidrogenases [NiFe] ligadas à membrana tolerantes ao oxigênio.
Biossíntese
A biossíntese dos aglomerados Fe-S foi bem estudada. A biogênese de aglomerados de ferro e enxofre foi estudada mais extensivamente nas bactérias E. coli e A. vinelandii e na levedura S. cerevisiae . Pelo menos três sistemas biossintéticos diferentes foram identificados até agora, a saber, sistemas nif, suf e isc, que foram identificados pela primeira vez em bactérias. O sistema nif é responsável pelos clusters na enzima nitrogenase. Os sistemas suf e isc são mais gerais.
O sistema isc de levedura é o mais bem descrito. Várias proteínas constituem a maquinaria biossintética por meio da via isc. O processo ocorre em duas etapas principais: (1) o cluster Fe / S é montado em uma proteína-esqueleto seguido por (2) transferência do cluster pré-formado para as proteínas receptoras. A primeira etapa desse processo ocorre no citoplasma de organismos procarióticos ou na mitocôndria de organismos eucarióticos . Nos organismos superiores, os aglomerados são, portanto, transportados para fora da mitocôndria para serem incorporados às enzimas extramitocondriais. Esses organismos também possuem um conjunto de proteínas envolvidas nos processos de transporte e incorporação de aglomerados de Fe / S que não são homólogas às proteínas encontradas em sistemas procarióticos.
Análogos sintéticos
Análogos sintéticos dos aglomerados de Fe-S de ocorrência natural foram relatados pela primeira vez por Holm e colaboradores. O tratamento de sais de ferro com uma mistura de tiolatos e sulfeto fornece derivados como ( Et 4 N ) 2 Fe 4 S 4 (SCH 2 Ph) 4 ].
Veja também
Referências
Leitura adicional
- Beinert, H. (2000). “Proteínas ferro-enxofre: estruturas antigas, ainda cheias de surpresas”. J. Biol. Inorg. Chem . 5 (1): 2–15. doi : 10.1007 / s007750050002 . PMID 10766431 . S2CID 20714007 .
- Beinert, H .; Kiley, PJ (1999). "Proteínas Fe-S em funções sensoriais e regulatórias". Curr. Opin. Chem. Biol . 3 (2): 152–157. doi : 10.1016 / S1367-5931 (99) 80027-1 . PMID 10226040 .
- Johnson, MK (1998). "Proteínas ferro-enxofre: novos papéis para clusters antigos". Curr. Opiniões Chem. Biol . 2 (2): 173–181. doi : 10.1016 / S1367-5931 (98) 80058-6 . PMID 9667933 .
- Comitê de Nomenclatura da União Internacional de Bioquímica (NC-IUB) (1979). "Nomenclatura de proteínas de enxofre de ferro. Recomendações 1978" . EUR. J. Biochem . 93 (3): 427–430. doi : 10.1111 / j.1432-1033.1979.tb12839.x . PMID 421685 .
- Noodleman, L., Lovell, T., Liu, T., Himo, F. e Torres, RA (2002). "Insights sobre propriedades e energia das proteínas ferro-enxofre de clusters simples para nitrogenase". Curr. Opiniões Chem. Biol . 6 (2): 259–273. doi : 10.1016 / S1367-5931 (02) 00309-5 . PMID 12039013 .CS1 maint: vários nomes: lista de autores ( link )
- Spiro, TG, Ed. (1982). Proteínas ferro-enxofre . Nova York: Wiley. ISBN 0-471-07738-0.CS1 maint: vários nomes: lista de autores ( link )
links externos
- Ferro-Enxofre + Proteínas na Biblioteca Nacional de Medicina dos EUA. Cabeçalhos de Assuntos Médicos (MeSH)
- Exemplos de aglomerados de ferro-enxofre


