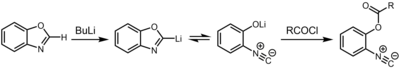Isocianeto - Isocyanide
Um isocianeto (também chamado de isonitrila ou carbilamina ) é um composto orgânico com o grupo funcional -N≡C. É o isômero do nitrila relacionado (-C≡N), portanto, o prefixo é isociano . O fragmento orgânico está conectado ao grupo isocianeto através do átomo de nitrogênio , não através do carbono . Eles são usados como blocos de construção para a síntese de outros compostos.
Propriedades
Estrutura e ligação
A distância CN em isocianetos é 115,8 pm em isocianeto de metila . Os ângulos do CNC estão próximos de 180 °.
Semelhante ao monóxido de carbono , os isocianetos são descritos por duas estruturas de ressonância , uma com uma ligação tripla entre o nitrogênio e o carbono e outra com uma ligação dupla entre eles. O par solitário π do nitrogênio estabiliza a estrutura e é responsável pela linearidade dos isocianetos, embora a reatividade dos isocianetos reflita algum caráter carbeno, pelo menos em um sentido formal. Assim, ambas as estruturas de ressonância são representações úteis. Eles são suscetíveis à polimerização .
Espectroscopia
Os isocianetos exibem uma forte absorção em seus espectros de IV na faixa de 2165–2110 cm −1 .
A simetria eletrônica sobre o núcleo do isocianeto 14 N resulta em um relaxamento quadrupolar lento de forma que o acoplamento do spin nuclear do 13 C- 14 N pode ser observado, com constantes de acoplamento de ca. 5 Hz para o núcleo 13 C do isocianeto e 5–14 Hz para o núcleo 13 C ao qual o grupo isocianeto está ligado.
Odor
Seu odor desagradável é lendário. Para citar Lieke, " Es besitzt einen penetranten, höchst unangenehmen Geruch; das Oeffnen eines Gefässes mit Cyanallyl reicht hin, die Luft eines Zimmers mehrere Tage lang zu verpesten, ... " (Tem um odor penetrante e extremamente desagradável; a abertura de um frasco de alil [iso] cianeto é o suficiente para sujar o ar em uma sala por vários dias). Observe que na época de Lieke, a diferença entre isocianeto e nitrila não era totalmente avaliada.
Ivar Karl Ugi afirma que " O desenvolvimento da química dos isocianetos provavelmente sofreu apenas um pequeno atraso devido ao odor característico dos isonitrilos voláteis, que foi descrito por Hofmann e Gautier como 'altamente específico, quase opressor', 'horrível' e ' extremamente angustiante '. É verdade que muitos potenciais trabalhadores neste campo foram afastados pelo odor, mas isso é fortemente compensado pelo fato de que os isonitrilos podem ser detectados até mesmo em traços, e que a maioria das rotas que levam à formação de isonitrilas foram descobertas através do odor desses compostos. " Os isocianetos foram investigados como armas não letais em potencial .
Alguns isocianetos transmitem odores menos desagradáveis, como malte, borracha natural, creosoto, cereja ou madeira velha. Os derivados não voláteis, como o tosilmetil isocianeto , não apresentam odor.
Toxicidade
Enquanto alguns isocianetos ( por exemplo, isocianeto de ciclohexila) são tóxicos, outros "não apresentam toxicidade apreciável para mamíferos". Referindo-se ao isocianeto de etila, estudos toxicológicos na década de 1960 na Bayer mostraram que "doses orais e subcutâneas de 500-5000 mg / kg podem ser toleradas por camundongos".
Síntese
Muitas rotas para isocianetos foram desenvolvidas.
De formamidas
Comumente, os isocianetos são sintetizados por desidratação de formamidas . A formamida pode ser desidratada com cloreto de toluenossulfonil , oxicloreto de fósforo , fosgênio , difosgênio ou o reagente de Burgess na presença de uma base como piridina ou trietilamina.
- RNHC (O) H + ArSO 2 Cl + 2C 5 H 5 N → RNC + [C 5 H 5 NH] + [ArSO 3 ] - + [C 5 H 5 NH] + Cl -
Os precursores da formamida são, por sua vez, preparados a partir de aminas por formilação com ácido fórmico ou anidrido de formilacetila. Ou a partir da reação de Ritter de alcenos (e outras fontes de carbocações) e cianeto de hidrogênio.
De diclorocarbeno
Na reação da carbilamina (também conhecida como síntese de isocianeto de Hofmann), a base alcalina reage com o clorofórmio para produzir diclorocarbeno . O carbeno então converte aminas primárias em isocianetos. Ilustrativo é a síntese de terc- butil isocianeto a partir de terc- butilamina na presença de quantidade catalítica do catalisador de transferência de fase cloreto de benziltrietilamônio .
- Me 3 CNH 2 + CHCl 3 + 3 NaOH → Me 3 CNC + 3 NaCl + 3 H 2 O
Como só é eficaz para aminas primárias, essa reação pode ser usada como teste químico para verificar sua presença.
Rota do cianeto de prata
De interesse histórico, mas nem sempre de valor prático, o primeiro isocianeto, isocianeto de alila , foi preparado pela reação de iodeto de alila e cianeto de prata .
- RI + AgCN → RNC + AgI
Outros métodos
Outra rota para os isocianetos envolve a desprotonação de oxazoles e benzoxazoles na posição 2. O composto de organolítio resultante existe em equilíbrio químico com o 2-isocianofenolato , que pode ser capturado por um eletrófilo , como um cloreto de ácido .
Reações
Os isocianetos têm reatividade diversa.
Os isocianetos são estáveis a uma base forte (geralmente são feitos em condições fortemente básicas), mas são sensíveis ao ácido. Na presença de ácido aquoso, os isocianetos hidrolisam nas formamidas correspondentes :
- RNC + H 2 O → RN (H) C (O) H
Esta reação é usada para destruir misturas de isocianetos odoríferos. Alguns isocianetos podem polimerizar na presença dos ácidos de Lewis e Bronsted.
Os isocianetos participam de muitas reações multicomponentes de interesse na síntese orgânica , duas das quais são: a reação Ugi e a reação de Passerini .
Os isocianetos também participam de reações de cicloadição , como a cicloadição [4 + 1] com tetrazinas. Dependendo do grau de substituição do isocianeto, esta reação converte isocianetos em carbonilas ou dá cicloaddutos estáveis. Eles também são inseridos nas ligações C-Cl dos cloretos de acila na reação de isocianeto Nef , um processo que se acredita ser combinado e ilustra seu caráter carbeno.
Os isocianetos também mostraram ser um reagente útil em reações catalisadas por paládio com uma ampla variedade de compostos sendo formados usando este método.
A posição α dos isocianetos tem acidez substancial. Por exemplo, isocianeto de benzila tem um ap K a de 27,4. Em comparação, o cianeto de benzila tem um ap K a de 21,9. Na fase gasosa, CH 3 NC é 1,8 kcal / mol menos ácido do que CH 3 CN.
A cloração de isocianetos dá dicloretos de isocianeto .
Ligantes na química de coordenação

Os isocianetos formam complexos de coordenação com a maioria dos metais de transição. Eles se comportam como análogos ricos em elétrons do monóxido de carbono. Por exemplo , isocianeto de terc-butila forma Fe 2 (tBuNC) 9 , que é análogo a Fe 2 (CO) 9 . Embora estruturalmente semelhantes, os carbonilos análogos diferem de várias maneiras, principalmente porque t-BuNC é um ligante doador melhor do que CO. Assim, Fe (tBuNC) 5 é facilmente protonado, enquanto sua contraparte Fe (CO) 5 não é.
Isocianetos de ocorrência natural
Apenas alguns compostos de ocorrência natural exibem a funcionalidade isocianeto. O primeiro foi descoberto em 1957 em um extrato do fungo Penicillium notatum . O composto xantocilina mais tarde foi usado como um antibiótico . Desde então, vários outros isocianetos foram isolados. A maioria dos isocianetos marinhos são terpenóides, enquanto alguns dos isocianetos terrestres se originam de α-aminoácidos.
Nomenclatura
Enquanto na nomenclatura IUPAC, na maioria dos casos, o sufixo "isonitrila" ou "carbilamina" é usado para cianetos orgânicos (RC≡N), os nomes para isocianetos têm o prefixo "isociano". Os nomes IUPAC tornam-se isocianometano , isocianoetano, isocianopropano, etc.
O termo às vezes usado "carbilamina" entra em conflito com a nomenclatura sistemática. Uma amina sempre tem três ligações simples, enquanto um isocianeto tem apenas uma ligação única e uma ligação múltipla.
O grupo funcional isocianamida consiste em um grupo amino ligado a uma porção isocianamida . para nomenclatura como sufixo de isonitrila ou prefixo de isociano é usado dependendo da tabela de prioridade.

![{\ displaystyle \ left [{\ ce {R}} - {\ overset {\ oplus} {\ ce {N}}} {\ ce {#}} {\ overset {\ ominus} {\ ce {C}} } {\ ce {: \, <-> R - {\ ddot {N}} = C {:}}} \ direita]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/31596ad44ed69b7ad7230333e4059f48ef0d3b65)