Isoforona - Isophorone

|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
3,5,5-Trimetilciclohex-2-en-1-ona |
|
| Outros nomes
3,5,5-Trimetil-2-ciclohexeno-1-ona
1,1,3-Trimetil-3-ciclohexeno-5-ona Isoforona Isoacetoforona IP |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.001.024 |
| Número EC | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 9 H 14 O | |
| Massa molar | 138,210 g · mol −1 |
| Aparência | Líquido incolor a branco |
| Odor | Hortelã-pimenta |
| Densidade | 0,9255 g / cm 3 |
| Ponto de fusão | -8,1 ° C (17,4 ° F; 265,0 K) |
| Ponto de ebulição | 215,32 ° C (419,58 ° F; 488,47 K) |
| 1,2 g / 100 mL | |
| Solubilidade | éter , acetona , hexano , diclorometano , benzeno , tolueno , álcool |
| Pressão de vapor | 0,3 mmHg (20 ° C) |
|
Índice de refração ( n D )
|
1,4766 |
| Viscosidade | 2,62 cP |
| Termoquímica | |
| 43,4 kJ / mol | |
| Perigos | |
| Ponto de inflamação | 84 ° C (183 ° F; 357 K) |
| 460 ° C (860 ° F; 733 K) | |
| Limites explosivos | 0,8–3,8% |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
2280 mg / kg (rato, oral) 2330 mg / kg (rato, oral) 2690 mg / kg (camundongo, oral) |
|
LC 50 ( concentração mediana )
|
4600 ppm (cobaia, 8 h) |
|
LC Lo ( menor publicado )
|
885 ppm (rato, 6 horas) 1840 ppm (rato, 4 horas) |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
TWA 25 ppm (140 mg / m 3 ) |
|
REL (recomendado)
|
TWA 4 ppm (23 mg / m 3 ) |
|
IDLH (perigo imediato)
|
200 ppm |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
A isoforona é uma cetona cíclica α, β-insaturada . É um líquido incolor com um odor característico de hortelã-pimenta, embora as amostras comerciais possam parecer amareladas. Utilizado como solvente e precursor de polímeros, é produzido em larga escala industrialmente.
Estrutura e reatividade
A isoforona sofre reações características de uma cetona α, β-insaturada. A hidrogenação dá o derivado de ciclohexanona. A epoxidação com peróxido de hidrogênio básico fornece o óxido.
A isoforona é degradada pelo ataque de radicais hidroxila .
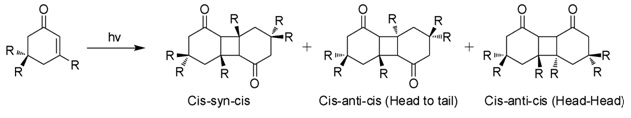
Fotodimerização
Quando exposta à luz solar em soluções aquosas, a isoforona sofre fotociclodição 2 + 2 para dar três fotodímeros isoméricos (Figura). Estes "dicetômeros" são cis-syn-cis, cabeça com cauda (HT), cys-anti-cys (HT) e cabeça-cabeça (HH). A formação de fotodímeros HH é favorecida em relação aos fotodímeros HT com o aumento da polaridade do meio.
Ocorrência Natural
A isoforona ocorre naturalmente em cranberries .
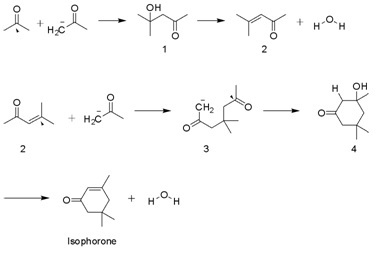
Síntese
A isoforona é produzida em uma escala de milhares de toneladas pela condensação aldólica da acetona usando KOH. Álcool de diacetona , óxido de mesitila e 3-hidroxi-3,5,5-trimetilciclohexan-1-ona são intermediários. Um produto secundário é a beta-isoforona , onde o grupo C = C não está conjugado com a cetona.
Formulários
O derivado parcialmente hidrogenado trimetilciclohexanona é usado na produção de policarbonatos . Condensa com fenol para dar um análogo de bisfenol A . Os policarbonatos produzidos pela fosgenação desses dois dióis produzem um polímero com estabilidade térmica aprimorada. O ácido trimetiladípico e a 2,2,4-trimetilhexametilenodiamina são produzidos a partir de trimetilciclohexanona e trimetilciclohexanol. Eles são usados para fazer poliamidas especiais . A hidrocianação dá o nitrilo seguido pela aminação redutiva dá a isoforona diamina . Esta diamina é usada para produzir diisocianato de isoforona que tem certas aplicações de nicho.
A hidrogenação completa dá 3,3,5-Trimetilciclohexanol , um precursor de filtros solares e armas químicas.
Segurança
O valor LD50 da isoforona em ratos e coelhos por exposição oral é de cerca de 2,00 g / kg. Os aspectos de segurança da isoforona foram objeto de vários estudos.
História
O uso da isoforona como solvente resultou da busca por formas de se destinar ou reciclar a acetona , produto residual da síntese de fenol pelo método de Hock .
Veja também
Referências
- ^ Merck Index , 13th Edition, 5215 .
- ^ a b c d e f Guia de bolso de NIOSH aos perigos químicos. "# 0355" . Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH).
- ^ a b c "Isoforona" . Concentrações imediatamente perigosas para a vida e a saúde (IDLH) . Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH).
- ^ a b c Hardo Siegel, Manfred Eggersdorfer (2005). "Cetonas". Enciclopédia de Química Industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a15_077 . ISBN 9783527306732 . CS1 maint: usa parâmetro de autores ( link )
- ^ Richard L. Wasson, Herbert O. House (1957). "Óxido de isoforona". Org. Synth . 37 : 58. doi : 10.15227 / orgsyn.037.0058 . CS1 maint: usa parâmetro de autores ( link )
- ^ "TOXNET" . toxnet.nlm.nih.gov . Arquivado do original em 24/10/2017 . Página visitada em 2016-03-11 .
- ^ Gonçalves, Huguette; Robinet, Germaine; Barthelat, Michèle; Lattes, Armand (28/01/1998). "Supramolecularity and Photodimerization of Isophorone: FTIR and Molecular Mechanics Studies". O Journal of Physical Chemistry Uma . 102 (8): 1279–1287. doi : 10.1021 / jp9729270 .
- ^ [1]
- ^ Volker Serini (2000). "Policarbonatos". Enciclopédia de Química Industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a21_207 . ISBN 978-3527306732 . CS1 maint: usa parâmetro de autores ( link )
- ^ "Efeitos de Toxicidade" . tools.niehs.nih.gov . Página visitada em 2016-03-11 .
- ^ W. Morton Grant, Dr. Joel S. Schuman (11 de fevereiro de 2016). "Toxicologia do olho: efeitos sobre os olhos e sistema visual de produtos químicos, drogas, metais e minerais, plantas, toxinas e venenos; também, efeitos colaterais sistêmicos do olho". Med (conjunto de 2 volumes) 4a edição, página 863 .
- ^ História da isoforona na Degussa