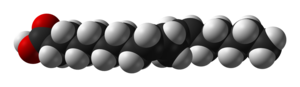
Ácido linoleico - Linoleic acid
|
|
|

|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Ácido (9 Z , 12 Z ) -Octadeca-9,12-dienóico |
|
| Outros nomes
cis , cis -9,12-ácido octadecadienóico
C18: 2 ( número de lipídios ) |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 3DMet | |
| 1727101 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard |
100.000.428 |
| Número EC | |
| 57557 | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 18 H 32 O 2 | |
| Massa molar | 280,452 g · mol −1 |
| Aparência | Óleo incolor |
| Densidade | 0,9 g / cm 3 |
| Ponto de fusão | −12 ° C (10 ° F) −6,9 ° C (19,6 ° F) −5 ° C (23 ° F) |
| Ponto de ebulição | 229 ° C (444 ° F) a 16 mmHg 230 ° C (446 ° F) a 21 mbar 230 ° C (446 ° F) a 16 mmHg |
| 0,139 mg / L | |
| Pressão de vapor | 16 Torr a 229 ° C |
| Perigos | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | 112 ° C (234 ° F) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O ácido linoléico é um composto orgânico com a fórmula COOH (CH 2 ) 7 CH = CHCH 2 CH = CH (CH 2 ) 4 CH 3 . Ambos os grupos alquenos são cis . É um ácido graxo às vezes denotado 18: 2 (n-6) ou 18: 2 cis- 9,12 . Um linoleato é um sal ou éster deste ácido.
O ácido linoléico é um ácido graxo ômega-6 poliinsaturado . É um óleo incolor ou branco que é virtualmente insolúvel em água, mas solúvel em muitos solventes orgânicos. Normalmente ocorre na natureza como um triglicerídeo (éster de glicerina ), em vez de um ácido graxo livre . É um dos dois ácidos graxos essenciais para os humanos, que devem ser obtidos por meio da dieta.
A palavra "linoléico" deriva do latim linum "linho" + oleum "óleo", refletindo o fato de que foi isolado pela primeira vez do óleo de linhaça .
Em fisiologia
O consumo de ácido linoléico é vital para uma boa saúde, pois é um ácido graxo essencial. Em ratos, foi demonstrado que uma dieta deficiente em linoleato (a forma de sal do ácido) causa descamação moderada da pele, queda de cabelo e cicatrização deficiente.
Metabolismo e eicosanóides
O ácido linoléico é um precursor do ácido araquidônico (AA) com alongamento e saturação. AA é o precursor de algumas prostaglandinas , leucotrienos (LTA, LTB, LTC) e tromboxano (TXA).
O metabolismo de LA em AA começa com a conversão de LA em ácido gama-linolênico (GLA), efetuado pela Δ 6 dessaturase . O GLA é convertido em ácido di-homo-γ-linolênico (DGLA), o precursor imediato do AA.
LA é também convertida por várias lipoxigenases , ciclo-oxigenases , citocromo P450 enzimas (CYP monooxigenases ), e não enzimáticos autoxidação mecanismos para mono- hidroxilo produtos viz,. Ácido 13-Hydroxyoctadecadienoic , e ácido 9-Hydroxyoctadecadienoic ; esses dois metabólitos hidroxilados são oxidados enzimaticamente em seus metabólitos ceto, ácido 13-oxo-octadecadienóico e ácido 9-oxo-octadecdienóico. Certas enzimas do citocromo P450, as epoxigenases CYP , catalisam a oxidação de LA em produtos epóxido, a saber, seu 12,13-epóxido, ácido vernólico , e seu 9,10-epóxido, ácido coronárico . Esses produtos de ácido linoléico estão implicados na fisiologia e patologia humana.
Usos e reações
O ácido linoléico é um componente de óleos de secagem rápida , úteis em tintas a óleo e vernizes . Essas aplicações exploram a labilidade dos grupos CH duplamente alílicos (-CH = CH-C H 2 -CH = CH-) em relação ao oxigênio no ar ( autoxidação ). A adição de oxigênio leva à reticulação e formação de um filme estável.
A redução do grupo ácido carboxílico do ácido linoléico produz álcool linoleílico .
O ácido linoléico é um surfactante com concentração micelar crítica de 1,5 x 10 −4 M @ pH 7,5.
O ácido linoléico tornou-se cada vez mais popular na indústria de produtos de beleza devido às suas propriedades benéficas na pele. Pesquisas apontam para as propriedades antiinflamatórias, redutoras de acne, clareadoras e retentoras de umidade do ácido linoléico quando aplicado topicamente na pele.
Fontes dietéticas
É abundante em óleo de cártamo , girassol e milho e compreende mais da metade de sua composição em peso. Está presente em quantidades médias em óleos de soja , gergelim e amêndoas .
| Nome | % LA † | ref. |
|---|---|---|
| Óleo de salicornia | 75% | |
| Óleo de cártamo | 74,62% | |
| Óleo de prímula | 65-80% | |
| Óleo de semente de melão | 70% | |
| Óleo de semente de papoula | 70% | |
| Óleo de semente de uva | 69,6% | |
| Óleo de girassol | 65,7% | |
| Óleo de semente de pera espinhosa | 63% | |
| Óleo de alcachofra | 60% | |
| Óleo de cânhamo | 54,3% | |
| Óleo de milho | 59% | |
| Óleo de gérmen de trigo | 55% | |
| Óleo de semente de algodão | 54% | |
| Óleo de soja | 51% | |
| óleo de noz | 51% | |
| Óleo de gergelim | 45% | |
| Óleo de farelo de arroz | 39% | |
| óleo de argan | 37% | |
| Óleo de pistache | 32,7% | |
| Óleo de amendoim | 32% | |
| Óleo de pêssego | 29% | |
| Amêndoas | 24% | |
| Óleo de canola | 21% | |
| Gordura de frango | 18-23% | |
| ovo gema | 16% | |
| Óleo de linhaça (linho) | 15% | |
| Banha | 10% | |
| Azeite | 10% (3,5 - 21%) | |
| azeite de dendê | 10% | |
| Durio graveolens | 4,95% | |
| Manteiga de cacau | 3% | |
| Óleo de macadâmia | 2% | |
| Manteiga | 2% | |
| Óleo de côco | 2% | |
| † val médio | ||
Outras ocorrências
As baratas liberam ácido oleico e linoléico após a morte, o que desencoraja outras baratas de entrar na área. Isso é semelhante ao mecanismo encontrado em formigas e abelhas, que liberam ácido oleico após a morte.
História
Em 1844, F. Sacc , trabalhando no laboratório de Justus von Liebig , isolou o ácido linoléico do óleo de linhaça. Em 1886, K. Peters determinou a existência de duas ligações duplas. Seu papel essencial na dieta humana foi descoberto por GO Burr e outros em 1930. Sua estrutura química foi determinada por TP Hilditch e outros em 1939, e foi sintetizado por RA Raphael e F. Sondheimer em 1950.
Veja também
- Ácido linoléico conjugado
- Ácido graxo ômega-6: efeitos negativos para a saúde
- Ácidos graxos essenciais
- Interações de ácidos graxos essenciais
- Eicosanóides
- Nutrientes essenciais
- Linolein
Referências
- ^ a b c O índice Merck , 11a edição, 5382
- ^ a b c William M. Haynes (2016). CRC Handbook of Chemistry and Physics (97ª ed.). Boca Raton: CRC Press. pp. 3–338. ISBN 978-1-4987-5429-3.
- ^ a b c d Registro de CAS RN 60-33-3 no banco de dados de substância GESTIS do instituto para segurança e saúde ocupacional
- ^ "Ácidos graxos" . Cyber Lipid. Arquivado do original em 28 de outubro de 2018 . Retirado em 31 de julho de 2017 .
- ^ Mattes, RD (2009). "Existe um gosto de ácido graxo?" . Annu. Rev. Nutr . 29 : 305–27. doi : 10.1146 / annurev-nutr-080508-141108 . PMC 2843518 . PMID 19400700 .
- ^ Simopoulos, Artemis P. (2008). "A importância da proporção de ácidos graxos ômega-6 / ômega-3 nas doenças cardiovasculares e outras doenças crônicas" . Biologia Experimental e Medicina . 233 (6): 674–688. doi : 10.3181 / 0711-mr-311 . PMID 18408140 . S2CID 9044197 .
- ^ Whelan, Jay; Fritsche, Kevin (maio de 2013). "Ácido Linoleico" . Avanços na nutrição . 4 (3): 311–312. doi : 10.3945 / an.113.003772 . PMC 3650500 . PMID 23674797 .
- ^ Cunnane S, Anderson M (1 de abril de 1997). "Deficiência puro linoleato no rato: influência sobre o crescimento, a acumulação de ácidos gordos polinsaturados n-6, e (1- 14 C) oxidação linoleato" . J Lipid Res . 38 (4): 805–12. doi : 10.1016 / S0022-2275 (20) 37247-3 . PMID 9144095 . Página visitada em 15 de janeiro de 2007 .
- ^ Ruthig DJ, Meckling-Gill KA (1º de outubro de 1999). "Ambos os ácidos graxos (n-3) e (n-6) estimulam a cicatrização de feridas na linha de células epiteliais intestinais de rato, IEC-6" . Journal of Nutrition . 129 (10): 1791–8. doi : 10.1093 / jn / 129.10.1791 . PMID 10498749 .
- ^ Whelan J, Fritsche K. (2013). "Ácido linoléico" . Adv Nutr . 4 (3): 311–312. doi : 10.3945 / an.113.003772 . PMC 3650500 . PMID 23674797 .CS1 maint: usa o parâmetro de autores ( link )
- ^ Wlodawer, P; Samuelsson, B (1973). Na organização e mecanismo da prostaglandina sintetase " . The Journal of Biological Chemistry . 248 (16): 5673–8. doi : 10.1016 / S0021-9258 (19) 43558-8 . PMID 4723909 .
- ^ Terano, Takashi; Salmon, John A .; Moncada, Salvador (1984). "Biossíntese e atividade biológica do leucotrieno B5". Prostaglandinas . 27 (2): 217–32. doi : 10.1016 / 0090-6980 (84) 90075-3 . PMID 6326200 .
- ^ As evidências sugerem que os bebês devem adquirir Δ 6 dessaturase do leite materno. Bebês alimentados com leite materno têm concentrações mais altas de GLA do que bebês alimentados com fórmula, enquanto bebês alimentados com fórmula têm concentrações elevadas de LA David F. Horrobin (1993). "Metabolismo dos ácidos graxos na saúde e na doença: o papel da Δ-6-desaturase". American Journal of Clinical Nutrition . 57 (5 Suplemento): 732S – 7S. doi : 10.1093 / ajcn / 57.5.732S . PMID 8386433 .
- ^ Jandacek, Ronald J. (20 de maio de 2017). "Linoleic Acid: A Nutritional Quandary" . Cuidados de saúde . 5 (2): 25. doi : 10.3390 / Health5020025 . ISSN 2227-9032 . PMC 5492028 . PMID 28531128 .
- ^ Ulrich Poth (2002). "Óleos de Secagem e Produtos Relacionados". Enciclopédia de Química Industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a09_055 .
- ^ Adkins, Homer; Gillespie, RH (1949). "Álcool oleílico". Sínteses orgânicas . 29 : 80. doi : 10.15227 / orgsyn.029.0080 .
- ^ Diezel, WE; Schulz, E .; Skanks, M .; Heise, H. (1993). "Óleos vegetais: aplicação tópica e efeitos antiinflamatórios (teste de óleo de cróton)". Dermatologische Monatsschrift . 179 : 173.
- ^ Letawe, C; Boone, M; Pierard, GE (março de 1998). "Análise de imagens digitais do efeito do ácido linoléico aplicado topicamente sobre os microcomedões da acne". Dermatologia Clínica e Experimental . 23 (2): 56–58. doi : 10.1046 / j.1365-2230.1998.00315.x . PMID 9692305 . S2CID 28594076 .
- ^ Ando, H; Ryu, A; Hashimoto, A; Oka, M; Ichihashi, M (março de 1998). "O ácido linoléico e o ácido α-linolênico iluminam a hiperpigmentação da pele induzida por ultravioleta". Arquivos de Pesquisa Dermatológica . 290 (7): 375–381. doi : 10.1007 / s004030050320 . PMID 9749992 . S2CID 23036319 .
- ^ Darmstadt, GL; Mao-Qiang, M; Chi, E; Saha, SK; Ziboh, VA; Preto, RE; Santosham, M; Elias, PM (2002). "Impacto dos óleos tópicos na barreira da pele: possíveis implicações para a saúde neonatal em países em desenvolvimento". Acta Paediatrica . 91 (5): 546–554. CiteSeerX 10.1.1.475.1064 . doi : 10.1080 / 080352502753711678 . PMID 12113324 .
- ^ "Home Page do Laboratório de Dados Nutrientes" . USDA National Nutrient Database for Standard Reference, Release 20 . Departamento de Agricultura dos EUA, Serviço de Pesquisa Agrícola. 2007. Arquivado do original em 14 de abril de 2016.
- ^ Kaur, Narinder; Chugh, Vishal; Gupta, Anil K. (outubro de 2014). "Ácidos graxos essenciais como componentes funcionais dos alimentos - uma revisão" . Journal of Food Science and Technology . 51 (10): 2289–2303. doi : 10.1007 / s13197-012-0677-0 . PMC 4190204 . PMID 25328170 .
- ^ "Óleo de prímula para a menopausa ajuda" . 26 de janeiro de 2018.
- ^ Oomah, B. Dave; Busson, Muriel; Godfrey, David V; Drover, John C. G (1 de janeiro de 2002). "Características do óleo de semente de cânhamo (Cannabis sativa L.)". Food Chemistry . 76 (1): 33–43. doi : 10.1016 / S0308-8146 (01) 00245-X .
- ^ Óleo, amendoim, salada ou culinária: pesquise óleo de amendoim em "USDA Food Composition Databases" . Arquivado do original em 3 de março de 2015 . Página visitada em 16 de setembro de 2009 .
- ^ Wu, Hao; Shi, John; Xue, Sophia; Kakuda, Yukio; Wang, Dongfeng; Jiang, Yueming; Sim, Xingqian; Li, Yanjun; Subramanian, Jayasankar (2011). “Óleo essencial extraído do grão de pêssego (Prunus persica) e suas propriedades físico-químicas e antioxidantes”. LWT - Food Science and Technology . 44 (10): 2032–2039. doi : 10.1016 / j.lwt.2011.05.012 .
- ^ MK Nutter, EE Lockhart e RS Harris (1943). "A composição química das gorduras de depósito em galinhas e perus". Jornal da American Oil Chemists 'Society . 20 (11): 231–234. doi : 10.1007 / BF02630880 . S2CID 84893770 .
- ^ "Azeite: características químicas" .
- ^ Beltran; Del Rio, C; Sánchez, S; Martínez, L (2004). "Influência da data de colheita e rendimento da colheita na composição de ácidos graxos de azeites virgens de Cv. Picual" (PDF) . J. Agric. Food Chem . 52 (11): 3434–3440. doi : 10.1021 / jf049894n . PMID 15161211 .
- ^ Nasaruddin, Mohd hanif; Noor, Noor Qhairul Izzreen Mohd; Mamat, Hasmadi (2013). "Komposisi Proksimat dan Komponen Asid Lemak Durian Kuning (Durio graveolens) Sabah" [Composição de ácidos graxos e próximos de Sabah Yellow Durian ( Durio graveolens )] (PDF) . Sains Malaysiana (em malaio). 42 (9): 1283–1288. ISSN 0126-6039 . OCLC 857479186 . Retirado em 28 de novembro de 2017 .
- ^ "Notícias da Terra: Antigo 'cheiro de morte' revelado" . BBC. 9 de setembro de 2009.
- ^ F. Sacc (1844) "Ueber das Leinöl, seine physicalischen und chemischen Eigenscharften und seine Oxydationsproducte". Liebig Annalen , volume 51, páginas 213-230.
- ^ F. Sacc (1845): " Expériences sur les propriétés physiques et chimiques de l'huile de Lin ". SChweizer. Gesell. N. Dekschr. , volume 7
- ^ (1886), Monatsch ., Volume 7, páginas 522-
- ^ (1930: J Biol Chem , volume 86, páginas 587-
- ^ RA Raphael e Franz Sondheimer (1950): "A síntese de ácidos alifáticos de cadeia longa a partir de compostos acetilênicos. Parte III. A síntese de ácido linoléico". Journal of the Chemical Society ( retomado ), artigo 432, doi : 10.1039 / jr9500002100
Leitura adicional
- "Resumo do composto: ácido linoléico" . PubChem . Biblioteca Nacional de Medicina dos EUA.
links externos
- Espectro de MS de ácido linoléico
- Ácidos graxos: ligações duplas interrompidas por metileno , biblioteca de lipídios AOCS


