Borohidreto de lítio - Lithium borohydride

|
|
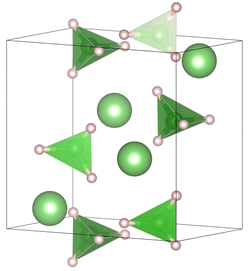 Célula unitária de borohidreto de lítio em temperatura ambiente
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Tetrahidridoborato de lítio (1–)
|
|
| Outros nomes
Hidroborato de lítio,
tetrahidroborato de lítio Borato (1-), tetrahidro-, lítio, boranato de lítio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.037.277 |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| LiBH 4 | |
| Massa molar | 21,784 g / mol |
| Aparência | Sólido branco |
| Densidade | 0,666 g / cm 3 |
| Ponto de fusão | 268 ° C (514 ° F; 541 K) |
| Ponto de ebulição | 380 ° C (716 ° F; 653 K) se decompõe |
| reage | |
| Solubilidade em éter | 2,5 g / 100 mL |
| Estrutura | |
| ortorrômbico | |
| Pnma | |
|
a = 7,17858 (4), b = 4,43686 (2), c = 6,80321 (4)
|
|
|
Volume da rede ( V )
|
216,685 (3) A 3 |
|
Unidades de fórmula ( Z )
|
4 |
| [4] B | |
| Termoquímica | |
|
Capacidade de calor ( C )
|
82,6 J / mol K |
|
Entropia molar padrão ( S |
75,7 J / mol K |
| -198,83 kJ / mol | |
| Perigos | |
| > 180 ° C (356 ° F; 453 K) | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O borohidreto de lítio (LiBH 4 ) é um borohidreto conhecido em síntese orgânica como um agente redutor de ésteres . Embora menos comum do que o boro-hidreto de sódio relacionado , o sal de lítio oferece algumas vantagens, sendo um agente redutor mais forte e altamente solúvel em éteres, embora permaneça mais seguro de manusear do que o hidreto de alumínio e lítio .
Preparação
O boro-hidreto de lítio pode ser preparado pela reação de metátese que ocorre na moagem de bolas do boro-hidreto de sódio e brometo de lítio mais comumente disponíveis :
- NaBH 4 + LiBr → NaBr + LiBH 4
Alternativamente, pode ser sintetizado por tratamento de trifluoreto de boro com hidreto de lítio em éter dietílico :
- BF 3 + 4 LiH → LiBH 4 + 3 LiF
Reações
O borohidreto de lítio é um agente redutor mais forte do que o borohidreto de sódio . Em misturas de metanol e éter dietílico , o boro-hidreto de lítio é capaz de reduzir os ésteres em álcoois e as amidas primárias em aminas . Em contraste, esses substratos não são afetados pelo boro-hidreto de sódio. A reatividade aumentada é atribuída à polarização do substrato de carbonila por complexação com o cátion de lítio.
Quimiosseletividade
O uso de boro-hidreto de lítio é particularmente vantajoso em algumas preparações devido à sua maior quimiosseletividade em relação a outros agentes redutores populares, como hidreto de alumínio e lítio . Por exemplo, ao contrário do hidreto de alumínio e lítio, o boro-hidreto de lítio reduzirá os ésteres, nitrilos , lactonas , amidas primárias e epóxidos enquanto poupa grupos nitro , ácidos carbâmicos , halogenetos de alquila e amidas secundárias / terciárias .
Geração de hidrogênio
O borohidreto de lítio reage com a água para produzir hidrogênio. Esta reação pode ser usada para geração de hidrogênio.
Armazenamento de energia

O borohidreto de lítio é conhecido como um dos transportadores de energia química de maior densidade de energia . Embora atualmente sem importância prática, o sólido irá liberar 65 MJ / kg de calor após o tratamento com oxigênio atmosférico. Uma vez que tem uma densidade de 0,67 g / cm 3 , oxidação de boro-hidreto de lítio líquido dá 43 MJ / L . Em comparação, a gasolina dá 44 MJ / kg (ou 35 MJ / L), enquanto o hidrogênio líquido dá 120 MJ / kg (ou 8,0 MJ / L). A alta densidade de energia específica do borohidreto de lítio tornou-o um candidato atraente a ser proposto como combustível para automóveis e foguetes, mas, apesar da pesquisa e defesa, ele não foi amplamente utilizado. Tal como acontece com todos os transportadores de energia à base de hidreto químico, o boro-hidreto de lítio é muito complexo para reciclar (isto é, recarregar) e, portanto, sofre de uma baixa eficiência de conversão de energia . Embora as baterias, tais como iões de lítio transportar uma densidade de energia de até 0,72 MJ / kg e 2,0 MJ / L, o seu DC para DC eficiência de conversão pode ser tão elevada quanto 90%. Em vista da complexidade dos mecanismos de reciclagem de hidretos metálicos, tais eficiências de conversão de alta energia não são práticas com a tecnologia atual.
| Substância | Energia específica MJ / kg | Densidade g / cm 3 | Densidade de energia MJ / L |
|---|---|---|---|
| LiBH 4 | 65,2 | 0,666 | 43,4 |
| Gasolina normal | 44 | 0,72 | 34,8 |
| Hidrogênio líquido | 120 | 0,0708 | 8 |
| bateria de íon de lítio | 0,72 | 2,8 | 2 |
Veja também
Notas
- ^ A maior proporção de densidade de energia para energia específica para hidrogênio é devido à densidade de massa muito baixa (0,071 g / cm 3 ).

