Óxido de lítio - Lithium oxide

|
|
|
|
 |
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Óxido de lítio
|
|
| Outros nomes
Lithia, Kickerite
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.031.823 |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
|
Li 2O |
|
| Massa molar | 29,88 g / mol |
| Aparência | sólido branco |
| Densidade | 2,013 g / cm 3 |
| Ponto de fusão | 1.438 ° C (2.620 ° F; 1.711 K) |
| Ponto de ebulição | 2.600 ° C (4.710 ° F; 2.870 K) |
| reage violentamente para formar LiOH | |
| log P | 9,23 |
|
Índice de refração ( n D )
|
1.644 |
| Estrutura | |
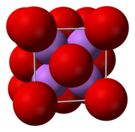
| Antifluorito (cúbico), cF12 | |
| Fm 3 m, No. 225 | |
| Tetraédrico (Li + ); cúbico (O 2− ) | |
| Termoquímica | |
|
Capacidade de calor ( C )
|
1,8105 J / g K ou 54,1 J / mol K |
|
Entropia molar padrão ( S |
37,89 J / mol K |
| -20,01 kJ / g ou -595,8 kJ / mol | |
|
Energia livre de Gibbs (Δ f G ˚)
|
-562,1 kJ / mol |
| Perigos | |
| Riscos principais | Corrosivo, reage violentamente com a água |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| Compostos relacionados | |
|
Outros ânions
|
Sulfeto de lítio |
|
Outros cátions
|
Óxido de sódio Óxido de potássio Óxido de rubídio Óxido de césio |
|
Peróxido de lítio Superóxido de lítio |
|
|
Compostos relacionados
|
Hidróxido de lítio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
Óxido de lítio ( Li
2O ) ou lithia é um composto químico inorgânico . É um sólido branco. Embora não seja especificamente importante, muitos materiais são avaliados com base em seu conteúdo de Li 2 O. Por exemplo, o conteúdo de Li 2 O do principal espodumênio mineral de lítio (LiAlSi 2 O 6 ) é de 8,03%.
Produção
O óxido de lítio é produzido pela decomposição térmica do peróxido de lítio a 300-400 ° C.
O óxido de lítio se forma junto com pequenas quantidades de peróxido de lítio quando o metal de lítio é queimado no ar e se combina com o oxigênio:
- 4Li + O
2→ 2 Li
2O .
Li puro
2O pode ser produzido pela decomposição térmica do peróxido de lítio , Li
2O
2, a 450 ° C
- 2 li
2O
2→ 2 Li
2O + O
2
Estrutura
O óxido de lítio sólido adota uma estrutura antifluorita com centros de Li + de quatro coordenadas e óxidos de oito coordenadas.
O estado fundamental da fase gasosa Li
2A molécula O é linear com um comprimento de ligação consistente com uma forte ligação iônica. A teoria VSEPR preveria uma forma dobrada semelhante a H
2O .
Usos
O óxido de lítio é usado como fundente em esmaltes cerâmicos; e cria azuis com cobre e rosa com cobalto . O óxido de lítio reage com água e vapor , formando hidróxido de lítio e deve ser isolado deles.
Seu uso também está sendo investigado para avaliação de espectroscopia de emissão não destrutiva e monitoramento de degradação em sistemas de revestimento de barreira térmica . Ele pode ser adicionado como um co-dopante com ítria na camada superior de cerâmica de zircônia, sem uma grande diminuição na vida útil esperada do revestimento. Em altas temperaturas, o óxido de lítio emite um padrão espectral muito detectável, que aumenta de intensidade junto com a degradação do revestimento. A implementação permitiria o monitoramento in situ de tais sistemas, possibilitando um meio eficiente de prever a vida útil até a falha ou manutenção necessária.
O metal de lítio pode ser obtido a partir do óxido de lítio por eletrólise, liberando oxigênio como subproduto.


