Doença de Lyme - Lyme disease
| Doença de Lyme | |
|---|---|
| Outros nomes | Borreliose de Lyme |
 | |
| Um carrapato adulto (a maioria dos casos de Lyme é causada por ninfas, e não por carrapatos adultos) | |
| Especialidade | Doença infecciosa |
| Sintomas | Expansão da área de vermelhidão no local da picada de um carrapato , febre , dor de cabeça , cansaço |
| Complicações | Paralisia do nervo facial , artrite , meningite |
| Início usual | Uma semana depois de uma mordida |
| Causas | Borrelia espalhada por carrapatos |
| Método de diagnóstico | Com base nos sintomas, exposição a carrapatos, exames de sangue |
| Prevenção | Prevenção de picadas de carrapatos (vestir os membros, DEET ), doxiciclina |
| Medicamento | Doxiciclina , amoxicilina , ceftriaxona , cefuroxima |
| Frequência | ~ 476.000 por ano nos EUA (2010-2018) |
A doença de Lyme , também conhecida como borreliose de Lyme , é uma doença transmitida por um vetor causada pela bactéria Borrelia, que é transmitida por carrapatos do gênero Ixodes . O sinal mais comum de infecção é uma erupção cutânea vermelha em expansão , conhecida como eritema migrante , que aparece no local da picada do carrapato cerca de uma semana depois de sua ocorrência. A erupção geralmente não causa coceira nem dor. Aproximadamente 70–80% das pessoas infectadas desenvolvem erupções na pele. O diagnóstico precoce pode ser difícil. Outros sintomas iniciais podem incluir febre, dor de cabeça e cansaço . Se não for tratada, os sintomas podem incluir perda da capacidade de mover um ou ambos os lados da face , dores nas articulações , fortes dores de cabeça com rigidez do pescoço ou palpitações cardíacas , entre outros. Meses a anos mais tarde, podem ocorrer episódios repetidos de dor e inchaço nas articulações. Ocasionalmente, as pessoas desenvolvem dores agudas ou formigamento nos braços e nas pernas. Apesar do tratamento adequado, cerca de 10 a 20% das pessoas desenvolvem dores nas articulações, problemas de memória e cansaço por pelo menos seis meses.
A doença de Lyme é transmitida aos humanos pela picada de carrapatos infectados do gênero Ixodes . Nos Estados Unidos, os carrapatos que causam preocupação são geralmente do tipo Ixodes scapularis e devem ser fixados por pelo menos 36 horas antes que a bactéria possa se espalhar. Na Europa, os carrapatos Ixodes ricinus podem espalhar a bactéria mais rapidamente. Na América do Norte, as bactérias de Borrelia burgdorferi , B. bissettiae , e B. mayonii causam a doença de Lyme. Na Europa e na Ásia, Borrelia afzelii , Borrelia garinii , B. spielmanii , e 4 outras espécies também causam a doença. A doença não parece ser transmissível entre pessoas, por outros animais ou através dos alimentos. O diagnóstico é baseado em uma combinação de sintomas, história de exposição a carrapatos e, possivelmente, testes de anticorpos específicos no sangue. Os exames de sangue costumam ser negativos nos estágios iniciais da doença. O teste de carrapatos individuais normalmente não é útil.
A prevenção inclui esforços para prevenir picadas de carrapatos usando roupas para cobrir os braços e pernas e usando DEET ou repelentes de insetos à base de picaridina . O uso de pesticidas para reduzir o número de carrapatos também pode ser eficaz. Os carrapatos podem ser removidos com uma pinça . Se o carrapato removido estava cheio de sangue, uma única dose de doxiciclina pode ser usada para prevenir o desenvolvimento de infecção, mas geralmente não é recomendada, pois o desenvolvimento de infecção é raro. Se uma infecção se desenvolver, vários antibióticos são eficazes, incluindo doxiciclina, amoxicilina e cefuroxima . O tratamento padrão geralmente dura duas ou três semanas. Algumas pessoas desenvolvem febre e dores musculares e nas articulações devido ao tratamento que pode durar um ou dois dias. Naqueles que desenvolvem sintomas persistentes, a antibioticoterapia de longo prazo não se mostrou útil.
A doença de Lyme é a doença mais comum transmitida por carrapatos no hemisfério norte . Estima-se que afete 300.000 pessoas por ano nos Estados Unidos e 65.000 pessoas por ano na Europa. As infecções são mais comuns na primavera e no início do verão. A doença de Lyme foi diagnosticada como uma condição separada pela primeira vez em 1975 em Lyme, Connecticut . Foi originalmente confundido com artrite reumatóide juvenil . A bactéria envolvida foi descrita pela primeira vez em 1981 por Willy Burgdorfer . Os sintomas crônicos após o tratamento são bem descritos e são conhecidos como "síndrome da doença de Lyme pós-tratamento" (PTLDS). PTLDS é diferente da doença de Lyme crônica , um termo não mais apoiado pela comunidade científica e usado de diferentes maneiras por diferentes grupos. Alguns profissionais de saúde afirmam que o PTLDS é causado por infecção persistente, mas não se acredita que isso seja verdade porque nenhuma evidência de infecção persistente pode ser encontrada após o tratamento padrão. Uma vacina para a doença de Lyme foi comercializada nos Estados Unidos entre 1998 e 2002, mas foi retirada do mercado devido às vendas fracas. A pesquisa está em andamento para desenvolver novas vacinas.
sinais e sintomas

A doença de Lyme pode afetar vários sistemas do corpo e produzir uma ampla gama de sintomas. Nem todas as pessoas com a doença de Lyme apresentam todos os sintomas, e muitos dos sintomas não são específicos da doença de Lyme, mas também podem ocorrer com outras doenças.
O período de incubação desde a infecção até o início dos sintomas é geralmente de uma a duas semanas, mas pode ser muito mais curto (dias) ou muito mais longo (meses a anos). Os sintomas de Lyme ocorrem com mais frequência de maio a setembro no hemisfério norte, porque o estágio ninfal do carrapato é responsável pela maioria dos casos. A infecção assintomática existe, mas ocorre em menos de 7% dos indivíduos infectados nos Estados Unidos. A infecção assintomática pode ser muito mais comum entre as pessoas infectadas na Europa.
Infecção localizada precoce
A infecção localizada precoce pode ocorrer quando a infecção ainda não se espalhou por todo o corpo. Somente o local onde a infecção entrou em contato com a pele é afetado. O sinal inicial de cerca de 80% das infecções de Lyme é uma erupção cutânea com eritema migratório (EM) no local da picada de um carrapato, geralmente perto de dobras cutâneas, como axila , virilha ou parte de trás do joelho , no tronco , sob as roupas tiras, ou no cabelo, orelhas ou pescoço das crianças. A maioria das pessoas infectadas não se lembra de ter visto um carrapato ou uma picada. A erupção aparece tipicamente uma ou duas semanas (variação de 3 a 32 dias) após a picada e se expande de 2 a 3 cm por dia até um diâmetro de 5 a 70 cm (mediana de 16 cm). A erupção é geralmente circular ou oval, vermelha ou azulada e pode ter um centro elevado ou mais escuro. Em cerca de 79% dos casos na Europa, mas apenas em 19% dos casos em áreas endêmicas dos Estados Unidos, a erupção gradualmente desaparece do centro em direção às bordas, possivelmente formando um padrão de "olho de boi". A erupção pode ficar quente, mas geralmente não coça, raramente é sensível ou dolorida e leva até quatro semanas para desaparecer se não for tratada.
A erupção EM é frequentemente acompanhada por sintomas de uma doença semelhante a um vírus, incluindo fadiga, dor de cabeça, dores no corpo, febre e calafrios, mas geralmente não é náusea ou problemas respiratórios superiores. Esses sintomas também podem aparecer sem erupção na pele ou permanecer após o desaparecimento da erupção. Lyme pode progredir para estágios posteriores sem esses sintomas ou erupção cutânea.
Pessoas com febre alta por mais de dois dias ou cujos outros sintomas de doenças semelhantes a vírus não melhoram apesar do tratamento com antibióticos para a doença de Lyme, ou que têm níveis anormalmente baixos de glóbulos brancos ou vermelhos ou plaquetas no sangue, devem ser investigados para possível coinfecção com outras doenças transmitidas por carrapatos , como erliquiose e babesiose .
Infecção disseminada precoce
Dentro de dias a semanas após o início da infecção local, a bactéria Borrelia pode se espalhar através do sistema linfático ou corrente sanguínea. Em 10-20% dos casos não tratados, erupções cutâneas EM se desenvolvem em locais por todo o corpo que não têm relação com a picada original do carrapato. Dores musculares transitórias e dores nas articulações também são comuns.
Em cerca de 10-15% das pessoas não tratadas, Lyme causa problemas neurológicos conhecidos como neuroborreliose . A neuroborreliose inicial geralmente aparece de 4 a 6 semanas (variação de 1 a 12 semanas) após a picada do carrapato e envolve alguma combinação de meningite linfocítica, neurite craniana, radiculopatia e / ou mononeurite múltipla. A meningite linfocítica causa alterações características no líquido cefalorraquidiano (LCR) e pode ser acompanhada por várias semanas por cefaleia variável e, menos comumente, sinais de meningite geralmente leves , como incapacidade de flexionar totalmente o pescoço e intolerância a luzes fortes , mas normalmente nenhum ou apenas febre muito baixa. Após vários meses, a neuroborreliose também pode apresentar sintomas otorrinolaringológicos. Até 76,5% desses otorrinolaringológicos apresentam-se como zumbido, o sintoma mais comum. Vertigem e tontura (53,7%) e hipoacusia (16,7%) foram os próximos sintomas mais comuns. Em crianças, também pode ocorrer perda parcial de visão . A neurite craniana é uma inflamação dos nervos cranianos . Quando devido a Lyme, geralmente causa paralisia facial que prejudica o piscar, o sorriso e a mastigação em um ou ambos os lados do rosto. Também pode causar visão dupla intermitente . A radiculopatia de Lyme é uma inflamação das raízes nervosas espinhais que costuma causar dor e, menos frequentemente , fraqueza , dormência ou sensação alterada nas áreas do corpo servidas por nervos conectados às raízes afetadas , por exemplo, membro (s) ou parte (s) do tronco . A dor é frequentemente descrita como diferente de qualquer outra sentida anteriormente, excruciante, migrante, piora à noite, raramente simétrica e frequentemente acompanhada por distúrbios extremos do sono. Mononeurite múltipla é uma inflamação que causa sintomas semelhantes em um ou mais nervos periféricos não relacionados. Raramente, neuroborreliose precoce pode envolver a inflamação do cérebro ou da medula espinal , com sintomas tais como confusão, marcha anormal, os movimentos oculares, ou discurso , movimento auditivos , planejamento motor prejudicada , ou agitando .
Na América do Norte, a paralisia facial é a apresentação típica de neuroborreliose precoce, ocorrendo em 5–10% das pessoas não tratadas, em cerca de 75% dos casos acompanhada de meningite linfocítica. A radiculopatia de Lyme é relatada com metade da freqüência, mas muitos casos podem não ser reconhecidos. Em adultos europeus, a apresentação mais comum é uma combinação de meningite linfocítica e radiculopatia conhecida como síndrome de Bannwarth , acompanhada em 36-89% dos casos por paralisia facial. Nessa síndrome, a dor radicular tende a começar na mesma região do corpo que a erupção cutânea com eritema migrans inicial , se houver, e precede uma possível paralisia facial e outros movimentos prejudicados . Em casos extremos, pode ocorrer comprometimento permanente da função motora ou sensorial dos membros inferiores. Em crianças europeias, as manifestações mais comuns são paralisia facial (em 55%), outras neurites cranianas e meningite linfocítica (em 27%).
Em cerca de 4–10% dos casos não tratados nos EUA e 0,3–4% dos casos não tratados na Europa, normalmente entre junho e dezembro, cerca de um mês (intervalo de 4 dias a 7 meses) após a picada do carrapato, a infecção pode causar o coração complicações conhecidas como cardite de Lyme . Os sintomas podem incluir palpitações cardíacas (em 69% das pessoas), tonturas , desmaios , falta de ar e dor no peito . Outros sintomas da doença de Lyme também podem estar presentes, como erupção cutânea EM , dores nas articulações , paralisia facial , dores de cabeça ou dor radicular . Em algumas pessoas, entretanto, a cardite pode ser a primeira manifestação da doença de Lyme. Lyme cardite em 19-87% das pessoas impacta negativamente no sistema de condução elétrica do coração, causando atrioventricular bloco que muitas vezes se manifesta como ritmos cardíacos que se alternam dentro de minutos entre anormalmente lento e anormalmente rápida. Em 10-15% das pessoas, Lyme causa complicações miocárdicas , como cardiomegalia , disfunção ventricular esquerda ou insuficiência cardíaca congestiva.
Outra doença de pele, encontrada na Europa, mas não na América do Norte, é o linfocitoma borrelial , um caroço arroxeado que se desenvolve no lóbulo da orelha, mamilo ou escroto .
Infecção disseminada tardia
Após vários meses, pessoas não tratadas ou tratadas de forma inadequada podem desenvolver sintomas crônicos que afetam muitas partes do corpo, incluindo articulações, nervos, cérebro, olhos e coração.
A artrite de Lyme ocorre em até 60% das pessoas não tratadas, geralmente começando cerca de seis meses após a infecção. Geralmente afeta apenas uma ou algumas articulações, geralmente um joelho ou possivelmente o quadril , outras articulações grandes ou a articulação temporomandibular . Geralmente há grande derrame e inchaço nas articulações , mas apenas dor leve ou moderada. Sem tratamento, o inchaço e a dor geralmente desaparecem com o tempo, mas retornam periodicamente. Os cistos de Baker podem se formar e romper. Em alguns casos, ocorre erosão articular.
Sintomas neurológicos crônicos ocorrem em até 5% das pessoas não tratadas. Uma neuropatia periférica ou polineuropatia pode se desenvolver, causando sensações anormais , como dormência, formigamento ou queimação, começando nos pés ou nas mãos e, com o tempo, possivelmente subindo pelos membros. Um teste pode mostrar uma sensação reduzida de vibrações nos pés. Uma pessoa afetada pode sentir como se estivesse usando uma meia ou luva, sem realmente fazer isso.
Uma síndrome neurológica chamada encefalopatia de Lyme está associada com memória sutil e dificuldades cognitivas, insônia , uma sensação geral de mal-estar e mudanças na personalidade. No entanto, problemas como depressão e fibromialgia são tão comuns em pessoas com doença de Lyme quanto na população em geral.
Lyme pode causar uma encefalomielite crônica que se assemelha à esclerose múltipla . Pode ser progressivo e envolver comprometimento cognitivo, névoa cerebral, enxaquecas , problemas de equilíbrio, fraqueza nas pernas, marcha desajeitada, paralisia facial, problemas de bexiga, vertigem e dor nas costas. Em casos raros, a doença de Lyme não tratada pode causar psicose franca , que foi diagnosticada erroneamente como esquizofrenia ou transtorno bipolar . Podem ocorrer ataques de pânico e ansiedade; também, comportamento delirante pode ser visto, incluindo delírios somatoformes , às vezes acompanhados por uma síndrome de despersonalização ou desrealização, onde as pessoas começam a se sentir desligadas de si mesmas ou da realidade.
A acrodermatite crônica atrófica (ACA) é uma doença crônica da pele observada principalmente na Europa entre os idosos. ACA começa como uma mancha azul-avermelhada de pele descolorida, geralmente no dorso das mãos ou pés. A lesão atrofia lentamente ao longo de várias semanas ou meses, com a pele tornando-se primeiro fina e enrugada e depois, se não for tratada, completamente seca e sem pelos.
Causa


A doença de Lyme é causada por espiroquetas , bactérias espirais do gênero Borrelia . As espiroquetas são circundadas por peptidoglicanos e flagelos , juntamente com uma membrana externa semelhante às bactérias Gram-negativas. Por causa de seu envelope de membrana dupla, as bactérias Borrelia são frequentemente erroneamente descritas como Gram negativas, apesar das diferenças consideráveis em seus componentes de envelope das bactérias Gram-negativas. As espécies de Borrelia relacionadas a Lyme são conhecidas coletivamente como Borrelia burgdorferi sensu lato e apresentam uma grande diversidade genética .
B. burgdorferi sensu lato é um complexo de espécies composto por 20 genoespécies aceitas e três propostas. Oito espécies são conhecidas por causar a doença de Lyme: B. mayonii (encontrada na América do Norte), B. burgdorferi sensu stricto , B. bissettiae (ambas encontradas na América do Norte e Europa), B. afzelii , B. garinii, B. spielmanii, e B. lusitaniae (todos encontrados na Eurásia ). Alguns estudos também propuseram que B. valaisiana às vezes pode infectar humanos, mas essa espécie não parece ser uma causa importante de doença.
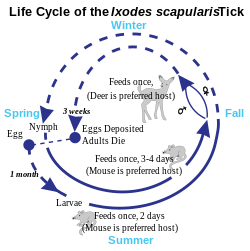
Ciclo de vida do carrapato
Existem três estágios no ciclo de vida de um carrapato. Larva, ninfa e adulto. Durante o estágio de ninfa, os carrapatos transmitem com mais frequência a doença de Lyme e costumam ser mais ativos no final da primavera e no início do verão em regiões onde o clima é ameno. Durante a fase adulta, a transmissão da doença de Lyme é menos comum devido ao fato de que é menos possível para os carrapatos adultos picarem humanos e porque eles tendem a ser maiores em tamanho e, portanto, podem ser facilmente vistos e removidos.
Transmissão
A doença de Lyme é classificada como uma zoonose , pois é transmitida aos humanos a partir de um reservatório natural entre pequenos mamíferos e pássaros por carrapatos que se alimentam de ambos os conjuntos de hospedeiros . Carrapatos de corpo duro do gênero Ixodes são os vetores da doença de Lyme (também o vetor da Babesia ). A maioria das infecções é causada por carrapatos na fase ninfal , porque eles são muito pequenos e, portanto, podem se alimentar por longos períodos sem serem detectados. Os carrapatos das ninfas geralmente têm o tamanho de uma semente de papoula e, às vezes, têm a cabeça escura e o corpo translúcido. Ou os carrapatos das ninfas podem ser mais escuros. (Os carrapatos larvais mais jovens são muito raramente infectados.) Embora os veados sejam os hospedeiros preferidos dos carrapatos adultos e as populações de carrapatos sejam muito mais baixas na ausência de veados, os carrapatos geralmente não adquirem Borrelia do veado, em vez disso, eles os obtêm de pequenos carrapatos infectados mamíferos como o camundongo de pés brancos e , ocasionalmente, pássaros. As áreas onde Lyme é comum estão se expandindo.
Dentro do intestino médio carrapato, a Borrelia ' s de proteína de superfície externa (OspA) se liga ao receptor carrapato para OspA, conhecido como TROSPA. Quando o carrapato se alimenta, a Borrelia diminui a regulação da OspA e aumenta a OspC, outra proteína de superfície. Depois que as bactérias migram do intestino médio para as glândulas salivares, o OspC se liga à Salp15, uma proteína salivar do carrapato que parece ter efeitos imunossupressores que aumentam a infecção. A infecção bem-sucedida do hospedeiro mamífero depende da expressão bacteriana de OspC.
Picadas de carrapatos muitas vezes passam despercebidas por causa do pequeno tamanho do carrapato em seu estágio ninfal, bem como secreções de carrapatos que impedem o hospedeiro de sentir coceira ou dor da picada. No entanto, a transmissão é bastante rara, com apenas cerca de 1,2 a 1,4 por cento das picadas de carrapatos reconhecidas resultando na doença de Lyme.
Na Europa, o principal vetor é o Ixodes ricinus , também chamado de carrapato da ovelha ou da mamona . Na China, Ixodes persulcatus (o carrapato da taiga) é provavelmente o vetor mais importante. Na América do Norte, o carrapato de patas pretas ou carrapato de cervo ( Ixodes scapularis ) é o principal vetor na costa leste.
É improvável que o carrapato estrela solitário ( Amblyomma americanum ), que é encontrado em todo o sudeste dos Estados Unidos até o Texas , transmita a doença de Lyme espiroquetas , embora possa estar implicada em uma síndrome relacionada chamada doença exantema associada ao carrapato do sul , que assemelha-se a uma forma branda da doença de Lyme.
Na costa oeste dos Estados Unidos , o principal vetor é o carrapato de patas pretas ( Ixodes pacificus ). A tendência dessa espécie de carrapato de se alimentar predominantemente de espécies hospedeiras, como o lagarto de vedação ocidental, que são resistentes à infecção por Borrelia , parece diminuir a transmissão da doença de Lyme no oeste.
A transmissão pode ocorrer através da placenta durante a gravidez e, como com uma série de outras doenças espiroquetas, resultados adversos da gravidez são possíveis com infecção não tratada; o tratamento imediato com antibióticos reduz ou elimina esse risco.
Não há evidências científicas para apoiar a transmissão da doença de Lyme por meio de transfusão de sangue, contato sexual ou leite materno.
Coinfecções transmitidas por carrapatos
Carrapatos que transmitem B. burgdorferi para humanos também podem carregar e transmitir vários outros parasitas, como Babesia microti e Anaplasma phagocytophilum , que causam as doenças babesiose e anaplasmose granulocítica humana (HGA), respectivamente. Entre as pessoas com doença de Lyme inicial, dependendo de sua localização, 2–12% também terão HGA e 2–40% terão babesiose. Os carrapatos em certas regiões, incluindo as terras ao longo do Mar Báltico oriental, também transmitem vírus que causam encefalite transmitida por carrapatos .
As coinfecções complicam os sintomas de Lyme, especialmente o diagnóstico e o tratamento. É possível que um carrapato carregue e transmita uma das coinfecções e não a Borrelia , tornando o diagnóstico difícil e muitas vezes indescritível. Os Centros de Controle e Prevenção de Doenças estudaram 100 carrapatos na zona rural de Nova Jersey e descobriram que 55% dos carrapatos estavam infectados com pelo menos um dos patógenos.
Fisiopatologia
B. burgdorferi pode se espalhar por todo o corpo durante o curso da doença e foi encontrada na pele, coração, articulações, sistema nervoso periférico e sistema nervoso central. Muitos dos sinais e sintomas da doença de Lyme são uma consequência da resposta imune à espiroqueta nesses tecidos.
B. burgdorferi é injetado na pele pela picada de um carrapato Ixodes infectado . A saliva do carrapato, que acompanha a espiroqueta na pele durante o processo de alimentação, contém substâncias que interrompem a resposta imunológica no local da picada. Isso fornece um ambiente protetor onde a espiroqueta pode estabelecer infecção. Os espiroquetas se multiplicam e migram para fora da derme . A resposta inflamatória do hospedeiro às bactérias na pele causa a característica lesão EM circular. Os neutrófilos , entretanto, que são necessários para eliminar os espiroquetas da pele, não aparecem em números necessários na lesão EM em desenvolvimento porque a saliva do carrapato inibe a função dos neutrófilos. Isso permite que a bactéria sobreviva e, eventualmente, se espalhe por todo o corpo.
Dias ou semanas após a picada do carrapato, as espiroquetas se espalham pela corrente sanguínea para as articulações, coração, sistema nervoso e locais distantes da pele, onde sua presença dá origem a uma variedade de sintomas da doença disseminada. A propagação de B. burgdorferi é auxiliada pela fixação da protease plasmina do hospedeiro à superfície do espiroqueta.
Se não for tratada, a bactéria pode persistir no corpo por meses ou até anos, apesar da produção de anticorpos B. burgdorferi pelo sistema imunológico. As espiroquetas podem evitar a resposta imune, diminuindo a expressão de proteínas de superfície que são direcionadas por anticorpos, variação antigênica da proteína de superfície VlsE, inativando componentes imunes chave, como complemento , e escondendo-se na matriz extracelular , o que pode interferir na função do sistema imunológico fatores.
No cérebro, B. burgdorferi pode induzir os astrócitos a sofrer astrogliose (proliferação seguida de apoptose ), o que pode contribuir para a neurodisfunção. As espiroquetas também podem induzir as células hospedeiras a secretar ácido quinolínico , que estimula o receptor NMDA nas células nervosas, o que pode ser responsável pela fadiga e mal-estar observados na encefalopatia de Lyme . Além disso, a patologia difusa da substância branca durante a encefalopatia de Lyme pode interromper as conexões da substância cinzenta e pode ser responsável por déficits de atenção, memória, capacidade visuoespacial, cognição complexa e estado emocional. A doença da substância branca pode ter um potencial maior de recuperação do que a doença da substância cinzenta, talvez porque a perda neuronal seja menos comum. Foi observada resolução das hiperintensidades da substância branca na RM após o tratamento com antibióticos.
O triptofano , um precursor da serotonina , parece estar reduzido no sistema nervoso central em uma série de doenças infecciosas que afetam o cérebro, incluindo Lyme. Os pesquisadores estão investigando se esta secreção de neuro-hormônios é a causa de distúrbios neuropsiquiátricos que se desenvolvem em algumas pessoas com borreliose.
Estudos imunológicos
A exposição à bactéria Borrelia durante a doença de Lyme possivelmente causa uma resposta inflamatória prejudicial e duradoura , uma forma de doença autoimune induzida por patógenos . A produção dessa reação pode ser devido a uma forma de mimetismo molecular , em que Borrelia evita ser morta pelo sistema imunológico por se assemelhar a partes normais dos tecidos do corpo.
Os sintomas crônicos de uma reação auto-imune podem explicar por que alguns sintomas persistem mesmo depois que as espiroquetas foram eliminadas do corpo. Essa hipótese pode explicar por que a artrite crônica persiste após a antibioticoterapia, semelhante à febre reumática , mas sua aplicação mais ampla é controversa.
Diagnóstico
A doença de Lyme é diagnosticada com base nos sintomas, achados físicos objetivos (como erupção cutânea com eritema migrans (EM), paralisia facial ou artrite ), história de possível exposição a carrapatos infectados e, possivelmente , exames laboratoriais . Pessoas com sintomas iniciais da doença de Lyme devem fazer um exame de pele de corpo inteiro para erupções EM e perguntar se as erupções do tipo EM se manifestaram nos últimos 1–2 meses. A presença de erupção cutânea EM e exposição recente a carrapatos (ou seja, estar ao ar livre em um provável habitat de carrapatos onde Lyme é comum , dentro de 30 dias do aparecimento da erupção) são suficientes para o diagnóstico de Lyme; nenhuma confirmação laboratorial é necessária ou recomendada. A maioria das pessoas infectadas não se lembra de um carrapato ou de uma mordida, e a erupção EM não precisa se parecer com um olho de boi (a maioria das erupções EM nos Estados Unidos não tem) ou ser acompanhada por quaisquer outros sintomas. Nos Estados Unidos, Lyme é mais comum nos estados da Nova Inglaterra e do Meio-Atlântico e em partes de Wisconsin e Minnesota , mas está se expandindo para outras áreas. Várias áreas fronteiriças do Canadá também apresentam alto risco de Lyme.
Na ausência de erupção cutânea EM ou história de exposição a carrapatos, o diagnóstico de Lyme depende da confirmação laboratorial. As bactérias que causam a doença de Lyme são difíceis de observar diretamente nos tecidos do corpo e também difíceis e demoradas de crescer em laboratório. Os testes mais usados procuram, em vez disso, a presença de anticorpos contra essas bactérias no sangue. Um resultado positivo no teste de anticorpos não prova por si só uma infecção ativa, mas pode confirmar uma infecção suspeita por causa dos sintomas, achados objetivos e histórico de exposição a carrapatos em uma pessoa. Como de 5 a 20% da população normal tem anticorpos contra Lyme, as pessoas sem história e sintomas sugestivos da doença de Lyme não devem ser testadas para anticorpos de Lyme: um resultado positivo provavelmente seria falso, possivelmente causando tratamento desnecessário.
Em alguns casos, quando a história, os sinais e os sintomas são fortemente sugestivos de doença de Lyme disseminada precoce, o tratamento empírico pode ser iniciado e reavaliado conforme os resultados dos exames laboratoriais se tornem disponíveis.
Testando em laboratório "ou" Teste experimental
Testes de anticorpos no sangue por ELISA e Western blot são o método mais amplamente usado para o diagnóstico de Lyme. Um protocolo de duas camadas é recomendado pelos Centros de Controle e Prevenção de Doenças (CDC): o teste ELISA sensível é realizado primeiro e, se for positivo ou duvidoso, o Western blot mais específico é executado. O sistema imunológico leva algum tempo para produzir anticorpos em quantidade. Após o início da infecção de Lyme, os anticorpos dos tipos IgM e IgG geralmente podem ser detectados pela primeira vez, respectivamente, em 2-4 semanas e 4-6 semanas, e atingem o pico em 6-8 semanas. Quando uma erupção EM aparece pela primeira vez, os anticorpos detectáveis podem não estar presentes. Portanto, é recomendado que o teste não seja realizado e o diagnóstico seja baseado na presença de erupção cutânea EM. Até 30 dias após o início da suspeita de infecção de Lyme, a infecção pode ser confirmada pela detecção de anticorpos IgM ou IgG; depois disso, recomenda-se que sejam considerados apenas anticorpos IgG. Um resultado de teste de IgM positivo e negativo após o primeiro mês de infecção é geralmente indicativo de um resultado falso-positivo. O número de anticorpos IgM geralmente entra em colapso 4-6 meses após a infecção, enquanto os anticorpos IgG podem permanecer detectáveis por anos.
Outros testes podem ser usados em casos de neuroborreliose. Na Europa, a neuroborreliose é geralmente causada por Borrelia garinii e quase sempre envolve pleocitose linfocítica , ou seja, as densidades de linfócitos (células que combatem a infecção) e proteínas no líquido cefalorraquidiano (LCR) normalmente aumentam para níveis caracteristicamente anormais, enquanto o nível de glicose permanece normal. Além disso, o sistema imunológico produz anticorpos contra Lyme dentro do espaço intratecal, que contém o LCR. A demonstração por punção lombar e análise do LCR de pleocitose e produção de anticorpos intratecais são necessárias para o diagnóstico definitivo de neuroborreliose na Europa (exceto em casos de neuropatia periférica associada a acrodermatite crônica atrófica , que geralmente é causada por Borrelia afzelii e confirmada por testes de anticorpos no sangue). Na América do Norte, a neuroborreliose é causada por Borrelia burgdorferi e pode não ser acompanhada pelos mesmos sinais do LCR; eles confirmam o diagnóstico de neuroborreliose do sistema nervoso central (SNC) se positivo, mas não o excluem se negativo. As diretrizes americanas consideram a análise do LCR opcional quando os sintomas parecem estar confinados ao sistema nervoso periférico (SNP), por exemplo, paralisia facial sem sintomas evidentes de meningite. Ao contrário dos testes de sangue e anticorpos intratecais, os testes de pleocitose do LCR voltam ao normal após o término da infecção e, portanto, podem ser usados como marcadores objetivos do sucesso do tratamento e informar as decisões sobre recuar. Na infecção envolvendo o SNP, os estudos de eletromiografia e de condução nervosa podem ser usados para monitorar objetivamente a resposta ao tratamento.
Na cardite de Lyme, os eletrocardiogramas são usados para evidenciar anormalidades da condução cardíaca, enquanto a ecocardiografia pode mostrar disfunção miocárdica . A biópsia e a confirmação das células de Borrelia no tecido miocárdico podem ser usadas em casos específicos, mas geralmente não são feitas devido ao risco do procedimento.
Os testes de reação em cadeia da polimerase (PCR) para a doença de Lyme também foram desenvolvidos para detectar o material genético ( DNA ) da espiroqueta da doença de Lyme. A cultura ou PCR são os meios atuais para detectar a presença do organismo, pois os estudos sorológicos apenas testam os anticorpos de Borrelia . O PCR tem a vantagem de ser muito mais rápido do que a cultura. No entanto, os testes de PCR são suscetíveis a resultados falsos positivos , por exemplo, pela detecção de resíduos de células de Borrelia mortas ou contaminação de amostras. Mesmo quando realizada de maneira adequada, a PCR geralmente mostra resultados falso-negativos porque poucas células de Borrelia podem ser encontradas no sangue e no líquido cefalorraquidiano (LCR) durante a infecção. Portanto, os testes de PCR são recomendados apenas em casos especiais, por exemplo, diagnóstico de artrite de Lyme, porque é uma forma altamente sensível de detecção de DNA de ospA no líquido sinovial. Embora a sensibilidade da PCR no LCR seja baixa, seu uso pode ser considerado quando houver suspeita de que os resultados do teste de produção de anticorpos intratecal sejam falsamente negativos, por exemplo, em neuroborreliose muito precoce (<6 semanas) ou em pessoas imunossuprimidas .
Várias outras formas de testes laboratoriais para a doença de Lyme estão disponíveis, algumas das quais não foram devidamente validadas. Os antígenos OspA , eliminados pela bactéria Borrelia na urina, são uma técnica promissora em estudo. O uso de partículas de nanotrap para sua detecção está sendo analisado e o OspA foi associado a sintomas ativos de Lyme. Altos títulos de anticorpos imunoglobulina G (IgG) ou imunoglobulina M (IgM) para antígenos Borrelia indicam doença, mas títulos mais baixos podem ser enganosos, porque os anticorpos IgM podem permanecer após a infecção inicial e os anticorpos IgG podem permanecer por anos.
O CDC não recomenda testes de antígeno de urina, testes de PCR em urina, coloração imunofluorescente para formas deficientes de parede celular de B. burgdorferi e testes de transformação de linfócitos.
Imaging
A neuroimagem é controversa quanto ao fato de fornecer padrões específicos exclusivos da neuroborreliose , mas pode auxiliar no diagnóstico diferencial e na compreensão da fisiopatologia da doença. Embora controversas, algumas evidências mostram que certos testes de neuroimagem podem fornecer dados úteis no diagnóstico de uma pessoa. A ressonância magnética (MRI) e a tomografia computadorizada por emissão de fóton único (SPECT) são dois dos exames que podem identificar anormalidades no cérebro de uma pessoa afetada por esta doença. Os achados de neuroimagem em uma ressonância magnética incluem lesões na substância branca periventricular, bem como ventrículos aumentados e atrofia cortical. Os resultados são considerados pouco excepcionais porque as lesões foram consideradas reversíveis após o tratamento com antibióticos. Imagens produzidas com SPECT mostram várias áreas onde uma quantidade insuficiente de sangue está sendo enviada ao córtex e à substância branca subcortical. No entanto, as imagens SPECT são reconhecidamente inespecíficas porque mostram um padrão heterogêneo na imagem. As anormalidades vistas nas imagens SPECT são muito semelhantes às observadas em pessoas com vacuidades cerebrais e doença de Creutzfeldt-Jakob , o que as torna questionáveis.
Diagnóstico diferencial
Foi relatado que as clínicas comunitárias diagnosticaram erroneamente 23–28% das erupções cutâneas com eritema migrans (EM) e 83% de outras manifestações objetivas da doença de Lyme inicial. Erupções cutâneas EM são frequentemente diagnosticadas como picadas de aranha , celulite ou herpes zoster . Muitos diagnósticos errados são creditados ao conceito errôneo generalizado de que as erupções EM devem se parecer com um alvo. Na verdade, as principais características distintivas da erupção EM são a velocidade e a extensão em que ela se expande, respectivamente até 2–3 cm / dia e um diâmetro de pelo menos 5 cm, e em 50% dos casos mais de 16 cm. A erupção se expande para longe de seu centro, que pode ou não ter uma aparência diferente ou estar separada do restante da erupção por uma limpeza em forma de anel. Em comparação com erupções cutâneas EM, as picadas de aranha são mais comuns nos membros, tendem a ser mais dolorosas e coceira ou inchaço, e algumas podem causar necrose (mancha azul escura afundando na pele morta). A celulite se desenvolve mais comumente ao redor de uma ferida ou úlcera, raramente é circular e tem maior probabilidade de se tornar inchada e sensível. Erupções cutâneas EM costumam aparecer em locais incomuns para celulite, como axila, virilha, abdômen ou parte de trás do joelho. Como Lyme, o herpes geralmente começa com dor de cabeça, febre e fadiga, seguidos de dor ou dormência. No entanto, ao contrário de Lyme, no herpes zoster, esses sintomas são geralmente seguidos pelo aparecimento de erupções cutâneas compostas por várias pequenas bolhas junto com o dermátomo de um nervo , e o herpes também pode ser confirmado por testes laboratoriais rápidos.
A paralisia facial causada pela doença de Lyme (LDFP) é freqüentemente diagnosticada como paralisia de Bell . Embora a paralisia de Bell seja o tipo mais comum de paralisia facial unilateral (cerca de 70% dos casos), o LDFP pode ser responsável por cerca de 25% dos casos de paralisia facial em áreas onde a doença de Lyme é comum. Em comparação com o LDFP, a paralisia de Bell afeta com muito menos frequência os dois lados do rosto. Embora o LDFP e a paralisia de Bell tenham sintomas semelhantes e evoluam de forma semelhante se não forem tratados, o tratamento com corticosteroides é benéfico para a paralisia de Bell, embora seja prejudicial para o LDFP. A história recente de exposição a um provável habitat de carrapato durante os meses mais quentes, erupção cutânea EM, sintomas semelhantes a vírus, como dor de cabeça e febre e / ou paralisia em ambos os lados da face, devem ser avaliados quanto à probabilidade de LDFP; se for maior que o mínimo, deve-se iniciar a terapia empírica com antibióticos, sem corticosteroides, e reavaliada após a conclusão dos exames laboratoriais para doença de Lyme.
Ao contrário da meningite viral , a meningite linfocítica de Lyme tende a não causar febre, durar mais e recorrer. A meningite linfocítica também é caracterizada por possivelmente co-ocorrendo com erupção cutânea EM , paralisia facial ou obstrução parcial da visão e tendo uma porcentagem muito menor de leucócitos polimorfonucleares no LCR .
A radiculopatia de Lyme que afeta os membros costuma ser diagnosticada erroneamente como uma radiculopatia causada pela compressão da raiz do nervo, como a ciática . Embora a maioria dos casos de radiculopatia sejam compressivos e resolvidos com tratamento conservador (por exemplo, repouso) dentro de 4-6 semanas, as diretrizes para o tratamento da radiculopatia recomendam primeiro avaliar os riscos de outras causas possíveis que, embora menos frequentes, requerem diagnóstico e tratamento imediato, incluindo infecções como como Lyme e telhas. Uma história de atividades ao ar livre em prováveis habitats de carrapatos nos últimos 3 meses, possivelmente seguida por uma erupção cutânea ou sintomas semelhantes aos virais e dor de cabeça atual, outros sintomas de meningite linfocítica ou paralisia facial levaria à suspeita de doença de Lyme e recomendação de exames sorológicos e testes de punção lombar para confirmação.
A radiculopatia de Lyme que afeta o tronco pode ser diagnosticada erroneamente como uma miríade de outras condições, como diverticulite e síndrome coronariana aguda . O diagnóstico da doença de Lyme em estágio avançado costuma ser complicado por uma aparência multifacetada e sintomas inespecíficos, levando um revisor a chamar Lyme de novo "grande imitador". A doença de Lyme pode ser diagnosticada erroneamente como esclerose múltipla , artrite reumatóide , fibromialgia , síndrome da fadiga crônica , lúpus , doença de Crohn , HIV ou outras doenças autoimunes e neurodegenerativas . Como todas as pessoas com infecção em estágio avançado terão um teste de anticorpos positivo, exames de sangue simples podem excluir a doença de Lyme como uma possível causa dos sintomas de uma pessoa.
Prevenção
Picadas de carrapatos podem ser evitadas evitando ou reduzindo o tempo em habitats prováveis de carrapatos e tomando precauções ao entrar e sair de um deles.
A maioria das infecções humanas de Lyme são causadas por picadas de ninfas Ixodes entre abril e setembro. Os carrapatos preferem locais úmidos e sombreados em florestas , arbustos, gramíneas altas e serapilheira ou pilhas de madeira. A densidade de carrapatos tende a ser mais alta em bosques, seguidos por bordas sem manutenção entre bosques e gramados (cerca de metade da altura), plantas ornamentais e cobertura do solo perene (cerca de um quarto) e gramados (cerca de 30 vezes menos). As larvas e ninfas ixodes tendem a ser abundantes também onde os ratos fazem ninhos, como paredes de pedra e toras de madeira. As larvas e ninfas ixodes normalmente esperam por hospedeiros potenciais ("busca") nas folhas ou gramíneas próximas ao solo com as patas dianteiras estendidas; quando um hospedeiro roça seus membros, o carrapato rapidamente se agarra e sobe no hospedeiro procurando um local de pele para morder. No nordeste dos Estados Unidos, estima-se que 69% das picadas de carrapatos ocorram em residências, 11% em escolas ou acampamentos, 9% em parques ou áreas de lazer, 4% no trabalho, 3% durante a caça e 4% em outras áreas. As atividades associadas a picadas de carrapatos em residências incluem jardinagem, limpeza de mato, jardinagem, brincar no quintal e deixar entrar cães ou gatos que vagam do lado de fora em áreas arborizadas ou gramadas. Nos parques, picadas de carrapatos costumam acontecer durante caminhadas ou acampamentos. Andar em um gramado aparado ou no centro de uma trilha sem tocar na vegetação adjacente é menos arriscado do que rastejar ou sentar em um tronco ou parede de pedra. Os animais de estimação não devem circular livremente em habitats prováveis de carrapatos.
Como precaução, o CDC recomenda molhar ou borrifar roupas, sapatos e equipamentos de acampamento, como barracas, mochilas e sacos de dormir com solução de permetrina a 0,5% e pendurá-los para secar antes do uso. A permetrina é inodora e segura para os humanos, mas altamente tóxica para os carrapatos. Depois de rastejar em tecido tratado com permetrina por apenas 10 a 20 segundos, as ninfas do carrapato ficam irritadas e caem ou morrem. Sapatos e meias fechados tratados com permetrina reduzem em 74 vezes o número de mordidas de ninfas que fazem o primeiro contato com um sapato de uma pessoa que também usa shorts tratados (porque as ninfas geralmente procuram perto do chão, este é um cenário de contato típico). Melhor proteção pode ser obtida enfiando calças tratadas com permetrina (calças) em meias tratadas e uma camisa de manga longa tratada nas calças de modo a minimizar as lacunas através das quais um carrapato pode atingir a pele do usuário. Roupas de cores claras podem facilitar a visualização dos carrapatos e removê-los antes que mordam. Descobriu-se que os uniformes dos trabalhadores militares e ao ar livre tratados com permetrina reduzem o número de casos de mordidas em 80-95%. A proteção com permetrina dura várias semanas de uso e lavagens em itens tratados pelo cliente e até 70 lavagens em itens tratados na fábrica. A permetrina não deve ser usada na pele humana, roupas íntimas ou gatos.
A EPA recomenda vários repelentes de carrapatos para uso na pele exposta, incluindo DEET , picaridina , IR3535 (um derivado do aminoácido beta-alanina), óleo de eucalipto limão (OLE, um composto natural) e ingrediente ativo de OLE para-mentano-diol ( PMD) . Ao contrário da permetrina, os repelentes repelem, mas não matam os carrapatos, protegem por apenas algumas horas após a aplicação e podem ser eliminados pelo suor ou água. O repelente mais popular é o DEET nos Estados Unidos e a picaridina na Europa. Ao contrário do DEET, a picaridina é inodora e tem menos probabilidade de irritar a pele ou prejudicar tecidos ou plásticos. Repelentes com concentração mais alta podem durar mais, mas não são mais eficazes; contra carrapatos, 20% de picaridina pode funcionar por 8 horas vs. 55–98,11% DEET por 5–6 horas ou 30–40% OLE por 6 horas. Os repelentes não devem ser usados sob as roupas, nos olhos, boca, feridas ou cortes, ou em bebês com menos de 2 meses (3 anos para OLE ou PMD). Se for usado protetor solar , deve-se aplicar repelente por cima. Os repelentes não devem ser borrifados diretamente no rosto, mas sim nas mãos e depois esfregados no rosto.
Depois de entrar em casa, roupas, equipamentos e animais de estimação devem ser verificados quanto a carrapatos. As roupas podem ser colocadas em uma secadora quente por 10 minutos para matar os carrapatos (apenas lavar ou secar quente não é suficiente). Tomar banho o mais rápido possível, procurar carrapatos por todo o corpo e removê-los reduz o risco de infecção. As ninfas de carrapatos não alimentadas são do tamanho de uma semente de papoula, mas um ou dois dias depois de morder e se prender a uma pessoa, elas parecem uma pequena bolha de sangue . As seguintes áreas devem ser verificadas com especial cuidado: axilas, entre as pernas, parte posterior do joelho, umbigo, tronco e, nas crianças, orelhas, pescoço e cabelo.
Remoção de carrapatos
Os carrapatos anexados devem ser removidos imediatamente. O risco de infecção aumenta com o tempo de fixação, mas na América do Norte o risco de doença de Lyme é pequeno se o carrapato for removido em 36 horas. O CDC recomenda inserir uma pinça de ponta fina entre a pele e o carrapato, segurando com muita firmeza e puxando a pinça fechada imediatamente para longe da pele, sem torcer, empurrar, espremer ou esmagar o carrapato. Após a remoção do carrapato, todas as partes do carrapato que permanecerem na pele devem ser removidas com uma pinça limpa, se possível. A ferida e as mãos devem ser limpas com álcool ou água e sabão. O carrapato pode ser eliminado colocando-o em um recipiente com álcool, saco lacrado, fita adesiva ou descarregado no vaso sanitário. A pessoa picada deve anotar onde e quando a picada aconteceu, para que possa ser informada a um médico se a pessoa tiver uma erupção ou sintomas semelhantes aos da gripe nas semanas seguintes. O CDC recomenda não usar os dedos, esmalte de unha, vaselina ou calor no carrapato para tentar removê-lo.
Na Austrália, onde o carrapato da paralisia australiana é prevalente, a Sociedade Australasiana de Imunologia Clínica e Alergia recomenda não usar pinças para remover os carrapatos, porque se a pessoa for alérgica, pode ocorrer anafilaxia . Em vez disso, um produto deve ser pulverizado no carrapato para fazer com que ele congele e depois caia. Um médico usaria nitrogênio líquido, mas produtos disponíveis em farmácias para verrugas congelantes podem ser usados em seu lugar. Outro método originário da Austrália consiste em usar cerca de 20 cm de fio dental ou linha de pesca para dar um nó por cima lentamente entre a pele e o carrapato e, em seguida, puxá-lo para longe da pele.
Antibióticos preventivos
O risco de transmissão infecciosa aumenta com a duração da fixação do carrapato. Requer entre 36 e 48 horas de fixação para a bactéria que faz com que Lyme se desloque de dentro do carrapato para a saliva. Se um carrapato de cervo com probabilidade suficiente de portar Borrelia for encontrado preso a uma pessoa e removido, e se o carrapato tiver ficado preso por 36 horas ou estiver ingurgitado, uma única dose de doxiciclina administrada nas 72 horas após a remoção pode reduzir o risco de doença de Lyme. Geralmente não é recomendado para todas as pessoas picadas, pois o desenvolvimento de infecção é raro: cerca de 50 pessoas picadas teriam que ser tratadas desta forma para prevenir um caso de eritema migratório (ou seja, a erupção cutânea típica encontrada em cerca de 70-80% das pessoas infectadas )
Paisagismo de jardim
Diversas práticas de paisagismo podem reduzir o risco de picadas de carrapatos em pátios residenciais. O gramado deve ser mantido aparado, o lixo das folhas e as ervas daninhas removidos e o uso da cobertura do solo evitado. Bosques , arbustos, paredes de pedra e pilhas de madeira devem ser separados do gramado por uma barreira de pedra ou lascas de madeira de 3 pés de largura. Sem vegetação na barreira, os carrapatos tenderão a não cruzá-la; acaricidas também podem ser borrifados para matar os carrapatos. Uma zona protegida contra carrapatos exposta ao sol a pelo menos 9 pés da barreira deve concentrar a atividade humana no quintal, incluindo pátios, playgrounds e jardinagem. Materiais como deck de madeira, concreto, tijolos, cascalho ou lascas de madeira podem ser usados no solo sob pátios e playgrounds para desencorajar carrapatos. Uma cerca de 8 pés de altura pode ser adicionada para manter os cervos longe da zona de segurança contra carrapatos.
Exposição profissional
Trabalhadores ao ar livre correm o risco de contrair a doença de Lyme se trabalharem em locais com carrapatos infectados. Isso inclui construção, paisagismo, silvicultura, limpeza de mato, levantamento topográfico, agricultura, trabalho em ferrovia, trabalho em campo petrolífero, trabalho em linha de serviços públicos, gestão de parque ou vida selvagem. Trabalhadores americanos nos estados do nordeste e centro-norte correm o maior risco de exposição a carrapatos infectados. Os carrapatos também podem transmitir outras doenças transmitidas por carrapatos aos trabalhadores dessas e de outras regiões do país. Os locais de trabalho com bosques, arbustos, grama alta ou serapilheira tendem a ter mais carrapatos. Os trabalhadores que trabalham ao ar livre devem ter muito cuidado para se proteger no final da primavera e no verão, quando os carrapatos jovens são mais ativos.
Animais hospedeiros
Lyme e outras doenças transmitidas por carrapatos de veado às vezes podem ser reduzidas reduzindo significativamente a população de veados da qual os carrapatos adultos dependem para alimentação e reprodução. Os casos da doença de Lyme diminuíram após a erradicação de cervos em uma ilha, Monhegan, Maine , e após o controle de cervos em Mumford Cove, Connecticut. É importante notar que a eliminação de veados pode levar a um aumento temporário na densidade do carrapato.
Por exemplo, nos EUA, reduzir a população de veados para níveis de 8 a 10 por milha quadrada (dos níveis atuais de 60 ou mais veados por milha quadrada nas áreas do país com as maiores taxas de doença de Lyme) pode reduzir o número de carrapatos e reduzir a propagação de Lyme e outras doenças transmitidas por carrapatos. No entanto, essa redução drástica pode ser muito difícil de implementar em muitas áreas, e densidades baixas a moderadas de veados ou outros grandes mamíferos hospedeiros podem continuar a alimentar carrapatos adultos suficientes para manter a densidade larval em níveis elevados. O controle veterinário de rotina de carrapatos de animais domésticos , incluindo gado, pelo uso de acaricidas pode contribuir para reduzir a exposição de humanos aos carrapatos.
Na Europa, os reservatórios conhecidos de Borrelia burgdorferi foram 9 pequenos mamíferos, 7 mamíferos de médio porte e 16 espécies de pássaros (incluindo passeriformes, aves marinhas e faisões). Esses animais parecem transmitir espiroquetas aos carrapatos e, portanto, participam da circulação natural de B. burgdorferi na Europa. O rato doméstico também é suspeito, assim como outras espécies de pequenos roedores, principalmente na Europa Oriental e na Rússia. "As espécies de reservatório que contêm mais patógenos são o veado europeu Capreolus capreolus ;" ele não parece servir como um grande reservatório de B. burgdorferi ", pensou Jaenson & al. (1992) (hospedeiro incompetente para B. burgdorferi e TBE vírus), mas é importante para a alimentação de carrapatos, como veados e javalis ( Sus scrofa ), nos quais foram identificadas uma Rickettsia e três espécies de Borrelia ", com alto risco de coinfecção em veados. No entanto, na década de 2000, em veados na Europa " foram identificadas duas espécies de Rickettsia e duas espécies de Borrelia ".
Vacinação
Uma vacina recombinante contra a doença de Lyme, baseada na proteína A da superfície externa (ospA) de B. burgdorferi , foi desenvolvida por SmithKline Beecham . Em ensaios clínicos envolvendo mais de 10.000 pessoas, a vacina, denominada LYMErix, conferiu imunidade protetora à Borrelia em 76% dos adultos e 100% das crianças, com apenas efeitos adversos ligeiros ou moderados e transitórios . O LYMErix foi aprovado com base nesses testes pela Food and Drug Administration (FDA) em 21 de dezembro de 1998.
Após a aprovação da vacina , sua entrada na prática clínica foi lenta por uma série de razões, incluindo seu custo, que muitas vezes não era reembolsado pelas seguradoras. Posteriormente, centenas de vacinados relataram que desenvolveram efeitos autoimunes e outros efeitos colaterais. Apoiado por alguns grupos de defesa, uma série de ações judiciais coletivas foram movidas contra a GlaxoSmithKline , alegando que a vacina havia causado esses problemas de saúde. Essas alegações foram investigadas pelo FDA e pelos Centros de Controle de Doenças, que não encontraram nenhuma conexão entre a vacina e as queixas auto-imunes.
Apesar da falta de evidências de que as reclamações foram causadas pela vacina, as vendas despencaram e o LYMErix foi retirado do mercado americano pela GlaxoSmithKline em fevereiro de 2002, em um cenário de cobertura negativa da mídia e temores dos efeitos colaterais da vacina. O destino de LYMErix foi descrito na literatura médica como um "conto de advertência"; um editorial na Nature citou a retirada do LYMErix como um exemplo no qual "temores públicos infundados colocam pressões sobre os desenvolvedores de vacinas que vão além das considerações de segurança razoáveis". O desenvolvedor original da vacina OspA no Instituto Max Planck disse à Nature : "Isso apenas mostra como o mundo pode ser irracional ... Não havia justificativa científica para a retirada da primeira vacina OspA LYMErix."
As vacinas foram formuladas e aprovadas para a prevenção da doença de Lyme em cães. Atualmente, três vacinas contra a doença de Lyme estão disponíveis. LymeVax, formulado por Fort Dodge Laboratories, contém espiroquetas mortas intactas que expõem o hospedeiro ao organismo. Galaxy Lyme, vacina da Intervet -Schering-Plough , tem como alvo as proteínas OspC e OspA . Os anticorpos OspC matam qualquer bactéria que não tenha sido morta pelos anticorpos OspA. Canine Recombinant Lyme, formulado pela Merial , gera anticorpos contra a proteína OspA, então um carrapato que se alimenta de um cão vacinado retira sangue cheio de anticorpos anti-OspA, que matam os espiroquetas no intestino do carrapato antes de serem transmitidos ao cão.
Uma vacina candidata à base de subunidade de proteína hexavalente (OspA) VLA15 desenvolvida pela Valneva recebeu a designação de via rápida da US Food and Drug Administration em 2017, o que permitirá um estudo mais aprofundado.
Tratamento
Os antibióticos são o tratamento primário. A abordagem específica para seu uso depende do indivíduo afetado e do estágio da doença. Para a maioria das pessoas com infecção localizada inicial, a administração oral de doxiciclina é amplamente recomendada como primeira escolha, pois é eficaz não apenas contra a bactéria Borrelia, mas também contra uma variedade de outras doenças transmitidas por carrapatos. Pessoas que tomam doxiciclina devem evitar a exposição ao sol devido ao maior risco de queimaduras solares . A doxiciclina é contra-indicada em crianças menores de oito anos de idade e mulheres grávidas ou amamentando; as alternativas à doxiciclina são amoxicilina , cefuroxima axetil e azitromicina . A azitromicina é recomendada apenas em caso de intolerância aos outros antibióticos. O tratamento padrão para celulite , cefalexina , não é útil para a doença de Lyme. Quando não está claro se uma erupção cutânea é causada por Lyme ou celulite, a IDSA recomenda o tratamento com cefuroxima ou amoxicilina / ácido clavulânico , pois são eficazes contra ambas as infecções. Os indivíduos com infecção de Lyme disseminada precoce ou tardia podem ter doença cardíaca sintomática, artrite de Lyme ou sintomas neurológicos como paralisia facial , radiculopatia , meningite ou neuropatia periférica . A administração intravenosa de ceftriaxona é recomendada como primeira escolha nesses casos; cefotaxima e doxiciclina estão disponíveis como alternativas.
Os regimes de tratamento para a doença de Lyme variam de 14 dias na doença localizada precoce, a 14-21 dias na doença disseminada precoce a 14-28 dias na doença disseminada tardia. As complicações neurológicas da doença de Lyme podem ser tratadas com doxiciclina, pois ela pode ser administrada por via oral e tem um custo menor, embora na América do Norte as evidências de eficácia sejam apenas indiretas. Em caso de falha, as diretrizes recomendam o retratamento com ceftriaxona injetável . Vários meses após o tratamento para a artrite de Lyme, se o inchaço nas articulações persistir ou retornar, uma segunda rodada de antibióticos pode ser considerada; antibióticos intravenosos são preferidos para retratamento em caso de resposta insatisfatória aos antibióticos orais. Fora isso, um regime prolongado de antibióticos com duração de mais de 28 dias não é recomendado, pois nenhuma evidência mostra que seja eficaz. Os níveis de anticorpos IgM e IgG podem ser elevados por anos, mesmo após o tratamento bem-sucedido com antibióticos. Como os níveis de anticorpos não são indicativos de sucesso do tratamento, o teste para eles não é recomendado.
A paralisia facial pode remitir sem tratamento; no entanto, o tratamento com antibióticos é recomendado para interromper outras complicações de Lyme. Corticosteroides não são recomendados quando a paralisia facial é causada pela doença de Lyme. Em pessoas com paralisia facial, recomenda-se o uso frequente de lágrimas artificiais durante a vigília, junto com pomada e um adesivo ou selar o olho durante o sono.
Cerca de um terço das pessoas com cardite de Lyme precisam de um marcapasso temporário até que a anormalidade da condução cardíaca seja resolvida e 21% precisam ser hospitalizados. A cardite de Lyme não deve ser tratada com corticosteroides.
Pessoas com artrite de Lyme devem limitar o nível de atividade física para evitar lesões nas articulações afetadas e, em caso de claudicação, devem usar muletas. A dor associada à doença de Lyme pode ser tratada com antiinflamatórios não esteróides (AINEs). As injeções de corticosteroides nas articulações não são recomendadas para a artrite de Lyme que está sendo tratada com antibióticos. Pessoas com artrite de Lyme tratadas com antibióticos intravenosos ou dois meses de antibióticos orais que continuam a ter inchaço nas articulações dois meses após o tratamento e têm teste PCR negativo para DNA de Borrelia no líquido sinovial dizem ter artrite de Lyme refratária a antibióticos; isso é mais comum após a infecção por certas cepas de Borrelia em pessoas com certas características genéticas e imunológicas. A artrite de Lyme refratária a antibióticos pode ser tratada sintomaticamente com AINEs, medicamentos antirreumáticos modificadores da doença (DMARDs) ou sinovectomia artroscópica . A fisioterapia é recomendada para adultos após a resolução da artrite de Lyme.
As pessoas que recebem tratamento devem ser avisadas de que a reinfecção é possível e como evitá-la .
Prognóstico
O primeiro sinal típico da doença de Lyme , erupção cutânea com eritema migrans (EM), remite em várias semanas, mesmo sem tratamento. No entanto, em pessoas não tratadas, a infecção geralmente se espalha para o sistema nervoso, coração ou articulações, podendo causar danos permanentes aos tecidos do corpo.
Pessoas que recebem tratamento antibiótico recomendado dentro de alguns dias após o aparecimento de uma erupção cutânea inicial EM têm as melhores perspectivas. A recuperação pode não ser total ou imediata. A porcentagem de pessoas que alcançam a recuperação completa nos Estados Unidos aumenta de cerca de 64-71% no final do tratamento para erupção cutânea EM para cerca de 84-90% após 30 meses; percentagens mais altas são relatadas na Europa. A falha do tratamento, ou seja, persistência dos sinais originais ou aparecimento de novos sinais da doença, ocorre apenas em algumas pessoas. As pessoas restantes são consideradas curadas, mas continuam a sentir sintomas subjetivos, por exemplo, dores articulares ou musculares ou fadiga . Esses sintomas geralmente são leves e não incapacitantes.
Pessoas tratadas apenas após manifestações da doença no sistema nervoso podem acabar com déficits neurológicos objetivos, além de sintomas subjetivos. Na Europa, uma média de 32-33 meses após os sintomas iniciais de Lyme em pessoas tratadas principalmente com doxiciclina 200 mg por 14-21 dias, a porcentagem de pessoas com sintomas persistentes foi muito maior entre aqueles com diagnóstico de neuroborreliose (50%) do que entre aqueles com apenas uma erupção cutânea EM (16%). Em outro estudo europeu, 5 anos após o tratamento para neuroborreliose, os sintomas persistentes foram menos comuns em crianças (15%) do que em adultos (30%), e neste último foi menos comum entre aqueles tratados dentro de 30 dias após o primeiro sintoma (16% ) do que entre os tratados posteriormente (39%); entre aqueles com sintomas persistentes, 54% tinham atividades diárias restritas e 19% estavam em licença médica ou incapacitadas.
Alguns dados sugerem que cerca de 90% das paralisias faciais de Lyme tratadas com antibióticos se recuperam totalmente em uma média de 24 dias após o aparecimento e a maior parte do restante se recupera apenas com anormalidade leve. No entanto, na Europa, 41% das pessoas tratadas para paralisia facial apresentaram outros sintomas persistentes no acompanhamento até 6 meses depois, incluindo 28% com dormência ou sensação alterada e 14% com fadiga ou problemas de concentração . Paralisia em ambos os lados da face está associada a pior e maior tempo de recuperação. Dados históricos sugerem que pessoas não tratadas com paralisia facial se recuperam quase na mesma taxa, mas 88% subsequentemente têm artrite de Lyme. Outra pesquisa mostra que a sincinesia (movimento involuntário de um músculo facial quando outro é movido voluntariamente) pode se tornar evidente apenas 6–12 meses depois que a paralisia facial parece estar resolvida, conforme os nervos danificados voltam a crescer e às vezes se conectam a músculos incorretos. A sinquinese está associada ao uso de corticosteroides . No acompanhamento de longo prazo, 16–23% das paralisias faciais de Lyme não se recuperam totalmente.
Na Europa, cerca de um quarto das pessoas com síndrome de Bannwarth ( radiculopatia de Lyme e meningite linfocítica ) tratadas com ceftriaxona intravenosa por 14 dias, em média 30 dias após os primeiros sintomas, tiveram que ser tratadas novamente 3-6 meses depois devido a uma resposta clínica insatisfatória ou objetivo contínuo marcadores de infecção no líquido cefalorraquidiano ; após 12 meses, 64% se recuperaram totalmente, 31% apresentavam sintomas leves ou infrequentes não incapacitantes que não exigiam o uso regular de analgésicos e 5% tinham sintomas que eram incapacitantes ou exigiam o uso substancial de analgésicos. Os sintomas persistentes não incapacitantes mais comuns foram dor de cabeça, fadiga , sensação alterada , dores nas articulações , distúrbios de memória , mal-estar , dor radicular , distúrbios do sono , dores musculares e distúrbios de concentração . Os sintomas incapacitantes persistentes incluem paralisia facial e outros movimentos prejudicados .
A recuperação da neuroborreliose tardia tende a ser mais demorada e menos completa do que a da neuroborreliose inicial, provavelmente devido a danos neurológicos irreversíveis.
Cerca de metade das pessoas com cardite de Lyme evoluem para bloqueio cardíaco completo , mas geralmente remite em uma semana. Outras anormalidades de condução do coração de Lyme remitem normalmente em 6 semanas. Cerca de 94% das pessoas têm recuperação total, mas 5% precisam de um marcapasso permanente e 1% acaba com bloqueio cardíaco persistente (a porcentagem real pode ser maior devido a casos não reconhecidos). As complicações miocárdicas de Lyme geralmente são leves e autolimitadas. No entanto, em alguns casos, a cardite de Lyme pode ser fatal.
Os tratamentos com antibióticos recomendados são eficazes em cerca de 90% dos casos de artrite de Lyme, embora possa levar vários meses para que a inflamação remeta e uma segunda rodada de antibióticos seja freqüentemente necessária. A artrite de Lyme refratária a antibióticos também desaparece, geralmente em 9 a 14 meses (variação de 4 meses a 4 anos); DMARDs ou sinovectomia podem acelerar a recuperação.
A reinfecção não é incomum. Em um estudo nos EUA, 6–11% das pessoas tratadas para uma erupção EM tiveram outra erupção EM em 30 meses. A segunda erupção geralmente é causada por uma infecção por uma cepa diferente de Borrelia .
Pessoas que apresentam sintomas subjetivos inespecíficos, como fadiga, dores nas articulações e musculares, ou dificuldades cognitivas por mais de seis meses após o tratamento recomendado para a doença de Lyme, apresentam síndrome da doença de Lyme pós-tratamento (PTLDS). Em 2016, a razão para os sintomas persistentes não era conhecida; a condição é geralmente tratada de forma semelhante à fibromialgia ou síndrome da fadiga crônica .
Epidemiologia
A doença de Lyme ocorre regularmente nas regiões temperadas do hemisfério norte .
África
No norte da África, B. burgdorferi sensu lato foi identificado no Marrocos , Argélia , Egito e Tunísia .
A doença de Lyme na África Subsaariana é atualmente desconhecida, mas as evidências indicam que pode ocorrer em humanos nesta região. A abundância de hospedeiros e vetores de carrapatos favoreceria o estabelecimento da infecção de Lyme na África. Na África Oriental, dois casos da doença de Lyme foram relatados no Quênia .
Ásia
Carrapatos infestados de B. burgdorferi sensu lato estão sendo encontrados com mais freqüência no Japão, bem como no noroeste da China, Nepal , Tailândia e extremo leste da Rússia. Borrelia também foi isolada na Mongólia .
Europa
Na Europa, a doença de Lyme é causada pela infecção por uma ou mais genoespécies europeias patogênicas da espiroqueta B. burgdorferi sensu lato , transmitida principalmente pelo carrapato Ixodes ricinus . Os casos de carrapatos infectados com B. burgdorferi sensu lato são encontrados predominantemente na Europa Central, particularmente na Eslovênia e na Áustria , mas foram isolados em quase todos os países do continente. O número de casos no sul da Europa, como Itália e Portugal, é muito menor. Os casos diagnosticados em alguns países ocidentais, como a Islândia, estão aumentando.
Reino Unido
No Reino Unido, o número de casos confirmados por laboratório da doença de Lyme tem aumentado continuamente desde que a notificação voluntária foi introduzida em 1986, quando 68 casos foram registrados no Reino Unido e na República da Irlanda juntos. No Reino Unido, houve 23 casos confirmados em 1988 e 19 em 1990, mas 973 em 2009 e 953 em 2010. Os números provisórios para os primeiros 3 trimestres de 2011 mostram um aumento de 26% em relação ao mesmo período de 2010.
Pensa-se, no entanto, que o número real de casos é significativamente maior do que sugerido pelos números acima, com a Health Protection Agency do Reino Unido estimando que há entre 2.000 e 3.000 casos por ano, (com uma média de cerca de 15% dos infecções adquiridas no exterior), enquanto o Dr. Darrel Ho-Yen, Diretor do Laboratório de Referência de Toxoplasma Escocês e Serviço Nacional de Testes de Doença de Lyme, acredita que o número de casos confirmados deve ser multiplicado por 10 "para levar em conta os casos diagnosticados erroneamente, testes que dão resultados falsos resultados, pacientes que não foram testados, pessoas que estão infectadas, mas não apresentam sintomas, falhas em notificar e indivíduos infectados que não consultam um médico. "
Apesar da doença de Lyme (infecção por Borrelia burgdorferi) ser uma doença de notificação obrigatória na Escócia desde janeiro de 1990, que deve, portanto, ser relatada com base na suspeita clínica, acredita-se que muitos GPs não estão cientes da exigência. Os relatórios obrigatórios, limitados apenas aos resultados dos testes de laboratório, foram introduzidos em todo o Reino Unido em outubro de 2010, de acordo com os Regulamentos de Proteção à Saúde (Notificação) de 2010.
Embora haja um maior número de casos da doença de Lyme em New Forest , Salisbury Plain , Exmoor , South Downs , partes de Wiltshire e Berkshire , Thetford Forest e a costa oeste e ilhas da Escócia, os carrapatos infectados estão disseminados e podem até ser encontrados nos parques de Londres. Um relatório de 1989 descobriu que 25% dos trabalhadores florestais em New Forest eram soropositivos , assim como entre 2% e 4-5% da população local geral da área.
Testes em cães de estimação realizados em todo o país em 2009 indicaram que cerca de 2,5% dos carrapatos no Reino Unido podem estar infectados, consideravelmente mais do que se pensava. Pensa-se que o aquecimento global pode levar a um aumento da atividade do carrapato no futuro, bem como a um aumento na quantidade de tempo que as pessoas passam em parques públicos, aumentando assim o risco de infecção.
América do Norte
Muitos estudos na América do Norte examinaram correlatos ecológicos e ambientais do número de pessoas afetadas pela doença de Lyme. Um estudo de 2005 usando modelagem de adequação climática de I. scapularis projetou que a mudança climática causaria um aumento geral de 213% no habitat vetorial adequado até o ano 2080, com expansões para o norte no Canadá, maior adequação no centro dos EUA e diminuição de habitat adequado e vetor retração no sul dos EUA. Uma revisão de estudos publicados em 2008 concluiu que a presença de florestas ou áreas florestadas foi a única variável que elevou consistentemente o risco de doença de Lyme, enquanto outras variáveis ambientais mostraram pouca ou nenhuma concordância entre os estudos. Os autores argumentaram que os fatores que influenciam a densidade do carrapato e o risco humano entre os locais ainda são mal compreendidos e que estudos futuros devem ser realizados por períodos de tempo mais longos, tornar-se mais padronizados nas regiões e incorporar o conhecimento existente da ecologia regional da doença de Lyme .
Canadá
Devido à mudança climática, a gama de carrapatos capazes de transmitir a doença de Lyme se expandiu de uma área limitada de Ontário para incluir áreas do sul de Quebec, Manitoba, norte de Ontário, sul de New Brunswick, sudoeste da Nova Escócia e partes limitadas de Saskatchewan e Alberta, como bem como British Columbia. Casos foram relatados no extremo leste da ilha de Newfoundland. Uma previsão baseada em modelo por Leighton et al. (2012) sugere que o alcance do carrapato I. scapularis se expandirá para o Canadá em 46 km / ano na próxima década, com o aquecimento das temperaturas climáticas como o principal impulsionador do aumento da velocidade de propagação.
México
Um estudo de 2007 sugere que as infecções por Borrelia burgdorferi são endêmicas no México, a partir de quatro casos relatados entre 1999 e 2000.
Estados Unidos
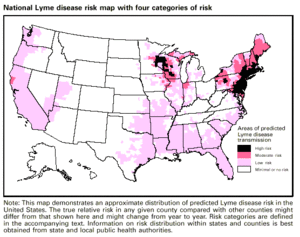
A cada ano, aproximadamente 30.000 novos casos são relatados ao CDC; no entanto, esse número provavelmente está subestimado. O CDC está atualmente conduzindo pesquisas sobre avaliação e diagnóstico da doença e os resultados preliminares sugerem que o número de novos casos seja em torno de 300.000.
A doença de Lyme é a doença transmitida por carrapatos mais comum na América do Norte e na Europa e uma das doenças infecciosas de crescimento mais rápido nos Estados Unidos. Dos casos relatados ao CDC dos Estados Unidos, a proporção de infecção da doença de Lyme é de 7,9 casos para cada 100.000 pessoas. Nos dez estados onde a doença de Lyme é mais comum, a média foi de 31,6 casos para cada 100.000 pessoas no ano de 2005.
Embora a doença de Lyme tenha sido relatada em todos os estados, cerca de 99% de todos os casos relatados estão confinados a apenas cinco áreas geográficas (Nova Inglaterra, Meio-Atlântico, Leste-Norte Central, Atlântico Sul e Oeste Norte-Central). As novas diretrizes de definição de caso Lyme do CDC 2011 são usadas para determinar os casos confirmados de vigilância do CDC.
A partir de janeiro de 2008, o CDC atribui peso igual às evidências laboratoriais de 1 uma cultura positiva para B. burgdorferi ; 2) teste de duas camadas ( triagem ELISA e confirmação de Western blot ); ou 3 ) Western blot de IgG de camada única (infecção antiga). Anteriormente, o CDC incluía apenas evidências laboratoriais com base em (1) e (2) em sua definição de caso de vigilância. A definição de caso agora inclui o uso de Western blot sem tela ELISA anterior.
O número de casos notificados da doença vem aumentando, assim como as regiões endêmicas da América do Norte. Por exemplo, B. burgdorferi sensu lato era considerado anteriormente como tendo sua capacidade de ser mantida em um ciclo enzoótico na Califórnia, porque foi assumido que a grande população de lagartos diluiria o número de pessoas afetadas por B. burgdorferi nas populações locais de carrapatos ; desde então, isso foi questionado, já que algumas evidências sugerem que os lagartos podem ser infectados.
Exceto por um estudo na Europa, muitos dos dados envolvendo lagartos são baseados na detecção de DNA da espiroqueta e não demonstraram que lagartos são capazes de infectar carrapatos que se alimentam deles. Como alguns experimentos sugerem que os lagartos são refratários à infecção por Borrelia , parece que seu envolvimento no ciclo enzoótico é mais complexo e específico da espécie.
Enquanto B. burgdorferi está mais associada a carrapatos hospedados por veados-de-cauda-branca e camundongos-de-pés-brancos , Borrelia afzelii é mais frequentemente detectada em carrapatos vetores que se alimentam de roedores, e Borrelia garinii e Borrelia valaisiana parecem estar associadas a pássaros. Roedores e pássaros são hospedeiros reservatórios competentes para B. burgdorferi sensu stricto . A resistência de uma genoespécie de espiroquetas da doença de Lyme às atividades bacteriolíticas da via alternativa do complemento de várias espécies hospedeiras pode determinar sua associação hospedeira-reservatório.
Podem existir várias condições semelhantes, mas aparentemente distintas, causadas por várias espécies ou subespécies de Borrelia na América do Norte. Uma condição regionalmente restrita que pode estar relacionada à infecção por Borrelia é a erupção cutânea associada ao carrapato do sul (STARI), também conhecida como doença de Masters. Amblyomma americanum , comumente conhecido como carrapato estrela solitária, é reconhecido como o vetor primário de STARI. Em algumas partes da distribuição geográfica de STARI, a doença de Lyme é bastante rara (por exemplo, Arkansas), portanto, as pessoas nessas regiões com sintomas semelhantes aos de Lyme - especialmente se seguirem uma picada de um carrapato estrela solitária - devem considerar STARI como um possibilidade. Geralmente é uma condição mais branda do que Lyme e geralmente responde bem ao tratamento com antibióticos.
Nos últimos anos, ocorreram de 5 a 10 casos por ano de uma doença semelhante à de Lyme em Montana. Ocorre principalmente em bolsões ao longo do rio Yellowstone, no centro de Montana. As pessoas desenvolveram uma erupção cutânea em forma de olho de boi ao redor da picada de um carrapato, seguida por semanas de fadiga e febre.
Os efeitos da doença de Lyme são comparáveis entre homens e mulheres. Uma ampla gama de grupos de idade é afetada, embora o número de casos seja mais alto entre as pessoas de 10 a 19 anos. Por razões desconhecidas, a doença de Lyme é sete vezes mais comum entre os asiáticos.
América do Sul
Na América do Sul, o reconhecimento e a ocorrência de doenças transmitidas por carrapatos estão aumentando. No Brasil, foi identificada uma doença semelhante a Lyme conhecida como síndrome de Baggio-Yoshinari , causada por microrganismos que não pertencem ao complexo B. burgdorferi sensu lato e transmitida por carrapatos dos gêneros Amblyomma e Rhipicephalus . O primeiro caso relatado de SBY no Brasil foi feito em 1992, em Cotia , São Paulo.
História
A história evolutiva da genética de Borrelia burgdorferi tem sido objeto de estudos recentes. Um estudo descobriu que antes do reflorestamento que acompanhou o abandono das fazendas pós-coloniais na Nova Inglaterra e a migração em massa para o meio-oeste que ocorreu durante o início do século 19, a doença de Lyme estava presente por milhares de anos na América e se espalhou ao longo com seus hospedeiros de carrapatos do Nordeste ao Centro-Oeste.
John Josselyn, que visitou a Nova Inglaterra em 1638 e novamente de 1663 a 1670, escreveu "há um número infinito de carrapatos pendurados nos arbustos no verão que se agarram às roupas do homem e se enfiam em suas calças, comendo-se em pouco tempo no a própria carne de um homem. Eu vi as meias daqueles que passaram pelo bosque cobertas com elas. "
Isso também é confirmado pelos escritos de Peter Kalm , um botânico sueco que foi enviado para a América por Linnaeus , e que encontrou as florestas de Nova York "repletas" de carrapatos quando ele a visitou em 1749. Quando a jornada de Kalm foi refeita 100 anos depois, as florestas haviam desaparecido e a bactéria Lyme provavelmente ficara isolada em alguns bolsões ao longo da costa nordeste, Wisconsin e Minnesota.
Talvez a primeira descrição detalhada do que agora é conhecido como doença de Lyme tenha aparecido nos escritos de John Walker após uma visita à ilha de Jura (Deer Island) na costa oeste da Escócia em 1764. Ele dá uma boa descrição de ambos os sintomas da doença de Lyme (com "dor intensa [nas] partes internas dos membros") e do próprio vetor do carrapato, que ele descreve como um "verme" com um corpo "de cor avermelhada e de forma comprimida com uma fila de pés de cada lado "que" penetra na pele ". Muitas pessoas desta área da Grã-Bretanha emigraram para a América do Norte entre 1717 e o final do século XVIII.
O exame de espécimes de museu preservados encontrou DNA de Borrelia em um carrapato Ixodes ricinus infectado da Alemanha que remonta a 1884, e em um camundongo infectado de Cape Cod que morreu em 1894. A autópsia de Ötzi, o Homem de Gelo , em 2010 , com 5.300 anos múmia velha , revelou a presença da sequência de DNA de Borrelia burgdorferi tornando-o o primeiro ser humano conhecido com a doença de Lyme.
Os primeiros estudos europeus sobre o que hoje é conhecido como doença de Lyme descreveram suas manifestações cutâneas. O primeiro estudo data de 1883 em Breslau , Alemanha (agora Wrocław , Polônia ), onde o médico Alfred Buchwald descreveu um homem que sofria por 16 anos com uma doença degenerativa da pele agora conhecida como acrodermatite crônica atrófica .
Em uma conferência de pesquisa em 1909, o dermatologista sueco Arvid Afzelius apresentou um estudo sobre uma lesão em forma de anel em expansão que ele observou em uma mulher idosa após a picada de um carrapato de ovelha. Ele chamou a lesão de eritema migrans . A condição da pele agora conhecida como linfocitoma borrelial foi descrita pela primeira vez em 1911.
A história moderna da compreensão médica da doença, incluindo sua causa, diagnóstico e tratamento, tem sido difícil.
Problemas neurológicos após picadas de carrapatos foram reconhecidos a partir da década de 1920. Os médicos franceses Garin e Bujadoux descreveram um fazendeiro com uma radiculite sensorial dolorosa acompanhada de meningite leve após uma picada de carrapato. Uma grande erupção em forma de anel também foi observada, embora os médicos não a relacionassem com a meningoradiculite. Em 1930, o dermatologista sueco Sven Hellerström foi o primeiro a propor EM e sintomas neurológicos após uma picada de carrapato foram relacionados. Na década de 1940, o neurologista alemão Alfred Bannwarth descreveu vários casos de meningite linfocítica crônica e polirradiculoneurite, alguns dos quais acompanhados de lesões cutâneas eritematosas.
Carl Lennhoff, que trabalhava no Instituto Karolinska na Suécia, acreditava que muitos problemas de pele eram causados por espiroquetas. Em 1948, ele usou uma coloração especial para observar microscopicamente o que ele acreditava serem espiroquetas em vários tipos de lesões de pele, incluindo EM. Embora suas conclusões mais tarde tenham se mostrado errôneas, o interesse pelo estudo das espiroquetas foi despertado. Em 1949, Nils Thyresson, que também trabalhava no Instituto Karolinska, foi o primeiro a tratar ACA com penicilina. Na década de 1950, a relação entre picada de carrapato, linfocitoma, EM e síndrome de Bannwarth foi reconhecida em toda a Europa, levando ao uso generalizado de penicilina para tratamento na Europa.
Em 1970, um dermatologista em Wisconsin chamado Rudolph Scrimenti reconheceu uma lesão EM em uma pessoa depois de relembrar um artigo de Hellerström que havia sido reimpresso em uma revista científica americana em 1950. Este foi o primeiro caso documentado de EM nos Estados Unidos. Com base na literatura europeia, ele tratou a pessoa com penicilina.
A síndrome completa agora conhecida como doença de Lyme não foi reconhecida até que um grupo de casos originalmente considerados artrite reumatóide juvenil foi identificado em três cidades no sudeste de Connecticut em 1975, incluindo as cidades de Lyme e Old Lyme , que deram à doença seu nome popular. Isso foi investigado pelos médicos David Snydman e Allen Steere, do Epidemic Intelligence Service , e por outros da Universidade de Yale , incluindo Stephen Malawista , que é creditado como um co-descobridor da doença. O reconhecimento de que as pessoas nos Estados Unidos tinham EM levou ao reconhecimento de que a "artrite de Lyme" era uma manifestação da mesma doença transmitida por carrapatos conhecida na Europa.
Antes de 1976, os elementos da infecção por B. burgdorferi sensu lato eram chamados ou conhecidos como meningopolineurite transmitida por carrapatos, síndrome de Garin-Bujadoux, síndrome de Bannwarth, doença de Afzelius, Montauk Knee ou febre do carrapato das ovelhas. Desde 1976, a doença é mais frequentemente referida como doença de Lyme, borreliose de Lyme ou simplesmente borreliose.
Em 1980, Steere, et al. , começou a testar regimes de antibióticos em adultos com doença de Lyme. No mesmo ano, o epidemiologista do Departamento de Saúde do Estado de Nova York, Jorge Benach, forneceu a Willy Burgdorfer , pesquisador do Rocky Mountain Biological Laboratory , coleções de I. dammini [ scapularis ] de Shelter Island, Nova York, uma área endêmica de Lyme conhecida como parte de uma investigação em andamento da febre maculosa das Montanhas Rochosas. Ao examinar os carrapatos em busca de riquétsias, Burgdorfer notou "espiroquetas mal coradas, bastante longas e irregularmente enroladas". Um exame posterior revelou espiroquetas em 60% dos carrapatos. Burgdorfer creditou sua familiaridade com a literatura europeia por sua compreensão de que os espiroquetas podem ser a "causa há muito procurada da ECM e da doença de Lyme". Benach forneceu-lhe mais carrapatos de Shelter Island e soros de pessoas diagnosticadas com a doença de Lyme. O pesquisador do Centro de Ciências da Saúde da Universidade do Texas, Alan Barbour, "ofereceu sua experiência para cultura e caracterização imunoquímica do organismo." Burgdorfer posteriormente confirmou sua descoberta isolando, de pessoas com doença de Lyme, espiroquetas idênticas às encontradas em carrapatos. Em junho de 1982, ele publicou suas descobertas na Science , e a espiroqueta foi batizada de Borrelia burgdorferi em sua homenagem.
Após a identificação de B. burgdorferi como o agente causador da doença de Lyme, os antibióticos foram selecionados para teste, guiados por sensibilidades antibióticas in vitro , incluindo antibióticos tetraciclina , amoxicilina , cefuroxima axetil , penicilina intravenosa e intramuscular e ceftriaxona intravenosa . O mecanismo de transmissão de carrapatos também foi objeto de muita discussão. Os espiroquetas B. burgdorferi foram identificados na saliva do carrapato em 1987, confirmando a hipótese de que a transmissão ocorreu através das glândulas salivares do carrapato.
Sociedade e cultura
A urbanização e outros fatores antropogênicos podem estar implicados na disseminação da doença de Lyme para os humanos. Em muitas áreas, a expansão de bairros suburbanos levou ao desmatamento gradual das áreas arborizadas circundantes e aumentou o contato de fronteira entre humanos e áreas densas por carrapatos. A expansão humana também resultou na redução de predadores que caçam veados, bem como ratos, esquilos e outros pequenos roedores - os principais reservatórios da doença de Lyme. Como consequência do aumento do contato humano com o hospedeiro e o vetor , a probabilidade de transmissão da doença aumentou muito. Os pesquisadores estão investigando possíveis ligações entre o aquecimento global e a propagação de doenças transmitidas por vetores, incluindo a doença de Lyme.
Controvérsia
O termo "doença de Lyme crônica" é controverso e não é reconhecido na literatura médica, e a maioria das autoridades médicas desaconselha o tratamento com antibióticos de longo prazo para a doença de Lyme. Estudos demonstraram que a maioria das pessoas com diagnóstico de "doença de Lyme crônica" não tem evidências objetivas de infecção anterior ou atual por B. burgdorferi ou são pessoas que devem ser classificadas como portadoras da síndrome da doença de Lyme pós-tratamento (PTLDS), que é definida como sintomas inespecíficos contínuos ou recorrentes (como fadiga, dor musculoesquelética e queixas cognitivas) em uma pessoa previamente tratada para a doença de Lyme.
O documentário de 2008 Under Our Skin é conhecido por promover teorias da conspiração sobre a "doença crônica de Lyme".
Outros animais
Animais de estimação
A prevenção da doença de Lyme é um passo importante para manter os cães seguros em áreas endêmicas. Educação de prevenção e uma série de medidas preventivas estão disponíveis. Em primeiro lugar, para os donos de cães que moram perto ou que costumam frequentar áreas infestadas por carrapatos, a vacinação de rotina de seus cães é um passo importante.
Outra medida preventiva crucial é o uso de acaricidas persistentes, como repelentes tópicos ou pesticidas que contenham triazapentadienos ( Amitraz ), fenilpirazóis ( Fipronil ) ou permetrina ( piretróides ). Esses acaricidas têm como alvo principalmente os estágios adultos dos carrapatos portadores de Lyme e reduzem o número de carrapatos reprodutivamente ativos no ambiente. As formulações desses ingredientes estão disponíveis em uma variedade de formas tópicas, incluindo spot-ons, sprays, pós, colares impregnados, soluções e xampus.
O exame de um cão para carrapatos depois de estar em uma área infestada de carrapatos é uma importante medida de precaução na prevenção da doença de Lyme. Os principais pontos a serem examinados incluem a cabeça, o pescoço e as orelhas.
Em cães, um prognóstico sério a longo prazo pode resultar em doença glomerular, que é uma categoria de lesão renal que pode causar doença renal crônica. Os cães também podem ter doenças crônicas nas articulações se a doença não for tratada. No entanto, a maioria dos casos de doença de Lyme em cães resulta na recuperação completa com, e às vezes sem, tratamento com antibióticos. Em casos raros, a doença de Lyme pode ser fatal para humanos e cães.
Referência
![]() Este artigo incorpora material de domínio público do documento dos Centros de Controle e Prevenção de Doenças : "Síndrome da Doença de Lyme Pós-tratamento" .
Este artigo incorpora material de domínio público do documento dos Centros de Controle e Prevenção de Doenças : "Síndrome da Doença de Lyme Pós-tratamento" .
Leitura adicional
- Ostfeld, Richard (2012). Doença de Lyme: A Ecologia de um Sistema Complexo . Nova York: Oxford University Press . ISBN 978-0199928477.
- Barbour, Alan G. (2015). Doença de Lyme: por que está se espalhando, como deixa você doente e o que fazer a respeito . Baltimore. ISBN 9781421417219.
- Halperin, John Jay, ed. (2018). Doença de Lyme: uma abordagem baseada em evidências (2ª ed.). Wallingford, Oxfordshire, Reino Unido: CABI. ISBN 1786392070.
- Radolf, Justin D .; Samuels, D. Scott, eds. (2021). Doença de Lyme e espiroquetas febris recorrentes: genômica, biologia molecular, interações do hospedeiro e patogênese da doença . Poole, Reino Unido: Caister. ISBN 1913652610.
links externos
- Organizações da doença de Lyme em Curlie
- CDC - Doença de Lyme
- Testes de doença de Lyme - testes de laboratório online
- NIH - Doença de Lyme
- Diretrizes NICE - Doença de Lyme
| Classificação | |
|---|---|
| Fontes externas |
|