Acetato de magnésio - Magnesium acetate
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Acetato de magnésio
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.005.050 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| Mg (CH 3 COO) 2 | |
| Massa molar | 142,394 (anidro) 214,455 (tetra-hidrato) |
| Aparência | Cristais higroscópicos brancos |
| Densidade | 1,45 g / cm 3 |
| Ponto de fusão | 80 ° C (176 ° F; 353 K) (tetra-hidrato) |
| Solúvel | |
| −116,0 · 10 −6 cm 3 / mol (+4 H 2 O | |
| Compostos relacionados | |
|
Outros cátions
|
Acetato de cálcio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
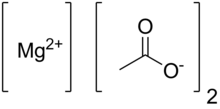
O acetato de magnésio anidro possui a fórmula química Mg (C 2 H 3 O 2 ) 2 e em sua forma hidratada, acetato de magnésio tetra-hidratado, possui a fórmula química Mg (CH 3 COO) 2 • 4H 2 O. Neste composto o magnésio possui um estado de oxidação de 2 + . O acetato de magnésio é o sal de magnésio do ácido acético . É deliquescente e, ao ser aquecido, se decompõe para formar óxido de magnésio . O acetato de magnésio é comumente usado como fonte de magnésio em reações biológicas.
Propriedades físicas
O acetato de magnésio aparece como cristais higroscópicos brancos . Tem cheiro de ácido acético e é solúvel em água. Quando está em solução aquosa, seu pH estará no lado alcalino do neutro.
Armazenar
Por ser muito higroscópico, deve ser armazenado longe da água. Também é incompatível com oxidantes fortes e não deve ser misturado com eles.
Síntese
Síntese do acetato de magnésio a partir da reação do hidróxido de magnésio com o ácido acético.
- 2 CH 3 COOH + Mg (OH) 2 → (CH 3 COO) 2 Mg + 2 H 2 O
Carbonato de magnésio suspenso em água destilada com solução de ácido acético a 20%.
- 2 CH 3 COOH + MgCO 3 → Mg (CH 3 COO) 2 + CO 2 + H 2 O
A reação do magnésio metálico com o ácido acético dissolvido em benzeno seco causa a formação de acetato de magnésio junto com a liberação de gás hidrogênio.
- Mg +2 CH 3 COOH → Mg (CH 3 COO) 2 + H 2
Usos e aplicações
Em 1881, Charles Clamond inventou a cesta Clamond , uma das primeiras mantas de gás eficazes . Os reagentes usados nesta invenção incluem acetato de magnésio , hidróxido de magnésio e água.
O acetato de magnésio é comumente usado como fonte de magnésio ou para o íon acetato em experimentos químicos. Um exemplo disso é quando o acetato de magnésio e o nitrato de magnésio foram usados para realizar simulações de dinâmica molecular e medições de tensão superficial. No experimento, os autores descobriram que o acetato tinha uma afinidade mais forte com a superfície em comparação com o íon nitrato e que o Mg 2+ era fortemente repelido para longe da interferência ar / líquido. Eles também descobriram que o Mg 2+ tinha uma tendência mais forte de se ligar ao íon acetato em comparação ao nitrato.
Um dos usos mais comuns do acetato de magnésio é na mistura chamada acetato de cálcio e magnésio (CMA). É uma mistura de acetato de cálcio e acetato de magnésio. O CMA é considerado uma alternativa ambientalmente correta para o degelo ao NaCl e ao CaCl 2 . O CMA também atua como um poderoso SO 2 , NO x e agente de controle de emissão de partículas tóxicas em processos de combustão de carvão para reduzir a chuva ácida e como um catalisador eficaz para a facilitação da combustão de carvão.
Foi descoberto que o acetato de magnésio causa uma mudança conformacional na enzima Primase da Escherichia coli . Neste experimento Mg (OAc) 2 , MnCl 2 , CaCl 2 , NaOAc, LiCl, MgSO 4 e MgCl 2 foram todos comparados para ver qual efeito eles tiveram na enzima Primase de Escherichia coli . Os experimentadores descobriram que o Mg (OAc) 2 causou a melhor mudança conformacional. MgSO 4 e MgCl 2 induziram o efeito ligeiramente, enquanto o resto não.
Quando o acetato de magnésio é misturado ao peróxido de hidrogênio, ele atua como um bactericida.
O acetato de magnésio demonstrou ser eficaz na incineração de compostos orgânicos na preparação para uma análise de flúor quando altas ou baixas concentrações de flúor estão presentes.
Segurança
O acetato de magnésio é um composto relativamente seguro de manusear e recebeu uma classificação de risco para a saúde igual a zero. Porém, sempre deve ser manuseado com luvas e óculos de segurança. Se entrar em contacto com os olhos, pele, ingerido ou inalado, irá causar irritação nas respectivas áreas: olhos, pele, sistema gastrointestinal e pulmões.
Referências
| AcOH | Ele | |||||||||||||||||||
| LiOAc |
Be (OAc) 2 BeAcOH |
B (OAc) 3 |
AcOAc ROAc |
NH 4 OAc | AcOOH | FAc | Ne | |||||||||||||
| NaOAc | Mg (OAc) 2 |
Al (OAc) 3 ALSOL Al (OAc) 2 OH Al 2 SO 4 (OAc) 4 |
Si | P | S | ClAc | Ar | |||||||||||||
| KOAc | Ca (OAc) 2 | Sc (OAc) 3 | Ti (OAc) 4 | VO (OAc) 3 |
Cr (OAc) 2 Cr (OAc) 3 |
Mn (OAc) 2 Mn (OAc) 3 |
Fe (OAc) 2 Fe (OAc) 3 |
Co (OAc) 2 | Ni (OAc) 2 | Cu (OAc) 2 | Zn (OAc) 2 | Ga (OAc) 3 | Ge | As (OAc) 3 | Se | BrAc | Kr | |||
| RbOAc | Sr (OAc) 2 | Y (OAc) 3 | Zr (OAc) 4 | Nb | Mo (OAc) 2 | Tc |
Ru 2 (OAc) 4 Cl Ru (OAc) 3 |
Rh 2 (OAc) 4 | Pd (OAc) 2 | AgOAc | Cd (OAc) 2 | Dentro |
Sn (OAc) 2 Sn (OAc) 4 |
Sb (OAc) 3 | Te | IAc | Xe | |||
| CsOAc | Ba (OAc) 2 | * | Lu (OAc) 3 | Hf | Ta | C | Ré | Os | Ir | Pt (OAc) 2 | Au |
Hg 2 (OAc) 2 , Hg (OAc) 2 |
TlOAc Tl (OAc) 3 |
Pb (OAc) 2 Pb (OAc) 4 |
Bi (OAc) 3 | Po | No | Rn | ||
| Fr | Ra | ** | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||
| * | La (OAc) 3 | Ce (OAc) x | Pr | WL | PM | Sm (OAc) 3 | Eu (OAc) 3 | Gd (OAc) 3 | Tb | Dy (OAc) 3 | Ho (OAc) 3 | Er | Tm | Yb (OAc) 3 | ||||||
| ** | Ac | º | Pa | UO 2 (OAc) 2 | Np | Pu | Sou | Cm | Bk | Cf | Es | Fm | Md | Não | ||||||
