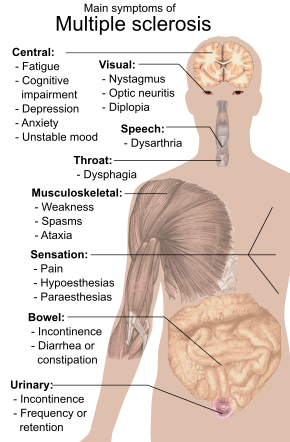
Esclerose múltipla -Multiple sclerosis
| Esclerose múltipla | |
|---|---|
| Outros nomes | Esclerose disseminada, encefalomielite disseminada |
 | |
| O tecido corado com CD68 mostra vários macrófagos na área de uma lesão desmielinizada causada por MS. | |
| Especialidade | Neurologia |
| Sintomas | Variável, incluindo quase qualquer sintoma ou sinal neurológico, sendo os problemas autonômicos , visuais, motores e sensoriais os mais comuns. |
| Início habitual | Idade 20-50 |
| Duração | Longo prazo |
| Causas | Desconhecido |
| Método de diagnóstico | Com base nos sintomas e exames médicos |
| Tratamento | Medicamentos, fisioterapia, terapia ocupacional |
| Prognóstico | Expectativa de vida menor de 5 a 10 anos |
| Frequência | 2 milhões (2015) |
| Mortes | 18.900 (2015) |
A esclerose múltipla ( EM ), também conhecida como encefalomielite disseminada , é a doença desmielinizante mais comum , na qual as capas isolantes das células nervosas do cérebro e da medula espinhal são danificadas. Esse dano interrompe a capacidade de partes do sistema nervoso de transmitir sinais , resultando em uma série de sinais e sintomas , incluindo problemas físicos, mentais e, às vezes, psiquiátricos. Os sintomas específicos podem incluir visão dupla , cegueira em um olho, fraqueza muscular e problemas com a sensaçãoou coordenação. A EM assume várias formas, com novos sintomas ocorrendo em ataques isolados (formas recorrentes) ou se acumulando ao longo do tempo (formas progressivas). Entre os ataques, os sintomas podem desaparecer completamente, embora os problemas neurológicos permanentes geralmente permaneçam, especialmente à medida que a doença avança.
Embora a causa não seja clara, acredita-se que o mecanismo subjacente seja a destruição pelo sistema imunológico ou a falha das células produtoras de mielina . As causas propostas para isso incluem fatores genéticos e ambientais, como infecções virais . A EM é geralmente diagnosticada com base nos sinais e sintomas apresentados e nos resultados de exames médicos complementares.
Não há cura conhecida para a esclerose múltipla. Os tratamentos tentam melhorar a função após um ataque e prevenir novos ataques. Os medicamentos usados para tratar a EM, embora modestamente eficazes, podem ter efeitos colaterais e ser mal tolerados. A fisioterapia e a terapia ocupacional podem ajudar na capacidade de funcionamento das pessoas. Muitas pessoas buscam tratamentos alternativos , apesar da falta de evidências de benefícios. O resultado a longo prazo é difícil de prever; bons resultados são mais frequentemente observados em mulheres, aqueles que desenvolvem a doença no início da vida, aqueles com curso recidivante e aqueles que inicialmente experimentaram poucos ataques. A expectativa de vida é de cinco a dez anos menor do que a da população não afetada.
A esclerose múltipla é a doença imunomediada mais comum que afeta o sistema nervoso central . Em 2015, cerca de 2,3 milhões de pessoas foram afetadas globalmente, com taxas variando amplamente em diferentes regiões e entre diferentes populações. Naquele ano, cerca de 18.900 pessoas morreram de esclerose múltipla, contra 12.000 em 1990. A doença geralmente começa entre as idades de vinte e cinquenta e é duas vezes mais comum em mulheres do que em homens. A EM foi descrita pela primeira vez em 1868 pelo neurologista francês Jean-Martin Charcot . O nome esclerose múltipla refere -se às inúmeras cicatrizes gliais (ou escleras – essencialmente placas ou lesões) que se desenvolvem na substância branca do cérebro e da medula espinhal. A partir de 2009, uma série de novos tratamentos e métodos de diagnóstico estão em desenvolvimento.
sinais e sintomas
Uma pessoa com EM pode ter quase qualquer sintoma ou sinal neurológico, sendo os problemas autonômicos , visuais, motores e sensoriais os mais comuns. Os sintomas específicos são determinados pela localização das lesões no sistema nervoso e podem incluir perda de sensibilidade ou alterações na sensação , como formigamento, formigamento ou dormência, fraqueza muscular, visão turva , reflexos muito pronunciados , espasmos musculares ou dificuldade de locomoção; dificuldades de coordenação e equilíbrio ( ataxia ); problemas de fala ou deglutição , problemas visuais ( nistagmo , neurite óptica ou visão dupla ), sensação de cansaço , dores agudas ou crônicas , dificuldades na bexiga e no intestino (como bexiga neurogênica ), entre outros.
Quando a esclerose múltipla está mais avançada, podem ocorrer dificuldades de locomoção e o risco de queda aumenta.
Dificuldades de pensamento e problemas emocionais, como depressão ou humor instável, também são comuns. O fenômeno de Uhthoff , um agravamento dos sintomas devido à exposição a temperaturas acima do normal, e o sinal de Lhermitte , uma sensação elétrica que percorre as costas ao dobrar o pescoço, são particularmente característicos da EM. A principal medida de incapacidade e gravidade é a escala expandida de status de incapacidade (EDSS), com outras medidas, como o composto funcional da esclerose múltipla, sendo cada vez mais usadas em pesquisas. A EDSS também está correlacionada com quedas em pessoas com EM. Embora seja uma medida popular, o EDSS foi criticado por algumas de suas limitações, como confiar demais na caminhada.
A condição começa em 85% dos casos como uma síndrome clinicamente isolada (CIS) ao longo de vários dias, com 45% com problemas motores ou sensoriais, 20% com neurite óptica e 10% com sintomas relacionados à disfunção do tronco cerebral , enquanto os 25 restantes % tem mais de uma das dificuldades anteriores. O curso dos sintomas ocorre inicialmente em dois padrões principais: como episódios de piora súbita que duram alguns dias a meses (chamados de recaídas , exacerbações, crises, ataques ou surtos) seguidos de melhora (85% dos casos) ou como um agravamento gradual ao longo do tempo sem períodos de recuperação (10-15% dos casos). Uma combinação desses dois padrões também pode ocorrer ou as pessoas podem iniciar um curso recorrente e remitente que se torna progressivo mais tarde.
As recaídas geralmente não são previsíveis, ocorrendo sem aviso prévio. As exacerbações raramente ocorrem com mais frequência do que duas vezes por ano. Algumas recaídas, no entanto, são precedidas por gatilhos comuns e ocorrem com mais frequência durante a primavera e o verão. Da mesma forma, infecções virais, como resfriado comum , gripe ou gastroenterite , aumentam seu risco. O estresse também pode desencadear um ataque. Mulheres com EM que engravidam apresentam menos recaídas; no entanto, durante os primeiros meses após o parto, o risco aumenta. No geral, a gravidez não parece influenciar a incapacidade a longo prazo. Muitos eventos foram encontrados para não afetar as taxas de recaída, incluindo vacinação , amamentação , trauma físico e fenômeno de Uhthoff .
Fase prodrômica
A EM pode ter uma fase prodrômica nos anos que antecedem a manifestação da EM, caracterizada por problemas psiquiátricos, comprometimento cognitivo e aumento da utilização dos cuidados de saúde.
Causas
A causa da EM é desconhecida; no entanto, acredita-se que ocorra como resultado de alguma combinação de fatores genéticos e ambientais, como agentes infecciosos.
Geografia
A EM é mais comum em pessoas que vivem mais longe do equador , embora existam exceções. Essas exceções incluem grupos étnicos de baixo risco e que vivem longe do equador, como os sami , ameríndios , huteritas canadenses , maoris da Nova Zelândia e inuítes do Canadá , bem como grupos de risco relativamente alto e que vivem mais perto de o equador, como sardos , sicilianos do interior , palestinos e parsi . A causa deste padrão geográfico não é clara. Enquanto o gradiente de incidência norte-sul está diminuindo, a partir de 2010 ele ainda está presente.
A EM é mais comum em regiões com populações do norte da Europa e a variação geográfica pode simplesmente refletir a distribuição global dessas populações de alto risco.
Uma relação entre a estação do nascimento e a EM dá suporte a essa ideia, com menos pessoas nascidas no hemisfério norte em novembro em comparação com maio sendo afetadas mais tarde na vida.
Fatores ambientais podem desempenhar um papel durante a infância, com vários estudos descobrindo que pessoas que se mudam para uma região diferente do mundo antes dos 15 anos adquirem o risco de EM da nova região. Se a migração ocorrer após os 15 anos, no entanto, a pessoa mantém o risco de seu país de origem. Há algumas evidências de que o efeito da mudança ainda pode se aplicar a pessoas com mais de 15 anos.
Genética
A EM não é considerada uma doença hereditária ; no entanto, várias variações genéticas demonstraram aumentar o risco. Alguns desses genes parecem ter níveis mais altos de expressão em células microgliais do que o esperado por acaso. A probabilidade de desenvolver a doença é maior em parentes de uma pessoa afetada, com maior risco entre os parentes mais próximos. Um gêmeo idêntico de um indivíduo afetado tem 30% de chance de desenvolver EM, 5% para um gêmeo não idêntico, 2,5% para um irmão e uma chance ainda menor de um meio-irmão. Se ambos os pais são afetados, o risco em seus filhos é 10 vezes maior do que na população em geral. A EM também é mais comum em alguns grupos étnicos do que em outros.
Os genes específicos que foram associados à EM incluem diferenças no sistema do antígeno leucocitário humano (HLA) – um grupo de genes no cromossomo 6 que serve como o principal complexo de histocompatibilidade (MHC). Que as diferenças na região HLA estão relacionadas à suscetibilidade é conhecida desde a década de 1980, e essa mesma região também tem sido implicada no desenvolvimento de outras doenças autoimunes, como diabetes tipo I e lúpus eritematoso sistêmico . O achado mais consistente é a associação entre esclerose múltipla e alelos do MHC definidos como DR15 e DQ6 . Outros loci mostraram efeito protetor, como HLA-C554 e HLA-DRB1 *11. No geral, estima-se que as diferenças de HLA sejam responsáveis por entre 20% e 60% da predisposição genética . Métodos genéticos modernos ( estudos de associação do genoma ) revelaram pelo menos 200 variantes fora do locus HLA que aumentam modestamente a probabilidade de EM.
Agentes infecciosos
Muitos micróbios foram propostos como desencadeantes da EM, mas nenhum foi confirmado. Uma hipótese é que a infecção por um micróbio disseminado contribui para o desenvolvimento da doença, e a distribuição geográfica desse organismo influencia significativamente a epidemiologia da EM. Duas versões opostas desta hipótese incluem a hipótese da higiene e a hipótese da prevalência, sendo a primeira mais favorecida. A hipótese da higiene propõe que a exposição a certos agentes infecciosos no início da vida é protetora; a doença é uma resposta a um encontro tardio com tais agentes. A hipótese de prevalência propõe que uma infecção precoce, persistente e silenciosa aumenta o risco de doença e, portanto, a doença é mais comum onde o agente infeccioso é mais comum. Apenas em alguns casos e após muitos anos causa desmielinização.
As evidências de um vírus como causa incluem a presença de bandas oligoclonais no cérebro e no líquido cefalorraquidiano da maioria das pessoas com EM, a associação de vários vírus com encefalomielite desmielinizante humana e a ocorrência de desmielinização em animais causada por algumas infecções virais. Os vírus do herpes humano são um grupo candidato de vírus. Indivíduos que nunca foram infectados pelo vírus Epstein-Barr têm um risco reduzido de contrair EM, enquanto aqueles infectados quando adultos jovens correm um risco maior do que aqueles que o tiveram em uma idade mais jovem. Embora alguns considerem que isso vai contra a hipótese da higiene, já que os não infectados provavelmente tiveram uma educação mais higiênica, outros acreditam que não há contradição, pois é um primeiro encontro com o vírus causador relativamente tarde na vida que é o gatilho para a doença. Outras doenças que podem estar relacionadas incluem sarampo , caxumba e rubéola .
Outro
O tabagismo pode ser um fator de risco independente para EM. O estresse pode ser um fator de risco, embora a evidência para apoiar isso seja fraca. A associação com exposições ocupacionais e toxinas – principalmente solventes orgânicos – foi avaliada, mas nenhuma conclusão clara foi alcançada. As vacinações foram estudadas como fatores causais; no entanto, a maioria dos estudos não mostra associação. Vários outros possíveis fatores de risco, como dieta e ingestão de hormônios , foram analisados; no entanto, as evidências sobre sua relação com a doença são "escassas e pouco convincentes". A gota ocorre menos do que seria esperado e níveis mais baixos de ácido úrico foram encontrados em pessoas com EM. Isso levou à teoria de que o ácido úrico é protetor, embora sua importância exata permaneça desconhecida. A obesidade durante a adolescência e a idade adulta jovem é um fator de risco para EM.
Fisiopatologia
As três principais características da EM são a formação de lesões no sistema nervoso central (também chamadas de placas), a inflamação e a destruição das bainhas de mielina dos neurônios . Essas características interagem de maneira complexa e ainda não totalmente compreendida para produzir a ruptura do tecido nervoso e, por sua vez, os sinais e sintomas da doença. Acredita-se que os cristais de colesterol prejudicam o reparo da mielina e agravam a inflamação. Acredita-se que a EM seja um distúrbio imunomediado que se desenvolve a partir de uma interação da genética do indivíduo e causas ambientais ainda não identificadas. Acredita-se que o dano seja causado, pelo menos em parte, pelo ataque ao sistema nervoso pelo próprio sistema imunológico de uma pessoa.
Lesões

O nome esclerose múltipla refere-se às cicatrizes (escleras – mais conhecidas como placas ou lesões) que se formam no sistema nervoso. Essas lesões afetam mais comumente a substância branca no nervo óptico , tronco cerebral , gânglios da base e medula espinhal , ou tratos da substância branca próximos aos ventrículos laterais . A função das células da substância branca é transportar sinais entre as áreas da substância cinzenta , onde o processamento é feito, e o resto do corpo. O sistema nervoso periférico raramente está envolvido.
Para ser específico, a EM envolve a perda de oligodendrócitos , as células responsáveis pela criação e manutenção de uma camada de gordura – conhecida como bainha de mielina – que ajuda os neurônios a transportar sinais elétricos (potenciais de ação). Isso resulta em um afinamento ou perda completa de mielina e, à medida que a doença avança, a quebra dos axônios dos neurônios. Quando a mielina é perdida, um neurônio não pode mais conduzir sinais elétricos com eficiência. Um processo de reparo, chamado remielinização , ocorre nas fases iniciais da doença, mas os oligodendrócitos são incapazes de reconstruir completamente a bainha de mielina da célula. Ataques repetidos levam a remielinizações sucessivamente menos efetivas, até que uma placa semelhante a uma cicatriz seja construída ao redor dos axônios danificados. Essas cicatrizes são a origem dos sintomas e, durante um ataque, a ressonância magnética (RM) geralmente mostra mais de dez novas placas. Isso pode indicar que há uma série de lesões abaixo das quais o cérebro é capaz de se reparar sem produzir consequências visíveis. Outro processo envolvido na criação de lesões é um aumento anormal do número de astrócitos devido à destruição de neurônios próximos. Vários padrões de lesão foram descritos.
Inflamação
Além da desmielinização, o outro sinal da doença é a inflamação . Com uma explicação imunológica , o processo inflamatório é causado pelas células T , um tipo de linfócito que desempenha um papel importante nas defesas do organismo. As células T ganham entrada no cérebro por meio de rupturas na barreira hematoencefálica . As células T reconhecem a mielina como estranha e a atacam, explicando por que essas células também são chamadas de "linfócitos autorreativos".
O ataque à mielina inicia processos inflamatórios, que desencadeiam outras células imunes e a liberação de fatores solúveis como citocinas e anticorpos . Uma quebra adicional da barreira hematoencefálica, por sua vez, causa vários outros efeitos prejudiciais, como inchaço , ativação de macrófagos e mais ativação de citocinas e outras proteínas destrutivas. A inflamação pode potencialmente reduzir a transmissão de informações entre os neurônios de pelo menos três maneiras. Os fatores solúveis liberados podem interromper a neurotransmissão por neurônios intactos. Esses fatores podem levar ou aumentar a perda de mielina, ou podem causar a quebra completa do axônio.
Barreira hematoencefalica
A barreira hematoencefálica (BHE) é uma parte do sistema capilar que impede a entrada de células T no sistema nervoso central. Pode tornar-se permeável a esses tipos de células secundária a uma infecção por um vírus ou bactéria. Depois de se reparar, normalmente depois que a infecção desaparece, as células T podem permanecer presas dentro do cérebro. O gadolínio não pode cruzar uma BHE normal e, portanto, a RM com gadolínio é usada para mostrar as quebras da BHE.
Diagnóstico
A esclerose múltipla é tipicamente diagnosticada com base nos sinais e sintomas apresentados, em combinação com imagens médicas de apoio e exames laboratoriais. Pode ser difícil de confirmar, especialmente no início, pois os sinais e sintomas podem ser semelhantes aos de outros problemas médicos.
Os critérios de McDonald , que se concentram em evidências clínicas, laboratoriais e radiológicas de lesões em diferentes momentos e em diferentes áreas, é o método de diagnóstico mais comumente usado, sendo os critérios de Schumacher e Poser de importância histórica.
A partir de 2017, não há um único teste (incluindo biópsia) que possa fornecer um diagnóstico definitivo.
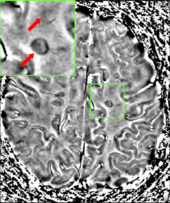
A ressonância magnética (RM) do cérebro e da coluna pode mostrar áreas de desmielinização (lesões ou placas). O gadolínio pode ser administrado por via intravenosa como meio de contraste para evidenciar placas ativas e, por eliminação, demonstrar a existência de lesões históricas não associadas a sintomas no momento da avaliação.
Os sinais da veia central (CVS) têm sido propostos como um bom indicador de SM em comparação com outras condições que causam lesões brancas. Um pequeno estudo encontrou menos CVS em pessoas idosas e hipertensas. Mais pesquisas sobre CVS como biomarcador para MS estão em andamento.
A atrofia cerebral é vista como um indicador de EM.
O teste do líquido cefalorraquidiano obtido de uma punção lombar pode fornecer evidências de inflamação crônica no sistema nervoso central. O líquido cefalorraquidiano é testado para bandas oligoclonais de IgG na eletroforese , que são marcadores de inflamação encontrados em 75 a 85% das pessoas com EM.
Diagnóstico diferencial
Existem várias doenças que se apresentam de forma semelhante à esclerose múltipla. Vômitos intratáveis, neurite óptica grave ou neurite óptica bilateral levantam a suspeita de transtorno do espectro da neuromielite óptica (NMOSD). O envolvimento de múltiplos nervos cranianos levanta a suspeita de neurossarcoidose . A mielite transversa longitudinalmente extensa (LETM), na qual o dano da medula espinhal abrange três ou mais segmentos vertebrais, levanta a suspeita de NMOSD, neurossarcoidose, mielite associada ao anti-MOG , doença reumatológica sistêmica ou distúrbio paraneoplásico .
Tipos e variantes
Vários fenótipos (comumente denominados tipos ), ou padrões de progressão, foram descritos. Os fenótipos usam o curso passado da doença na tentativa de prever o curso futuro. Eles são importantes não apenas para o prognóstico, mas também para as decisões de tratamento. Atualmente, a Sociedade Nacional de Esclerose Múltipla dos Estados Unidos e a Federação Internacional de Esclerose Múltipla , descreve quatro tipos de EM (revisado em 2013):
- Síndrome clinicamente isolada (CIS)
- MS recorrente-remitente (RRMS)
- EM progressiva primária (PPMS)
- MS progressiva secundária (SPMS)
A EM remitente-recorrente é caracterizada por recaídas imprevisíveis seguidas por períodos de meses a anos de relativa calma ( remissão ) sem novos sinais de atividade da doença. Os déficits que ocorrem durante as crises podem resolver ou deixar problemas , este último em cerca de 40% das crises e sendo mais comum quanto mais tempo a pessoa tiver a doença. Isso descreve o curso inicial de 80% dos indivíduos com EM.
O subtipo remitente-recorrente geralmente começa com uma síndrome clinicamente isolada (CIS). No CIS, uma pessoa tem um ataque sugestivo de desmielinização, mas não preenche os critérios para esclerose múltipla. 30 a 70% das pessoas que sofrem de CIS, mais tarde desenvolvem EM.
A EM progressiva primária ocorre em aproximadamente 10-20% dos indivíduos, sem remissão após os sintomas iniciais. Caracteriza-se pela progressão da incapacidade desde o início, com nenhuma, ou apenas ocasionais e pequenas, remissões e melhorias. A idade usual de início para o subtipo progressivo primário é mais tardia do que para o subtipo remitente-recorrente. É semelhante à idade em que a progressiva secundária geralmente se inicia na EM remitente-recorrente, por volta dos 40 anos de idade.
A EM secundária progressiva ocorre em cerca de 65% daqueles com EM inicial remitente-recorrente, que eventualmente apresentam declínio neurológico progressivo entre os ataques agudos sem quaisquer períodos definidos de remissão. Recaídas ocasionais e remissões menores podem aparecer. O período de tempo mais comum entre o início da doença e a conversão de EM recorrente-remitente para EM progressiva secundária é de 19 anos.
A esclerose múltipla se comporta de maneira diferente em crianças, levando mais tempo para atingir o estágio progressivo. No entanto, eles ainda o atingem em uma idade média mais baixa do que os adultos costumam fazer.
A EM de início tardio (LOMS) foi encontrada em um estudo para atingir a incapacidade mais rapidamente do que a EM de início na idade adulta.
Cursos especiais
Independentemente dos tipos publicados pelas associações de MS, agências reguladoras como o FDA costumam considerar cursos especiais, tentando refletir alguns resultados de ensaios clínicos em seus documentos de aprovação. Alguns exemplos podem ser "MS Altamente Ativo" (HAMS), "MS Secundário Ativo" (semelhante ao antigo Progressive-Relapsing) e "PPMS de progressão rápida".
Além disso, quando os déficits sempre se resolvem entre os ataques, isso às vezes é chamado de EM benigna , embora as pessoas ainda desenvolvam algum grau de deficiência a longo prazo. Por outro lado, o termo esclerose múltipla maligna é usado para descrever pessoas com EM que atingiram um nível significativo de incapacidade em um curto período.
Um painel internacional publicou uma definição padronizada para o curso HAMS.
Variantes
Variantes atípicas de EM foram descritas; estes incluem esclerose múltipla tumefativa , esclerose concêntrica de Balo, esclerose difusa de Schilder e esclerose múltipla de Marburg . Há um debate sobre se são variantes da EM ou doenças diferentes. Algumas doenças anteriormente consideradas variantes da EM, como a doença de Devic, agora são consideradas fora do espectro da EM.
Gestão
Embora não haja cura conhecida para a esclerose múltipla, várias terapias provaram ser úteis. Os principais objetivos da terapia são o retorno da função após um ataque, a prevenção de novos ataques e a prevenção de incapacidades. O início de medicamentos geralmente é recomendado em pessoas após o primeiro ataque, quando mais de duas lesões são vistas na ressonância magnética.
Como em qualquer tratamento médico, os medicamentos utilizados no manejo da EM apresentam diversos efeitos adversos . Tratamentos alternativos são procurados por algumas pessoas, apesar da escassez de evidências de eficácia.
Ataques agudos
Durante as crises sintomáticas, a administração de altas doses de corticosteroides intravenosos , como a metilprednisolona , é a terapia usual, com os corticosteroides orais parecendo ter um perfil de eficácia e segurança semelhante. Embora eficazes a curto prazo para aliviar os sintomas, os tratamentos com corticosteroides não parecem ter um impacto significativo na recuperação a longo prazo. O benefício a longo prazo não é claro na neurite óptica a partir de 2020. As consequências de ataques graves que não respondem aos corticosteróides podem ser tratáveis por plasmaférese .
Tratamentos modificadores da doença
Esclerose múltipla remitente recorrente
A partir de 2021, vários medicamentos modificadores da doença são aprovados pelas agências reguladoras para esclerose múltipla recorrente-remitente (EMRR). Eles são interferon beta-1a , interferon beta-1b , acetato de glatirâmero , mitoxantrona , natalizumabe , fingolimode , teriflunomida , fumarato de dimetila , alemtuzumabe , ocrelizumabe , siponimod , cladribina , ozanimod e ponesimod .
Em março de 2017, o FDA aprovou o ocrelizumabe , um anticorpo monoclonal anti - CD20 humanizado , como tratamento para EMRR, com requisitos para vários ensaios clínicos de Fase IV .
No RRMS, eles são modestamente eficazes na redução do número de ataques. Os interferons e o acetato de glatirâmero são tratamentos de primeira linha e são aproximadamente equivalentes, reduzindo as recaídas em aproximadamente 30%. A terapia de longo prazo iniciada precocemente é segura e melhora os resultados. O natalizumab reduz a taxa de recaída mais do que os agentes de primeira linha; no entanto, devido a questões de efeitos adversos é um agente de segunda linha reservado para aqueles que não respondem a outros tratamentos ou com doença grave. A mitoxantrona, cujo uso é limitado por efeitos adversos graves, é uma opção de terceira linha para aqueles que não respondem a outros medicamentos.
O tratamento da síndrome clinicamente isolada (CIS) com interferons diminui a chance de progredir para EM clínica. A eficácia de interferons e acetato de glatirâmero em crianças foi estimada em aproximadamente equivalente à de adultos. O papel de alguns agentes mais novos, como fingolimode, teriflunomida e fumarato de dimetila, ainda não está totalmente claro. É difícil tirar conclusões firmes sobre o melhor tratamento, especialmente em relação ao benefício a longo prazo e à segurança do tratamento precoce, dada a falta de estudos comparando diretamente terapias modificadoras da doença ou monitoramento de longo prazo dos resultados dos pacientes.
A partir de 2017, o rituximab foi amplamente utilizado off-label para tratar EMRR. Há uma falta de ensaios de controle randomizados de alta qualidade examinando rituximabe versus placebo ou outras terapias modificadoras da doença e, como tal, os benefícios do rituximabe para a esclerose múltipla recorrente-remitente permanecem inconclusivos.
A eficácia relativa de diferentes tratamentos não é clara, pois a maioria só foi comparada ao placebo ou a um pequeno número de outras terapias. Comparações diretas de interferons e acetato de glatirâmero indicam efeitos semelhantes ou apenas pequenas diferenças nos efeitos na taxa de recaída, progressão da doença e medidas de ressonância magnética . Alemtuzumab, natalizumab e fingolimode podem ser mais eficazes do que outros medicamentos na redução de recaídas a curto prazo em pessoas com EMRR. Natalizumabe e interferon beta-1a ( Rebif ) podem reduzir as recaídas em comparação com placebo e interferon beta-1a ( Avonex ), enquanto o interferon beta-1b ( Betaseron ), acetato de glatirâmero e mitoxantrona também podem prevenir recaídas. As evidências sobre a eficácia relativa na redução da progressão da incapacidade não são claras. Todos os medicamentos estão associados a efeitos adversos que podem influenciar seus perfis de risco para benefício.
Esclerose múltipla progressiva
A partir de 2011, apenas um medicamento, mitoxantrona, havia sido aprovado para EM secundária progressiva. Nesta população, evidências preliminares apoiam a mitoxantrona retardando moderadamente a progressão da doença e diminuindo as taxas de recaídas ao longo de dois anos.
A partir de 2013, a revisão de 9 imunomoduladores e imunossupressores não encontrou evidências de que nenhum deles fosse eficaz na prevenção da progressão da incapacidade em pessoas com EM progressiva.
Em março de 2017, o FDA aprovou o ocrelizumabe como tratamento para esclerose múltipla progressiva primária em adultos, o primeiro medicamento a obter essa aprovação. com requisitos para vários ensaios clínicos de Fase IV . Também é usado para o tratamento de formas recorrentes de esclerose múltipla, incluindo síndrome clinicamente isolada, doença remitente recorrente e doença progressiva secundária ativa em adultos.
Em 2019, o siponimod e a cladribina foram aprovados nos Estados Unidos para o tratamento da esclerose múltipla progressiva secundária.
Efeitos adversos
Os tratamentos modificadores da doença têm vários efeitos adversos. Uma das mais comuns é a irritação no local da injeção para o acetato de glatirâmero e os interferons (até 90% com injeções subcutâneas e 33% com injeções intramusculares). Ao longo do tempo, pode desenvolver-se um dente visível no local da injeção, devido à destruição local do tecido adiposo, conhecido como lipoatrofia . Os interferons podem produzir sintomas semelhantes aos da gripe ; algumas pessoas que tomam glatirâmer experimentam uma reação pós-injeção com rubor, aperto no peito, palpitações cardíacas e ansiedade, que geralmente dura menos de trinta minutos. Mais perigosos, mas muito menos comuns, são danos hepáticos causados por interferons, disfunção sistólica (12%), infertilidade e leucemia mieloide aguda (0,8%) por mitoxantrona e leucoencefalopatia multifocal progressiva que ocorre com natalizumabe (ocorrendo em 1 em 600 pessoas tratadas).
O fingolimode pode causar hipertensão e diminuição da frequência cardíaca , edema macular , enzimas hepáticas elevadas ou redução nos níveis de linfócitos . Evidências provisórias suportam a segurança a curto prazo da teriflunomida, com efeitos colaterais comuns, incluindo: dores de cabeça, fadiga, náusea, perda de cabelo e dor nos membros. Também houve relatos de insuficiência hepática e LMP com seu uso e é perigoso para o desenvolvimento fetal . Os efeitos colaterais mais comuns do fumarato de dimetila são rubor e problemas gastrointestinais. Embora o fumarato de dimetilo possa levar a uma redução na contagem de glóbulos brancos, não foram notificados casos de infecções oportunistas durante os ensaios.
Sintomas associados
Tanto os medicamentos quanto a neurorreabilitação demonstraram melhorar alguns sintomas, embora nenhum deles altere o curso da doença. Alguns sintomas têm uma boa resposta à medicação, como a espasticidade da bexiga , enquanto outros são pouco alterados. Equipamentos como cateteres para bexiga neurogênica ou auxiliares de mobilidade podem ser úteis para melhorar o estado funcional.
Uma abordagem multidisciplinar é importante para melhorar a qualidade de vida; no entanto, é difícil especificar uma 'equipe principal', pois muitos serviços de saúde podem ser necessários em diferentes momentos. Os programas multidisciplinares de reabilitação aumentam a atividade e a participação das pessoas com EM, mas não influenciam o nível de comprometimento. Estudos que investigam o fornecimento de informações em apoio à compreensão e participação do paciente sugerem que, embora as intervenções (informações escritas, auxílios à decisão, coaching, programas educacionais) possam aumentar o conhecimento, a evidência de um efeito na tomada de decisão e na qualidade de vida é mista e de baixa certeza. Há evidências limitadas para a eficácia geral de disciplinas terapêuticas individuais, embora haja boas evidências de que abordagens específicas, como exercícios e terapias psicológicas, sejam eficazes. O treinamento cognitivo, sozinho ou combinado com outras intervenções neuropsicológicas, pode mostrar efeitos positivos para a memória e a atenção, embora conclusões firmes não sejam atualmente possíveis devido ao pequeno número de amostras, metodologia variável, intervenções e medidas de resultados. A eficácia das abordagens paliativas, além dos cuidados padrão, é incerta, devido à falta de evidências. A eficácia das intervenções, incluindo exercícios, especificamente para a prevenção de quedas em pessoas com EM é incerta, embora haja alguma evidência de um efeito na função de equilíbrio e mobilidade. A terapia comportamental cognitiva mostrou ser moderadamente eficaz para reduzir a fadiga da EM. As evidências para a eficácia de intervenções não farmacológicas para dor crônica são insuficientes para recomendar tais intervenções isoladamente, porém seu uso em combinação com medicamentos pode ser razoável.
Não farmacêutico
Existem algumas evidências de que a terapia aquática é uma intervenção benéfica.
A espasticidade associada à EM pode ser difícil de controlar devido ao curso progressivo e flutuante da doença. Embora não haja uma conclusão firme sobre a eficácia na redução da espasticidade, as intervenções de TP podem ser uma opção segura e benéfica para pacientes com esclerose múltipla. A fisioterapia, incluindo intervenções de vibração, estimulação elétrica, terapia de exercícios, terapia em pé e terapia por ondas de choque radial (RSWT), foram benéficas para limitar a espasticidade, ajudar a limitar a excitabilidade ou aumentar a amplitude de movimento.
Tratamentos alternativos
Mais de 50% das pessoas com EM podem usar medicina complementar e alternativa , embora as porcentagens variem dependendo de como a medicina alternativa é definida. Quanto às características dos usuários, eles são mais frequentemente mulheres, têm SM há mais tempo, tendem a ser mais incapacitados e têm níveis mais baixos de satisfação com os cuidados de saúde convencionais. A evidência para a eficácia de tais tratamentos na maioria dos casos é fraca ou ausente. Os tratamentos de benefício não comprovado usados por pessoas com esclerose múltipla incluem suplementos e regimes alimentares, vitamina D, técnicas de relaxamento como ioga , fitoterapia (incluindo cannabis medicinal ), oxigenoterapia hiperbárica , auto-infecção com ancilostomídeos , reflexologia , acupuntura e atenção plena . Evidências sugerem que a suplementação de vitamina D, independentemente da forma e dose, não traz benefícios para pessoas com EM; isso inclui medidas como recorrência de recaída, incapacidade e lesões de ressonância magnética, enquanto os efeitos na qualidade de vida relacionada à saúde e fadiga não são claros. Não há evidências suficientes que apoiem a biotina em altas doses e algumas evidências de aumento da atividade da doença e maior risco de recaída com seu uso.
Prognóstico

O curso futuro esperado da doença depende do subtipo da doença; sexo, idade e sintomas iniciais do indivíduo; e o grau de deficiência que a pessoa tem. Sexo feminino, subtipo remitente-recorrente, neurite óptica ou sintomas sensoriais no início, poucas crises nos anos iniciais e principalmente na idade de início precoce, estão associados a um melhor curso.
Quase 40% das pessoas com EM atingem a sétima década de vida. No entanto, dois terços das mortes estão diretamente relacionadas às consequências da doença. Infecções e outras complicações são especialmente perigosas para os mais deficientes. Embora a maioria das pessoas perca a capacidade de andar antes da morte, 90% são capazes de andar de forma independente aos 10 anos do início e 75% aos 15 anos.
Epidemiologia
A EM é a doença autoimune mais comum do sistema nervoso central . Em 2010, o número de pessoas com EM era de 2 a 2,5 milhões (aproximadamente 30 por 100.000) em todo o mundo, com taxas variando amplamente em diferentes regiões. Estima-se que tenha resultado em 18.000 mortes naquele ano. Na África, as taxas são inferiores a 0,5 por 100.000, enquanto no Sudeste Asiático são 2,8 por 100.000, 8,3 por 100.000 nas Américas e 80 por 100.000 na Europa. As taxas ultrapassam 200 por 100.000 em certas populações de descendência do norte da Europa. O número de novos casos que se desenvolvem por ano é de cerca de 2,5 por 100.000.
As taxas de MS parecem estar aumentando; isso, no entanto, pode ser explicado simplesmente por um melhor diagnóstico. Estudos sobre padrões populacionais e geográficos têm sido comuns e levaram a uma série de teorias sobre a causa.
A EM geralmente aparece em adultos no final dos vinte ou trinta anos, mas raramente pode começar na infância e após os 50 anos de idade. O subtipo progressivo primário é mais comum em pessoas na casa dos cinquenta. Da mesma forma que muitos distúrbios autoimunes, a doença é mais comum em mulheres, e a tendência pode ser crescente. A partir de 2008, globalmente é cerca de duas vezes mais comum em mulheres do que em homens. Em crianças, é ainda mais comum em mulheres do que em homens, enquanto em pessoas com mais de cinquenta anos, afeta homens e mulheres quase igualmente.
História
Descoberta médica
Robert Carswell (1793–1857), professor britânico de patologia , e Jean Cruveilhier (1791–1873), professor francês de anatomia patológica, descreveram e ilustraram muitos dos detalhes clínicos da doença, mas não a identificaram como uma doença separada. Especificamente, Carswell descreveu as lesões que encontrou como "uma lesão notável da medula espinhal acompanhada de atrofia". Sob o microscópio, o patologista suíço Georg Eduard Rindfleisch (1836-1908) observou em 1863 que as lesões associadas à inflamação estavam distribuídas ao redor dos vasos sanguíneos.
O neurologista francês Jean-Martin Charcot (1825-1893) foi a primeira pessoa a reconhecer a esclerose múltipla como uma doença distinta em 1868. Resumindo relatórios anteriores e acrescentando suas próprias observações clínicas e patológicas, Charcot chamou a doença de esclerose em placas .
Histórico de diagnóstico
A primeira tentativa de estabelecer um conjunto de critérios diagnósticos foi também devido a Charcot em 1868. Ele publicou o que hoje é conhecido como a "Tríade de Charcot", consistindo em nistagmo , tremor de intenção e fala telegráfica (fala de varredura). Charcot também observou mudanças de cognição, descrevendo seus pacientes como tendo um "enfraquecimento acentuado da memória" e "concepções que se formaram lentamente".
O diagnóstico baseava-se na tríade de Charcot e na observação clínica até que Schumacher fez a primeira tentativa de padronizar os critérios em 1965, introduzindo alguns requisitos fundamentais: Disseminação das lesões no tempo (DIT) e no espaço (DIS), e que "sinais e sintomas não podem ser explicados melhor por outro processo de doença". Ambos os requisitos foram posteriormente herdados pelos critérios Poser e McDonald , cuja versão de 2017 está atualmente em uso.
Durante o século 20, teorias sobre a causa e patogênese foram desenvolvidas e tratamentos eficazes começaram a aparecer na década de 1990. Desde o início do século 21, refinamentos dos conceitos ocorreram. A revisão de 2010 dos critérios de McDonald permitiu o diagnóstico de EM com apenas uma lesão comprovada (CIS).
Em 1996, a Sociedade Nacional de Esclerose Múltipla dos EUA (NMSS) (Comitê Consultivo de Ensaios Clínicos) definiu a primeira versão dos fenótipos clínicos atualmente em uso. Nesta primeira versão, eles forneceram definições padronizadas para 4 cursos clínicos da EM: remitente-recorrente (RR), progressiva secundária (SP), progressiva primária (PP) e recidivante progressiva (PR). Em 2010, o PR foi abandonado e a CIS foi incorporada. Posteriormente, três anos depois, a revisão de 2013 dos “fenótipos para o curso da doença” foi forçada a considerar o CIS como um dos fenótipos da EM, tornando obsoletas algumas expressões como “conversão de CIS para EM”. Outras organizações propuseram posteriormente novos fenótipos clínicos, como HAMS (Highly Active MS) como resultado do trabalho em processos de aprovação de DMT.
Casos históricos

Existem vários relatos históricos de pessoas que provavelmente tiveram EM e viveram antes ou logo após a doença ser descrita por Charcot.
Uma jovem chamada Halldora, que viveu na Islândia por volta de 1200, de repente perdeu a visão e a mobilidade, mas as recuperou sete dias depois. Santa Lidwina de Schiedam (1380-1433), uma freira holandesa , pode ser uma das primeiras pessoas claramente identificáveis com EM. Dos 16 anos até sua morte aos 53 anos, ela teve dores intermitentes, fraqueza nas pernas e perda de visão: sintomas típicos da EM. Ambos os casos levaram à proposta de uma hipótese de "gene Viking" para a disseminação da doença.
Augustus Frederick d'Este (1794-1848), filho do príncipe Augustus Frederick, duque de Sussex e Lady Augusta Murray e neto de George III do Reino Unido , quase certamente tinha EM. D'Este deixou um diário detalhado descrevendo seus 22 anos vivendo com a doença. Seu diário começou em 1822 e terminou em 1846, embora tenha permanecido desconhecido até 1948. Seus sintomas começaram aos 28 anos com uma súbita perda visual transitória ( amaurose fugaz ) após o funeral de um amigo. Durante sua doença, ele desenvolveu fraqueza nas pernas, falta de jeito das mãos, dormência, tontura, distúrbios da bexiga e disfunção erétil . Em 1844, ele começou a usar uma cadeira de rodas. Apesar de sua doença, ele manteve uma visão otimista da vida. Outro relato inicial de EM foi mantido pelo diarista britânico WNP Barbellion , pseudônimo de Bruce Frederick Cummings (1889-1919), que manteve um registro detalhado de seu diagnóstico e luta. Seu diário foi publicado em 1919 como The Journal of a Disappointed Man .
Pesquisar
Vírus Epstein-Barr como causa
O vírus Epstein-Barr (EBV), um vírus do herpes que pode causar mononucleose infecciosa e infectar aproximadamente 95% dos adultos, tem sido cada vez mais suspeito de ser a causa primária da EM, embora apenas uma proporção muito pequena dos infectados com EBV venha a desenvolver mais tarde SENHORA. Um estudo de indivíduos nas forças armadas dos Estados Unidos entre 1993 e 2013 (população total superior a 10 milhões) comparou 801 pessoas que desenvolveram EM durante ou após o serviço militar com 1.566 controles pareados que não desenvolveram EM durante esse período de observação. O estudo encontrou um risco 32 vezes maior de desenvolver EM após a infecção pelo EBV. Ele não encontrou um risco aumentado após a infecção por outros vírus, incluindo o citomegalovírus transmitido de forma semelhante . A descoberta foi estatisticamente altamente significativa ( P = 0,001), sugerindo que o EBV pode ser uma das principais causas de EM. Um mecanismo hipotético do EBV causando EM é o mimetismo molecular entre as proteínas do EBV e as moléculas do sistema nervoso, causando autoimunidade.
Medicamentos
Medicamentos que influenciam os canais de íons de sódio dependentes de voltagem estão sob investigação como uma potencial estratégia neuroprotetora devido ao papel hipotético do sódio no processo patológico que leva à lesão axonal e ao acúmulo de incapacidade. Atualmente, não há evidências suficientes de um efeito dos bloqueadores dos canais de sódio para pessoas com EM.
Patogênese
A EM é uma entidade clinicamente definida com várias apresentações atípicas. Alguns auto-anticorpos foram encontrados em casos atípicos de EM, dando origem a famílias de doenças separadas e restringindo o conceito anteriormente mais amplo de EM.
Em primeiro lugar, autoanticorpos anti-AQP4 foram encontrados na neuromielite óptica (NMO), que anteriormente era considerada uma variante da EM. Depois disso, todo um espectro de doenças chamado NMOSD (doenças do espectro NMO) ou doenças anti-AQP4 foi aceito.
Posteriormente, verificou-se que alguns casos de EM apresentavam autoanticorpos anti-MOG , principalmente sobrepostos à variante de Marburg . Autoanticorpos anti-MOG também estão presentes na ADEM, e agora um segundo espectro de doenças separadas está sendo considerado. Neste momento, é nomeado de forma inconsistente entre diferentes autores, mas normalmente é algo semelhante a doenças desmielinizantes anti-MOG .
Finalmente, um terceiro tipo de auto-anticorpos é aceito. São vários auto-anticorpos anti-neurofascina que danificam os nódulos de Ranvier dos neurônios. Esses anticorpos estão mais relacionados à desmielinização nervosa periférica, mas também foram encontrados na EMPP crônica progressiva e na desmielinização central e periférica combinada (DCPD, que é considerada outra apresentação atípica da EM).
Além da importância dos autoanticorpos na EM, quatro padrões diferentes de desmielinização foram relatados, abrindo a porta para considerar a EM como uma doença heterogênea .
Biomarcadores de doenças
Uma vez que a progressão da doença é o resultado da degeneração dos neurônios, os papéis das proteínas que mostram a perda de tecido nervoso, como neurofilamentos , tau e N-acetilaspartato, estão sob investigação.
A melhoria nas técnicas de neuroimagem, como a tomografia por emissão de pósitrons (PET) ou a ressonância magnética (MRI), trazem uma promessa para melhores previsões de diagnóstico e prognóstico. Em relação à RM, existem várias técnicas que já mostraram alguma utilidade em ambientes de pesquisa e podem ser introduzidas na prática clínica, como sequências de recuperação de dupla inversão, transferência de magnetização , tensor de difusão e ressonância magnética funcional . Essas técnicas são mais específicas para a doença do que as existentes, mas ainda carecem de alguma padronização de protocolos de aquisição e criação de valores normativos. Este é particularmente o caso da espectroscopia de ressonância magnética de prótons , para a qual várias variações metodológicas observadas na literatura podem estar subjacentes a inconsistências contínuas em anormalidades metabólicas do sistema nervoso central, particularmente em N-acetil aspartato , mioinositol , colina , glutamato , GABA e GSH , observado para esclerose múltipla e seus subtipos. Existem outras técnicas em desenvolvimento que incluem agentes de contraste capazes de medir níveis de macrófagos periféricos , inflamação ou disfunção neuronal, e técnicas que medem a deposição de ferro que poderiam servir para determinar o papel dessa característica na EM ou da perfusão cerebral.
COVID-19
A taxa de hospitalização foi maior entre os indivíduos com esclerose múltipla e infecção por COVID-19, em 10%, enquanto a taxa de infecção combinada é estimada em 4%. A prevalência combinada de morte em indivíduos hospitalizados com EM é estimada em 4%.