N- Bromossuccinimida - N-Bromosuccinimide
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
1-bromopirrolidina-2,5-diona |
|||
| Outros nomes
N- bromossuccinimida; NBS
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 113916 | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard |
100,004,435 |
||
| Número EC | |||
| 26634 | |||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 4 H 4 Br N O 2 | |||
| Massa molar | 177,985 g · mol −1 | ||
| Aparência | Sólido branco | ||
| Densidade | 2,098 g / cm 3 (sólido) | ||
| Ponto de fusão | 175 a 178 ° C (347 a 352 ° F; 448 a 451 K) | ||
| Ponto de ebulição | 339 ° C (642 ° F; 612 K) | ||
| 14,7 g / L (25 ° C) | |||
| Solubilidade em CCl 4 | Insolúvel (25 ° C) | ||
| Perigos | |||
| Riscos principais | Irritante | ||
| Ficha de dados de segurança | [1] | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
N- bromossuccinimida ou NBS é um reagente químico usado em reações de substituição radical , adição eletrofílica e substituição eletrofílica em química orgânica . NBS pode ser uma fonte conveniente de Br • , oradical de bromo .
Preparação
O NBS está disponível comercialmente. Também pode ser sintetizado em laboratório. Para fazer isso, hidróxido de sódio e bromo são adicionados a uma solução de succinimida em água gelada . O produto NBS precipita e pode ser coletado por filtração.
NBS bruto dá melhor rendimento na reação de Wohl-Ziegler . Em outros casos, NBS impuro (levemente amarelado) pode dar resultados não confiáveis. Ele pode ser purificado por recristalização em água a 90–95 ° C (10 g de NBS para 100 mL de água).
Reações
Adição a alcenos
NBS irá reagir com alcenos 1 em solventes aquosos para dar bromo-hidrinas 2 . As condições preferidas são a adição em porções de NBS a uma solução do alceno em DMSO , DME , THF ou terc- butanol aquoso a 50% a 0 ° C. A formação de um íon bromônio e o ataque imediato pela água dão forte adição de Markovnikov e seletividades anti- estereoquímicas.
As reações colaterais incluem a formação de α-bromocetonas e compostos dibromo. Isso pode ser minimizado pelo uso de NBS recristalizado .
Com a adição de nucleófilos , em vez de água , vários alcanos bifuncionais podem ser sintetizados.
Brominação alílica e benzílica
As condições padrão para o uso de NBS em brominação alílica e / ou benzílica envolve o refluxo de uma solução de NBS em CCl 4 anidro com um iniciador radical - geralmente azobisisobutironitrila ( AIBN ) ou peróxido de benzoíla , irradiação ou ambos para efetuar a iniciação radical . Os intermediários de radicais alílicos e benzílicos formados durante esta reação são mais estáveis do que outros radicais de carbono e os principais produtos são os brometos alílicos e benzílicos. Isso também é chamado de reação Wohl-Ziegler .
O tetracloreto de carbono deve ser mantido anidro ao longo da reação, pois a presença de água pode provavelmente hidrolisar o produto desejado. O carbonato de bário é frequentemente adicionado para manter as condições anidras e sem ácido.
Na reação acima, embora uma mistura de produtos isoméricos de brometo alílico seja possível, apenas um é criado devido à maior estabilidade do radical na posição 4 sobre o radical centrado em metil.
Brominação de derivados de carbonil
NBS pode α-bromar derivados de carbonil por meio de uma via radical (como acima) ou via catálise ácida. Por exemplo, cloreto de hexanoílo 1 pode ser bromado na posição alfa por NBS usando catálise ácida.
A reação de enolatos , enol éteres ou enol acetatos com NBS é o método preferido de α-bromação, pois é de alto rendimento com poucos produtos colaterais.
Brominação de derivados aromáticos
Compostos aromáticos ricos em elétrons , como fenóis , anilinas e vários heterociclos aromáticos , podem ser bromados usando NBS. Usar DMF como solvente dá altos níveis de para-seletividade.
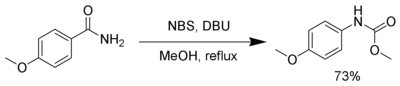
Reorganização de Hofmann
O NBS, na presença de uma base forte, como DBU , reage com amidas primárias para produzir um carbamato por meio do rearranjo de Hofmann .
Oxidação seletiva de álcoois
É incomum, mas é possível que o NBS oxide álcoois. EJ Corey et al. descobriram que se pode oxidar seletivamente álcoois secundários na presença de álcoois primários usando NBS em dimetoxietano aquoso (DME).
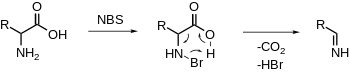
Descarboxilação oxidativa de α-aminoácidos
O NBS broma eletrof ilicamente a amina, que é seguida pela descarboxilação e liberação de uma imina. A hidrólise adicional produzirá um aldeído e amônia. (cf. descarboxilação dependente de PLP não oxidativa)
Precauções
Embora o NBS seja mais fácil e seguro de manusear do que o bromo, devem ser tomadas precauções para evitar a inalação. NBS deve ser armazenado em um refrigerador. O NBS se decompõe com o tempo, liberando bromo. O NBS puro é branco, mas é frequentemente encontrado para ser esbranquiçado ou de cor marrom pelo bromo.
Em geral, as reações envolvendo NBS são exotérmicas. Portanto, precauções extras devem ser tomadas quando usado em grande escala.