1-Butanol - 1-Butanol
|
|
|||
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Butan-1-ol |
|||
| Outros nomes
n -Butanol
n -butil álcool n -Butil hidróxido n -Propylcarbinol n -Propylmethanol 1-hidroxibutano Methylolpropane |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 3DMet | |||
| 969148 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard |
100.000.683 |
||
| Número EC | |||
| 25753 | |||
| KEGG | |||
| Malha | 1-butanol | ||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 1120 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 4 H 10 O | |||
| Massa molar | 74,123 g · mol −1 | ||
| Aparência | Líquido incolor, refrativo | ||
| Odor | tipo banana , áspera, alcoólica e doce | ||
| Densidade | 0,81 g / cm 3 | ||
| Ponto de fusão | −89,8 ° C (−129,6 ° F; 183,3 K) | ||
| Ponto de ebulição | 117,7 ° C (243,9 ° F; 390,8 K) | ||
| 73 g / L a 25 ° C | |||
| Solubilidade | muito solúvel em acetona miscível com etanol , éter etílico |
||
| log P | 0,839 | ||
| Pressão de vapor | 0,58 kPa (20 ° C) ILO International Chemical Safety Cards (ICSC) | ||
| Acidez (p K a ) | 16,10 | ||
| −56,536 · 10 −6 cm 3 / mol | |||
|
Índice de refração ( n D )
|
1,3993 (20 ° C) | ||
| Viscosidade | 2,573 mPa · s (a 25 ° C) | ||
| 1,66 D | |||
| Termoquímica | |||
|
Entropia molar padrão ( S |
225,7 J / (K · mol) | ||
| -328 (4) kJ / mol | |||
| -2670 (20) kJ / mol | |||
| Perigos | |||
| Ficha de dados de segurança | ICSC 0111 | ||
| Pictogramas GHS |
  
|
||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | 35 ° C (95 ° F; 308 K) | ||
| 343 ° C (649 ° F; 616 K) | |||
| Limites explosivos | 1,45-11,25% | ||
| Dose ou concentração letal (LD, LC): | |||
|
LD 50 ( dose mediana )
|
790 mg / kg (rato, oral) | ||
|
LD Lo (o mais baixo publicado )
|
3484 mg / kg (coelho, oral) 790 mg / kg (rato, oral) 1700 mg / kg (cão, oral) |
||
|
LC 50 ( concentração média )
|
9221 ppm (mamífero) 8000 ppm (rato, 4 h ) |
||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
TWA 100 ppm (300 mg / m 3 ) | ||
|
REL (recomendado)
|
C 50 ppm (150 mg / m 3 ) [pele] | ||
|
IDLH (perigo imediato)
|
1400 ppm | ||
| Compostos relacionados | |||
|
Compostos relacionados
|
Butanotiol n -butilamina dietil éter Pentano |
||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
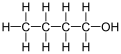
Butan-1-ol , também conhecido como n-butanol é um álcool primário com a fórmula química C 4 H 9 OH e uma estrutura linear. Os isômeros de butan-1-ol são isobutanol , butan-2-ol e terc- butanol . O butanol termo não modificado geralmente se refere ao isômero de cadeia linear.
O 1-butanol ocorre naturalmente como um produto secundário da fermentação do etanol de açúcares e outros sacarídeos e está presente em muitos alimentos e bebidas. Também é um aromatizante artificial permitido nos Estados Unidos, usado em manteiga, creme, frutas, rum, uísque, sorvetes e gelados, doces, assados e cordiais. Também é usado em uma ampla gama de produtos de consumo.
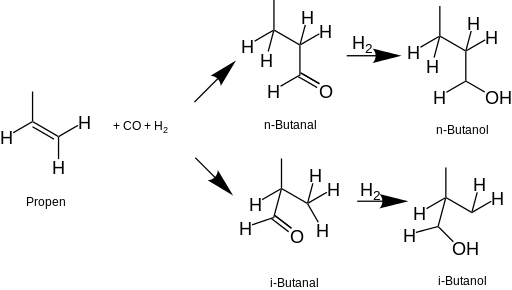
O maior uso do 1-butanol é como intermediário industrial, particularmente para a fabricação de acetato de butila (ele próprio um aromatizante artificial e solvente industrial). É um produto petroquímico derivado do propeno . Os números de produção estimados para 1997 são: Estados Unidos 784.000 toneladas; Europa Ocidental 575.000 toneladas; Japão 225.000 toneladas.
Produção
Desde a década de 1950, a maior parte do 1-butanol é produzida pela hidroformilação do propeno (processo oxo) para formar preferencialmente o butiraldeído n-butanal. Os catalisadores típicos são baseados em cobalto e ródio. O butiraldeído é então hidrogenado para produzir butanol.
Um segundo método para a produção de butanol envolve a reação Reppe de propileno com CO e água:
- CH 3 CH = CH 2 + H 2 O + 2 CO → CH 3 CH 2 CH 2 CH 2 OH + CO 2
Antigamente, o butanol era preparado a partir do crotonaldeído , que pode ser obtido a partir do acetaldeído .
O butanol também pode ser produzido pela fermentação da biomassa por bactérias. Antes da década de 1950, o Clostridium acetobutylicum era usado na fermentação industrial para produzir butanol. Pesquisas nas últimas décadas mostraram resultados de outros microrganismos que podem produzir butanol por fermentação.
Uso industrial
Constituindo 85% do seu uso, o 1-butanol é utilizado principalmente na produção de vernizes . É um solvente popular, por exemplo, para nitrocelulose . Uma variedade de ésteres butílicos são usados como solventes, por exemplo, butoxietanol . Muitos plastificantes são baseados em ésteres de butila, por exemplo, dibutil ftalato . O monômero butil acrilato é usado para produzir polímeros. É o precursor das n-butilaminas .
Biocombustível
O 1-butanol foi proposto como substituto do óleo diesel e da gasolina . É produzido em pequenas quantidades em quase todas as fermentações (ver óleo fúsel ). Clostridium produz rendimentos muito maiores de butanol. A pesquisa está em andamento para aumentar o rendimento do biobutanol a partir da biomassa .
O butanol é considerado um biocombustível potencial ( combustível butanol ). O butanol na concentração de 85 por cento pode ser usado em carros projetados para gasolina sem qualquer alteração no motor (ao contrário do etanol 85%), e fornece mais energia para um determinado volume do que o etanol, devido ao menor teor de oxigênio do butanol, e quase tanto quanto Gasolina. Portanto, um veículo com butanol retornaria o consumo de combustível mais comparável à gasolina do que ao etanol. O butanol também pode ser adicionado ao óleo diesel para reduzir as emissões de fuligem.
A produção ou, em alguns casos, o uso das seguintes substâncias pode resultar na exposição ao 1-butanol: couro artificial , ésteres de butila , cimento de borracha , tintas, essências de frutas, lacas, filmes e filmes fotográficos, capas de chuva, perfumes, plásticos de piroxilina , rayon , vidro de segurança, verniz de goma-laca e pano impermeabilizado.
Ocorrência na natureza
O butan-1-ol ocorre naturalmente como resultado da fermentação de carboidratos em várias bebidas alcoólicas, incluindo cerveja, conhaque de uva, vinho e uísque. Foi detectado nos compostos voláteis de lúpulo, jaca, leites tratados termicamente, melão almiscarado, queijo, semente de ervilha do sul e arroz cozido. O 1-butanol também é formado durante a fritura profunda de óleo de milho, óleo de semente de algodão, trilinoleína e trioleína.
Butan-1-ol é um dos " álcoois fusel " (do alemão para "licor ruim"), que inclui álcoois que têm mais de dois átomos de carbono e têm solubilidade significativa em água. É um componente natural de muitas bebidas alcoólicas, embora em concentrações baixas e variáveis. Ele (junto com álcoois fusel semelhantes) é considerado responsável por ressacas severas , embora experimentos em modelos animais não mostrem evidências disso.
O 1-butanol é usado como ingrediente em aromas processados e artificiais e para a extração de proteína livre de lipídios da gema de ovo, materiais aromatizantes naturais e óleos vegetais, na fabricação de extrato de lúpulo para fabricação de cerveja e como solvente na remoção de pigmentos de concentrado de proteína de folha de coalhada úmida .
Metabolismo e toxicidade
A toxicidade aguda do 1-butanol é relativamente baixa, com valores de DL 50 orais de 790–4.360 mg / kg (rato; valores comparáveis para o etanol são 7.000–15.000 mg / kg). É metabolizado completamente em vertebrados de maneira semelhante ao etanol : a álcool desidrogenase converte 1-butanol em butiraldeído ; este é então convertido em ácido butírico pela aldeído desidrogenase . O ácido butírico pode ser totalmente metabolizado em dióxido de carbono e água pela via de β-oxidação . No rato, apenas 0,03% de uma dose oral de 2.000 mg / kg foi excretada na urina. Em doses subletais, o 1-butanol atua como depressor do sistema nervoso central , semelhante ao etanol: um estudo em ratos indicou que a potência intoxicante do 1-butanol é cerca de 6 vezes maior do que a do etanol, possivelmente por causa de sua transformação mais lenta por álcool desidrogenase.
Outros perigos
O 1-butanol líquido, como é comum com a maioria dos solventes orgânicos, é extremamente irritante para os olhos; o contato repetido com a pele também pode causar irritação. Acredita-se que este seja um efeito genérico de "desengorduramento". Não foi observada sensibilização da pele. A irritação das vias respiratórias ocorre apenas em concentrações muito altas (> 2.400 ppm).
Com um ponto de inflamação de 35 ° C, o 1-butanol apresenta um risco moderado de incêndio: é ligeiramente mais inflamável do que o querosene ou o óleo diesel, mas menos inflamável do que muitos outros solventes orgânicos comuns. O efeito depressor no sistema nervoso central (semelhante à intoxicação por etanol) é um perigo potencial ao trabalhar com 1-butanol em espaços fechados, embora o limiar de odor (0,2-30 ppm) esteja muito abaixo da concentração que teria qualquer efeito neurológico.
Veja também
links externos
- Cartão Internacional de Segurança Química 0111
- Guia de bolso do NIOSH para perigos químicos. "# 0076" . Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH).
- Relatório de avaliação inicial do SIDS para n- butanol da Organização para Cooperação e Desenvolvimento Econômico (OCDE)
- Critérios de saúde ambiental 65 do IPCS : Butanóis: quatro isômeros
- Guia de saúde e segurança do IPCS 3: 1-butanol