Nitrato de níquel (II) - Nickel(II) nitrate
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Nitrato de níquel (II)
|
|
| Outros nomes
Nitrato de níquel Nitrato de níquel
Ácido nítrico, sal de níquel (2+) |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.032.774 |
| Número EC | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| Ni (NO 3 ) 2 | |
| Massa molar | 182,703 g / mol (anidro) 290,79 g / mol (hexahidrato) |
| Aparência | sólido higroscópico verde esmeralda |
| Odor | inodoro |
| Densidade | 2,05 g / cm 3 (hexahidrato) |
| Ponto de fusão | 56,7 ° C (134,1 ° F; 329,8 K) (hexahidrato) |
| Ponto de ebulição | 136,7 ° C (278,1 ° F; 409,8 K) (hexahidrato) |
| 243 (hexahidrato) g / 100ml (0 ° C) | |
| Solubilidade | solúvel em etanol |
| + 4300,0 · 10 −6 cm 3 / mol (+6 H 2 O) | |
|
Índice de refração ( n D )
|
1,422 (hexahidrato) |
| Estrutura | |
| monoclínico (hexahidrato) | |
| Perigos | |
| Ficha de dados de segurança | MSDS externo |
| Oxidante ( O ) Carc. Gato. 1 Muta. Gato. 3 Repr. Gato. 2 Tóxico ( T ) Nocivo ( Xn ) Irritante ( Xi ) Perigoso para o meio ambiente ( N ) |
|
| Frases R (desatualizado) | R49 , R61 , R8 , R20 / 22 , R38 , R41 , R42 / 43 , R48 / 23 , R68 , R50 / 53 |
| Frases S (desatualizado) | S53 , S45 , S60 , S61 |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
1620 mg / kg (oral, rato) |
| Compostos relacionados | |
|
Outros ânions
|
Sulfato de níquel (II) Cloreto de níquel (II) |
|
Outros cátions
|
Nitrato de paládio (II) |
|
Compostos relacionados
|
Nitrato de cobalto (II) Nitrato de cobre (II) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
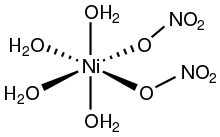
Nitrato de níquel é o composto inorgânico Ni (NO 3 ) 2 ou qualquer hidrato deste. A forma anidra não é comumente encontrada, portanto, "nitrato de níquel" geralmente se refere ao nitrato de níquel (II) hexa-hidratado . A fórmula para esta espécie é escrita de duas maneiras: Ni (NO 3 ) 2 . 6H 2 O e, mais descritivamente [Ni (H 2 O) 6 ] (NO 3 ) 2 . A última fórmula indica que o centro de níquel (II) está rodeado por seis moléculas de água neste sal hidratado. No hexahidrato, os ânions nitrato não estão ligados ao níquel. Também são conhecidos três outros hidratos: Ni (NO 3 ) 2 . 9H 2 O, Ni (NO 3 ) 2 . 4H 2 O e Ni (NO 3 ) 2 . 2H 2 O. Ni anidro (NO 3 ) 2 também é conhecido.
É preparado pela reação do óxido de níquel com ácido nítrico:
- NiO + 2 HNO 3 + 5 H 2 O → Ni (NO 3 ) 2 . 6H 2 O
O nitrato de níquel anidro normalmente não é preparado pelo aquecimento dos hidratos. Em vez disso, é gerado pela reação de hidratos com pentóxido de dinitrogênio ou de carbonil de níquel com tetróxido de dinitrogênio :
- Ni (CO) 4 + 2 N 2 O 4 → Ni (NO 3 ) 2 + 2 NO + 4 CO
O nitrato hidratado é frequentemente usado como um precursor de catalisadores de níquel com suporte .
Estrutura
Compostos de níquel (II) com ligantes oxigenados geralmente apresentam geometria de coordenação octaédrica. Dois polimorfos do tetrahidrato Ni (NO 3 ) 2 . 4H 2 O foram cristalizados. Em um, os ligantes nitrato monodentados são trans, enquanto no outro são cis.
Segurança
Como outros nitratos, o nitrato de níquel é oxidante . Também é irritante para os olhos, pele e, após a inalação do pó, para o trato respiratório . Pode causar alergia na pele . O nitrato de níquel é cancerígeno , junto com a maioria dos outros compostos de níquel. O íon níquel também é tóxico para organismos aquáticos.
Usos
O nitrato de níquel (II) é usado principalmente na eletrotipagem e galvanoplastia de níquel metálico.

