Bateria de níquel-cádmio - Nickel–cadmium battery
 De cima para baixo: pilhas "Gumstick", AA e AAA Ni – Cd
| |
| Energia especifica | 40–60 W · h / kg |
|---|---|
| Densidade de energia | 50-150 W · h / L |
| Poder específico | 150 W / kg |
| Eficiência de carga / descarga | 70–90% |
| Taxa de autodescarga | 10% / mês |
| Durabilidade do ciclo | 2.000 ciclos |
| Tensão nominal da célula | 1,2 V |
A bateria de níquel-cádmio ( bateria Ni-Cd ou bateria NiCad ) é um tipo de bateria recarregável que usa hidróxido de óxido de níquel e cádmio metálico como eletrodos . A abreviatura Ni-Cd é derivada dos símbolos químicos de níquel (Ni) e cádmio (Cd): a abreviatura NiCad é uma marca registrada da SAFT Corporation , embora este nome de marca seja comumente usado para descrever todas as baterias Ni – Cd.
As baterias de níquel-cádmio de célula úmida foram inventadas em 1899. Uma bateria de Ni-Cd tem uma tensão terminal durante a descarga de cerca de 1,2 volts, que diminui pouco até quase o final da descarga. A força eletromotriz máxima oferecida por uma célula Ni-Cd é de 1,3 V. As baterias Ni-Cd são feitas em uma ampla gama de tamanhos e capacidades, de tipos portáteis selados intercambiáveis com células secas de carbono-zinco, a grandes células ventiladas usadas para energia de reserva e força motriz. Comparadas com outros tipos de células recarregáveis, elas oferecem bom ciclo de vida e desempenho em baixas temperaturas com uma capacidade razoável, mas sua vantagem significativa é a capacidade de fornecer praticamente sua capacidade nominal total em altas taxas de descarga (descarregando em uma hora ou menos). No entanto, os materiais são mais caros do que os da bateria de chumbo-ácido e as células têm altas taxas de autodescarga.
As células seladas de Ni-Cd já foram amplamente utilizadas em ferramentas elétricas portáteis, equipamentos fotográficos, lanternas , iluminação de emergência, RC de passatempo e dispositivos eletrônicos portáteis. A capacidade superior das baterias de níquel-hidreto metálico e o custo mais baixo recente suplantaram amplamente o uso de Ni-Cd. Além disso, o impacto ambiental da eliminação do cádmio metálico tóxico contribuiu consideravelmente para a redução do seu uso. Na União Europeia, as baterias Ni-Cd agora podem ser fornecidas apenas para fins de substituição ou para certos tipos de novos equipamentos, como dispositivos médicos.
Baterias maiores de Ni-Cd de célula úmida ventiladas são usadas em iluminação de emergência, energia em espera e fontes de alimentação ininterrupta e outras aplicações.
História
A primeira bateria de Ni – Cd foi criada por Waldemar Jungner da Suécia em 1899. Naquela época, o único competidor direto era a bateria de chumbo-ácido , que era menos robusta física e quimicamente. Com pequenas melhorias nos primeiros protótipos, a densidade de energia aumentou rapidamente para cerca de metade da das baterias primárias e significativamente maior do que as baterias de chumbo-ácido. Jungner experimentou substituir o cádmio pelo ferro em quantidades variáveis, mas descobriu que as formulações de ferro eram insuficientes. O trabalho de Jungner era amplamente desconhecido nos Estados Unidos. Thomas Edison patenteou uma bateria de níquel ou cobalto-cádmio em 1902 e adaptou o projeto da bateria quando introduziu a bateria de níquel-ferro nos Estados Unidos, dois anos depois de Jungner ter construído uma. Em 1906, Jungner estabeleceu uma fábrica perto de Oskarshamn, na Suécia, para produzir baterias de Ni – Cd de design inundado.
Em 1932, os materiais ativos foram depositados dentro de um eletrodo poroso folheado a níquel e quinze anos depois começou o trabalho em uma bateria selada de níquel-cádmio.
A primeira produção nos Estados Unidos começou em 1946. Até este ponto, as baterias eram do tipo "bolso", construídas com bolsas de aço niquelado contendo materiais ativos de níquel e cádmio . Em meados do século XX, as baterias de Ni – Cd de placa sinterizada tornaram-se cada vez mais populares. A fusão do pó de níquel em uma temperatura bem abaixo de seu ponto de fusão usando altas pressões cria placas sinterizadas. As placas assim formadas são altamente porosas, cerca de 80 por cento em volume. As placas positivas e negativas são produzidas embebendo as placas de níquel em materiais ativos de níquel e cádmio, respectivamente. As placas sinterizadas são geralmente muito mais finas do que as do tipo bolsão, resultando em maior área de superfície por volume e correntes mais altas. Em geral, quanto maior for a área de superfície de material reativo em uma bateria, menor será sua resistência interna .
Desde a década de 2000, todas as baterias de Ni – Cd de consumo usam a configuração de rolo de gelatina .
Características
A taxa máxima de descarga de uma bateria Ni – Cd varia de acordo com o tamanho. Para uma célula de tamanho AA comum , a taxa de descarga máxima é de aproximadamente 1,8 amperes; para uma bateria de tamanho D, a taxa de descarga pode chegar a 3,5 amperes.
Os construtores de aeromodelismo ou barco muitas vezes usam correntes muito maiores de até cem amperes ou mais de baterias de Ni – Cd especialmente construídas, que são usadas para acionar os motores principais. 5–6 minutos de operação do modelo são facilmente alcançáveis com baterias bem pequenas, então um valor de potência / peso razoavelmente alto é alcançado, comparável aos motores de combustão interna , embora de menor duração. Neste, entretanto, eles foram amplamente substituídos por baterias de polímero de lítio (Lipo) e fosfato de ferro de lítio (LiFe), que podem fornecer densidades de energia ainda mais altas.
Voltagem
As células Ni – Cd têm um potencial de célula nominal de 1,2 volts (V). Isso é inferior a 1,5 V das células primárias alcalinas e de zinco-carbono e, conseqüentemente, não são adequadas como substitutas em todas as aplicações. No entanto, o 1,5 V de uma pilha alcalina primária se refere à sua voltagem inicial, e não à média. Ao contrário das células primárias alcalinas e de zinco-carbono, a voltagem terminal de uma célula Ni-Cd muda apenas um pouco à medida que descarrega. Como muitos dispositivos eletrônicos são projetados para funcionar com células primárias que podem descarregar até 0,90 a 1,0 V por célula, os 1,2 V relativamente estáveis de uma célula de Ni – Cd são suficientes para permitir a operação. Alguns consideram a tensão quase constante uma desvantagem, pois torna difícil detectar quando a carga da bateria está baixa.
As baterias Ni – Cd usadas para substituir as baterias de 9 V geralmente têm apenas seis células, para uma tensão terminal de 7,2 volts. Embora a maioria dos rádios de bolso funcione satisfatoriamente com esta voltagem, alguns fabricantes, como a Varta, fabricaram baterias de 8,4 volts com sete células para aplicações mais críticas.
Carregando
As baterias Ni – Cd podem ser carregadas em várias taxas diferentes, dependendo de como a célula foi fabricada. A taxa de carga é medida com base na porcentagem da capacidade de amp-hora com a qual a bateria é alimentada como uma corrente constante ao longo da duração da carga. Independentemente da velocidade de carga, mais energia deve ser fornecida à bateria do que sua capacidade real, para compensar a perda de energia durante o carregamento, com cargas mais rápidas sendo mais eficientes. Por exemplo, uma carga "durante a noite" pode consistir no fornecimento de uma corrente igual a um décimo da classificação ampere-hora (C / 10) por 14–16 horas; ou seja, uma bateria de 100 mAh leva 10 mA por 14 horas, para um total de 140 mAh para carregar nessa taxa. Na taxa de carga rápida, feita a 100% da capacidade nominal da bateria em 1 hora (1C), a bateria retém cerca de 80% da carga, então uma bateria de 100 mAh leva 125 mAh para carregar (ou seja, aproximadamente 1 hora e quinze minutos). Algumas baterias especializadas podem ser carregadas em até 10-15 minutos a uma taxa de carga de 4C ou 6C, mas isso é muito incomum. Também aumenta muito o risco de superaquecimento e ventilação das células devido a uma condição de sobrepressão interna: a taxa de aumento de temperatura da célula é governada por sua resistência interna e pelo quadrado da taxa de carga. A uma taxa de 4 ° C, a quantidade de calor gerada na célula é dezesseis vezes maior do que o calor à taxa de 1 ° C. A desvantagem de um carregamento mais rápido é o maior risco de sobrecarga, o que pode danificar a bateria. e o aumento da temperatura que a célula tem de suportar (o que potencialmente encurta sua vida).
A faixa de temperatura segura quando em uso é entre −20 ° C e 45 ° C. Durante o carregamento, a temperatura da bateria normalmente permanece baixa, em torno da mesma que a temperatura ambiente (a reação de carregamento absorve energia), mas à medida que a bateria se aproxima da carga completa, a temperatura sobe para 45–50 ° C. Alguns carregadores de bateria detectam esse aumento de temperatura para interromper o carregamento e evitar o carregamento excessivo.
Quando não está sob carga ou carga, uma bateria de Ni – Cd se autodescarrega aproximadamente 10% por mês a 20 ° C, variando até 20% por mês em temperaturas mais altas. É possível realizar uma carga lenta em níveis de corrente altos o suficiente para compensar essa taxa de descarga; para manter a bateria totalmente carregada. No entanto, se a bateria for armazenada sem uso por um longo período de tempo, ela deve ser descarregada até no máximo 40% da capacidade (alguns fabricantes recomendam descarregar totalmente e até mesmo entrar em curto-circuito depois de totalmente descarregada) e armazenada em um ambiente fresco e seco.
Sobrecarregando
As células seladas de Ni – Cd consistem em um vaso de pressão que supostamente contém qualquer geração de gases de oxigênio e hidrogênio até que eles possam se recombinar de volta à água. Essa geração ocorre normalmente durante a carga e descarga rápidas e excessivamente na condição de sobrecarga. Se a pressão ultrapassar o limite da válvula de segurança, a água na forma de gás é perdida. Como o vaso é projetado para conter uma quantidade exata de eletrólito, essa perda afetará rapidamente a capacidade da célula e sua capacidade de receber e fornecer corrente. Detectar todas as condições de sobrecarga exige grande sofisticação do circuito de carga e um carregador barato acabará por danificar até mesmo as células de melhor qualidade.
Eletroquímica
Uma célula Ni-Cd totalmente carregada contém:
- uma placa de eletrodo positivo de óxido-hidróxido de níquel (III)
- uma placa de eletrodo negativo de cádmio
- um separador e
- um eletrólito alcalino ( hidróxido de potássio ).
As baterias Ni-Cd geralmente possuem uma caixa de metal com uma placa de vedação equipada com uma válvula de segurança autovedante . As placas do eletrodo positivo e negativo, isoladas uma da outra pelo separador, são enroladas em forma de espiral dentro da caixa. Isso é conhecido como design de gelatina e permite que uma célula de Ni – Cd forneça uma corrente máxima muito mais alta do que uma célula alcalina de tamanho equivalente. As células alcalinas têm uma construção de bobina onde o invólucro da célula é preenchido com eletrólito e contém uma haste de grafite que atua como o eletrodo positivo. Como uma área relativamente pequena do eletrodo está em contato com o eletrólito (em oposição ao design de gelatina), a resistência interna para uma pilha alcalina de tamanho equivalente é maior, o que limita a corrente máxima que pode ser fornecida.
As reações químicas no eletrodo de cádmio durante a descarga são:
As reações no eletrodo de óxido de níquel são:
A reação líquida durante a descarga é
Durante a recarga, as reações vão da direita para a esquerda. O eletrólito alcalino (comumente KOH) não é consumido nesta reação e, portanto, sua gravidade específica , ao contrário das baterias de chumbo-ácido, não é um guia para seu estado de carga.
Quando Jungner construiu as primeiras baterias de Ni-Cd, ele usou óxido de níquel no eletrodo positivo e materiais de ferro e cádmio no negativo. Só mais tarde é que o cádmio metálico puro e o hidróxido de níquel foram usados. Até cerca de 1960, a reação química não era completamente compreendida. Houve várias especulações quanto aos produtos da reação. O debate foi finalmente resolvido por espectroscopia de infravermelho , que revelou hidróxido de cádmio e hidróxido de níquel.
Outra variação historicamente importante na célula básica de Ni-Cd é a adição de hidróxido de lítio ao eletrólito de hidróxido de potássio. Acreditava-se que isso prolongava a vida útil, tornando a célula mais resistente ao abuso elétrico. A bateria Ni – Cd em sua forma moderna é extremamente resistente ao abuso elétrico de qualquer maneira, então essa prática foi descontinuada.
Baterias de células ventiladas
Baterias de NiCd de célula ventilada ( célula úmida , célula inundada ) são usadas quando grandes capacidades e altas taxas de descarga são necessárias. As baterias de NiCd tradicionais são do tipo selado, o que significa que o gás de carga é normalmente recombinado e não liberam gás, a menos que sejam fortemente sobrecarregadas ou que ocorra uma falha. Ao contrário das células NiCd típicas, que são seladas, as células ventiladas têm um respiradouro ou válvula de liberação de baixa pressão que libera todos os gases de oxigênio e hidrogênio gerados quando sobrecarregados ou descarregados rapidamente. Por não ser um vaso de pressão , a bateria é mais segura, pesa menos e possui uma estrutura mais simples e econômica. Isso também significa que a bateria normalmente não é danificada por taxas excessivas de sobrecarga, descarga ou mesmo carga negativa.
Eles são usados na aviação, transporte ferroviário e de massa, energia reserva para telecomunicações, partida do motor para turbinas reserva, etc. O uso de baterias NiCd de célula ventilada resulta na redução do tamanho, peso e requisitos de manutenção em relação a outros tipos de baterias. As baterias de NiCd de célula ventilada têm vida longa (até 20 anos ou mais, dependendo do tipo) e operam em temperaturas extremas (de −40 a 70 ° C).
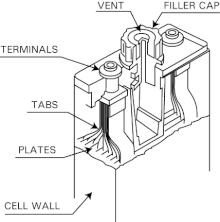
Uma caixa de bateria de aço contém as células conectadas em série para obter a tensão desejada (1,2 V por célula nominal). As células são geralmente feitas de uma poliamida ( náilon ) leve e durável , com várias placas de níquel-cádmio soldadas para cada eletrodo interno. Um separador ou revestimento feito de borracha de silicone atua como um isolante e uma barreira de gás entre os eletrodos. As células são inundadas com um eletrólito de solução aquosa de hidróxido de potássio ( KOH ) a 30% . A gravidade específica do eletrólito não indica se a bateria está descarregada ou totalmente carregada, mas muda principalmente com a evaporação da água. A parte superior da célula contém um espaço para o excesso de eletrólito e uma abertura de liberação de pressão. Grandes pinos de cobre banhados a níquel e grossos links de interconexão garantem resistência mínima em série equivalente para a bateria.
A descarga de gases significa que a bateria está sendo descarregada a uma taxa elevada ou recarregada a uma taxa superior à nominal. Isso também significa que o eletrólito perdido durante a ventilação deve ser substituído periodicamente por meio de manutenção de rotina. Dependendo dos ciclos de carga / descarga e do tipo de bateria, isso pode significar um período de manutenção de alguns meses a um ano.
A tensão da célula ventilada aumenta rapidamente no final da carga, permitindo o uso de um circuito de carregador muito simples. Normalmente, uma bateria é carregada com corrente constante a uma taxa de 1 CA até que todas as células tenham atingido pelo menos 1,55 V. Outro ciclo de carga segue a taxa de 0,1 CA, novamente até que todas as células tenham atingido 1,55 V. A carga é finalizada com uma equalização ou top- carga adicional, normalmente por não menos de 4 horas a uma taxa de 0,1 CA. O objetivo da sobrecarga é expelir o máximo (senão todos) dos gases coletados nos eletrodos, hidrogênio no negativo e oxigênio no positivo, e alguns desses gases se recombinam para formar água que, por sua vez, aumentará o nível de eletrólito ao seu nível mais alto, após o qual é seguro ajustar os níveis de eletrólito. Durante a sobrecarga ou carga complementar, as tensões da célula irão além de 1,6 V e então começarão a cair lentamente. Nenhuma célula deve subir acima de 1,71 V (célula seca) ou cair abaixo de 1,55 V (barreira de gás quebrada).
Em uma instalação de aeronave com um sistema elétrico de bateria flutuante, a tensão do regulador é configurada para carregar a bateria com carga potencial constante (normalmente 14 ou 28 V). Se esta tensão for ajustada muito alta, isso resultará em rápida perda de eletrólito. Um regulador de carga com falha pode permitir que a tensão de carga aumente bem acima desse valor, causando uma sobrecarga massiva com ebulição do eletrólito.
Formulários
As células seladas de Ni – Cd podem ser usadas individualmente ou montadas em conjuntos de baterias contendo duas ou mais células. As células pequenas são usadas para eletrônicos portáteis e brinquedos (como lâmpadas solares de jardim), geralmente usando células fabricadas nos mesmos tamanhos das células primárias . Quando as baterias Ni – Cd são substituídas por células primárias, a tensão terminal mais baixa e a capacidade de ampere-hora menor podem reduzir o desempenho em comparação com as células primárias. Células-botão em miniatura são às vezes usadas em equipamentos fotográficos, lâmpadas portáteis (lanterna ou tocha), standby de memória de computador, brinquedos e novidades.
Baterias Ni – Cd especiais são usadas em telefones sem fio e sem fio, iluminação de emergência e outras aplicações. Com uma resistência interna relativamente baixa , eles podem fornecer altas correntes de surto . Isso os torna uma escolha favorável para aeromodelos elétricos controlados remotamente, barcos e carros, bem como ferramentas elétricas sem fio e unidades de flash de câmera.
Células inundadas maiores são usadas para baterias de partida de aeronaves , veículos elétricos e energia de reserva .
Popularidade
Os avanços nas tecnologias de fabricação de baterias ao longo da segunda metade do século XX tornaram a produção de baterias cada vez mais barata. Dispositivos alimentados por bateria em geral têm crescido em popularidade. Em 2000, cerca de 1,5 bilhão de baterias de Ni – Cd eram produzidas anualmente. Até meados da década de 1990, as baterias de Ni – Cd detinham a esmagadora maioria da participação de mercado de baterias recarregáveis em eletrônicos domésticos.
A certa altura, as baterias de Ni – Cd representaram 8% de todas as vendas de baterias secundárias (recarregáveis) portáteis na UE, e no Reino Unido por 9,2% (descarte) e na Suíça por 1,3% de todas as vendas de baterias portáteis.
Na UE, a Diretiva de Baterias de 2006 restringiu as vendas de baterias de Ni – Cd a consumidores para dispositivos portáteis.
Disponibilidade
As células Ni – Cd estão disponíveis nos mesmos tamanhos das baterias alcalinas , de AAA a D, bem como em vários tamanhos de várias células, incluindo o equivalente a uma bateria de 9 volts. Uma única célula de Ni – Cd totalmente carregada, sem carga, carrega uma diferença de potencial entre 1,25 e 1,35 volts, que permanece relativamente constante enquanto a bateria é descarregada. Como uma bateria alcalina quase totalmente descarregada pode ter sua queda de voltagem tão baixa quanto 0,9 volts, as células Ni – Cd e as pilhas alcalinas são normalmente intercambiáveis para a maioria das aplicações.
Além das células individuais, existem baterias que contêm até 300 células (nominalmente 360 volts, tensão real sem carga entre 380 e 420 volts). Muitas células são usadas principalmente em aplicações automotivas e industriais de serviço pesado. Para aplicações portáteis, o número de células é normalmente inferior a 18 células (24 V). Baterias inundadas de tamanho industrial estão disponíveis com capacidades que variam de 12,5 Ah a várias centenas de Ah.
Comparação com outras baterias
Recentemente, as baterias de níquel-hidreto metálico e de íon-lítio tornaram-se disponíveis comercialmente e mais baratas, o primeiro tipo agora rivaliza com as baterias de Ni-Cd em custo. Onde a densidade de energia é importante, as baterias de Ni – Cd estão agora em desvantagem em comparação com as baterias de níquel-hidreto metálico e íons de lítio. No entanto, a bateria Ni – Cd ainda é muito útil em aplicações que requerem taxas de descarga muito altas porque ela pode suportar tal descarga sem danos ou perda de capacidade.
Quando comparada a outras formas de bateria recarregável, a bateria Ni – Cd tem uma série de vantagens distintas:
- As baterias são mais difíceis de danificar do que outras baterias, tolerando descarga profunda por longos períodos. Na verdade, as baterias de Ni – Cd em armazenamento de longo prazo são normalmente armazenadas totalmente descarregadas. Isso é diferente, por exemplo, das baterias de íon de lítio , que são menos estáveis e serão permanentemente danificadas se descarregadas abaixo de uma tensão mínima.
- A bateria funciona muito bem em condições adversas, perfeita para uso em ferramentas portáteis.
- As baterias Ni – Cd normalmente duram mais, em termos de número de ciclos de carga / descarga, do que outras baterias recarregáveis, como baterias de chumbo / ácido.
- Em comparação com as baterias de chumbo-ácido , as baterias de Ni-Cd têm uma densidade de energia muito maior . Uma bateria Ni – Cd é menor e mais leve do que uma bateria de chumbo-ácido comparável, mas não uma bateria NiMH ou Li-ion comparável. Nos casos em que o tamanho e o peso são considerações importantes (por exemplo, aeronave), as baterias de Ni – Cd são preferidas às baterias de chumbo-ácido mais baratas.
- Em aplicações de consumo, as baterias Ni – Cd competem diretamente com as baterias alcalinas . Uma célula Ni – Cd tem uma capacidade menor do que uma célula alcalina equivalente e custa mais. No entanto, como a reação química da bateria alcalina não é reversível, uma bateria de Ni – Cd reutilizável tem uma vida útil total significativamente maior. Houve tentativas de criar baterias alcalinas recarregáveis ou carregadores de bateria especializados para carregar baterias alcalinas de uso único, mas nenhum que tenha sido amplamente utilizado.
- A tensão terminal de uma bateria Ni – Cd diminui mais lentamente à medida que é descarregada, em comparação com as baterias de carbono-zinco. Como a voltagem de uma bateria alcalina cai significativamente conforme a carga cai, a maioria dos aplicativos de consumo são bem equipados para lidar com a voltagem da célula Ni – Cd ligeiramente mais baixa sem perda perceptível de desempenho.
- A capacidade de uma bateria Ni – Cd não é significativamente afetada por correntes de descarga muito altas. Mesmo com taxas de descarga de até 50C, uma bateria Ni – Cd fornecerá quase sua capacidade nominal. Em contraste, uma bateria de chumbo-ácido fornecerá apenas cerca de metade de sua capacidade nominal quando descarregada a uma temperatura relativamente modesta de 1,5 ° C.
- O dreno máximo de corrente contínua da bateria NiCd é comumente em torno de 15C. Em comparação com a bateria NiMH, onde o consumo máximo de corrente contínua utilizável não é superior a 5C.
- As baterias de níquel- hidreto metálico ( NiMH ) são as mais novas e mais semelhantes concorrentes das baterias de Ni-Cd. Em comparação com as baterias Ni – Cd, as baterias NiMH têm uma capacidade maior e são menos tóxicas, e agora são mais econômicas. No entanto, uma bateria Ni – Cd tem uma taxa de autodescarga mais baixa (por exemplo, 20% por mês para uma bateria Ni – Cd, contra 30% por mês para uma NiMH tradicional em condições idênticas), embora baixa autodescarga (" LSD ") As baterias NiMH estão agora disponíveis, com autodescarga substancialmente mais baixa do que as baterias Ni – Cd ou NiMH tradicionais. Isso resulta em uma preferência por baterias Ni – Cd em vez de baterias NiMH não LSD em aplicações onde o consumo de corrente da bateria é menor do que a própria taxa de autodescarga da bateria (por exemplo, controles remotos de televisão). Em ambos os tipos de célula, a taxa de autodescarga é mais alta para um estado de carga total e cai um pouco para estados de carga mais baixos. Finalmente, uma bateria de Ni – Cd de tamanho semelhante tem uma resistência interna ligeiramente menor e, portanto, pode atingir uma taxa de descarga máxima mais alta (o que pode ser importante para aplicações como ferramentas elétricas).
A principal desvantagem com as baterias Ni – Cd é seu custo mais alto e o uso de cádmio. Este metal pesado é um perigo ambiental e é altamente tóxico para todas as formas de vida superiores. Eles também são mais caros do que as baterias de chumbo-ácido porque o níquel e o cádmio custam mais. Uma das maiores desvantagens é que a bateria exibe um coeficiente de temperatura negativo muito acentuado. Isso significa que, conforme a temperatura da célula aumenta, a resistência interna diminui. Isso pode representar problemas consideráveis de carga, particularmente com os sistemas de carga relativamente simples empregados para baterias do tipo ácido-chumbo . Enquanto as baterias de chumbo-ácido podem ser carregadas simplesmente conectando um dínamo a elas, com um sistema de corte eletromagnético simples para quando o dínamo está estacionário ou ocorre uma sobrecarga de corrente, a bateria de Ni-Cd sob um esquema de carregamento semelhante exibiria descontrolado, onde a corrente de carga continuaria a aumentar até que o corte de sobrecorrente operasse ou a bateria se destruísse. Este é o principal fator que impede seu uso como baterias de partida do motor. Hoje, com sistemas de carregamento baseados em alternador com reguladores de estado sólido, a construção de um sistema de carregamento adequado seria relativamente simples, mas os fabricantes de automóveis relutam em abandonar a tecnologia testada e comprovada.
Efeito de memória
As baterias Ni – Cd podem sofrer um " efeito memória " se forem descarregadas e recarregadas no mesmo estado de carga centenas de vezes. O sintoma aparente é que a bateria "se lembra" do ponto em seu ciclo de descarga em que a recarga começou e, durante o uso subsequente, sofre uma queda repentina de tensão naquele ponto, como se a bateria tivesse sido descarregada. A capacidade da bateria não é reduzida substancialmente. Alguns componentes eletrônicos projetados para serem alimentados por baterias de Ni – Cd são capazes de suportar essa tensão reduzida por tempo suficiente para que a tensão volte ao normal. No entanto, se o dispositivo não for capaz de operar durante esse período de tensão reduzida, ele não conseguirá obter energia suficiente da bateria e, para todos os efeitos práticos, a bateria parece "descarregada" mais cedo do que o normal.
Há evidências de que a história do efeito memória se originou de satélites em órbita, onde eles carregavam e descarregavam de forma semelhante a cada órbita ao redor da Terra por um período de vários anos. Após este tempo, verificou-se que as capacidades das baterias diminuíram significativamente, mas ainda estavam aptas para o uso. É improvável que essa cobrança repetitiva precisa (por exemplo, 1.000 cargas / descargas com menos de 2% de variabilidade) possa ser reproduzida por indivíduos que usam produtos elétricos. O artigo original que descreve o efeito de memória foi escrito por cientistas da GE em seu Departamento de Negócios de Baterias em Gainesville, Flórida, e depois retirado por eles, mas o estrago estava feito.
A bateria sobrevive a milhares de ciclos de cargas / descargas. Também é possível diminuir o efeito de memória descarregando a bateria completamente cerca de uma vez por mês. Dessa forma, aparentemente a bateria não "lembra" o ponto em seu ciclo de carga.
Um efeito com sintomas semelhantes ao efeito memória é a chamada depressão de voltagem ou efeito de bateria lenta . Isso resulta de sobrecarga repetida; o sintoma é que a bateria parece estar totalmente carregada, mas descarrega rapidamente após apenas um breve período de operação. Em casos raros, grande parte da capacidade perdida pode ser recuperada por alguns ciclos de descarga profunda, uma função geralmente fornecida por carregadores automáticos de bateria. No entanto, esse processo pode reduzir a vida útil da bateria. Se bem tratada, uma bateria Ni – Cd pode durar 1.000 ciclos ou mais antes que sua capacidade caia para menos da metade de sua capacidade original. Muitos carregadores domésticos afirmam ser "carregadores inteligentes" que desligam e não danificam a bateria, mas este parece ser um problema comum.
Impacto ambiental
As baterias Ni – Cd contêm entre 6% (para baterias industriais) e 18% (para baterias comerciais) de cádmio , que é um metal pesado tóxico e, portanto, requer cuidados especiais durante o descarte da bateria.
Nos Estados Unidos , o custo de reciclagem da bateria esperado (a ser usado para descarte adequado no final da vida útil do serviço) é incluído no preço de compra da bateria.
De acordo com a chamada "diretiva de baterias" (2006/66 / EC), a venda de baterias de Ni-Cd para consumidores foi agora proibida na União Europeia, exceto para uso médico; sistemas de alarme; luz de emergência; e ferramentas elétricas portáteis. Esta última categoria foi banida a partir de 2016. De acordo com a mesma diretiva da UE, as baterias industriais de Ni – Cd usadas devem ser coletadas por seus produtores para serem recicladas em instalações dedicadas.
Veja também
- Reciclagem de bateria
- Comparação de tipos de bateria
- Lista de tamanhos de bateria
- Lista de tipos de bateria
- Relação potência-peso
Referências
Leitura adicional
- Bergstrom, Sven. "Baterias de níquel-cádmio - tipo de bolso". Journal of the Electrochemical Society, setembro de 1952. 1952 The Electrochemical Society.
- Ellis, GB, Mandel, H. e Linden, D. "Sintered Plate Nickel – Cadmium Batteries". Journal of the Electrochemical Society , The Electrochemical Society, setembro de 1952.
- General Electric, "Nickel-Cadmium Battery Application Engineering Handbook", 1971
- Marathon Battery Company, "Care and Maintenance of Nickel-Cadmium Batteries"
- SAFT, "NiCd Aircraft Batteries, Operating and Maintenance Manual (OMM)", 2002
links externos
- "Bateria de níquel-cádmio dura tanto quanto o carro." Popular Science , agosto de 1948, pp. 113-118.
- Baterias Ni – Cd para Aeronaves, Manual de Operação e Manutenção (PDF)
- A história das baterias de níquel-cádmio Alcad em Redditch 1918-1993