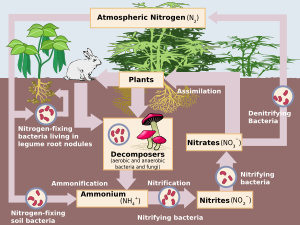
Nitrificação - Nitrification
A nitrificação é a oxidação biológicada amônia em nitrito seguida pela oxidação do nitrito em nitrato ocorrendo através de organismos separados ou oxidação direta da amônia em nitrato embactérias comammox . A transformação da amônia em nitrito é geralmente a etapa limitante da taxa de nitrificação. A nitrificação é uma etapa importante no ciclo do nitrogênio no solo . A nitrificação é umprocesso aeróbio realizado por pequenos grupos de bactérias autotróficas e arquéias .
Microbiologia
Oxidação de amônia
A oxidação da amônia em nitrito é realizada por dois grupos de organismos, bactérias oxidantes de amônia ( AOB ) e arquéias oxidantes de amônia ( AOA ). AOB pode ser encontrado entre Betaproteobacteria e Gammaproteobacteria . Desde a descoberta de AOA em 2005, dois isolados foram cultivados: Nitrosopumilus maritimus e Nitrososphaera viennensis . Em solos as MAA mais estudadas pertencem aos gêneros Nitrosomonas e Nitrococcus . Ao comparar AOB e AOA, AOA domina em ambos os solos e ambientes marinhos, sugerindo que Thaumarchaeota pode ser maior contribuinte para a oxidação de amônia nesses ambientes.
Oxidação de nitrito
A segunda etapa - a oxidação do nitrito em nitrato - é feita por bactérias (bactérias oxidantes de nitrito, NOB ) dos táxons Nitrospirae , Nitrospinae , Proteobacteria e Chloroflexi . Eles estão presentes no solo, nas nascentes geotérmicas, nos ecossistemas de água doce e marinhos.
Oxidação completa de amônia
A oxidação da amônia a nitrato em uma única etapa dentro de um organismo foi prevista em 2006 e descoberta em 2015 na espécie Nitrospira inopinata . Uma cultura pura do organismo foi obtida em 2017, representando uma revolução na nossa compreensão do processo de nitrificação.
História
A ideia de que a oxidação da amônia a nitrato é de fato um processo biológico foi dada pela primeira vez por Louis Pasteur em 1862. Mais tarde, em 1875, Alexander Müller, durante a avaliação da qualidade da água de poços em Berlim, observou que a amônia era estável em soluções esterilizadas, mas nitrificada em águas naturais . A. Müller afirmou que a nitrificação é assim realizada por microrganismos. Em 1877, Jean-Jacques Schloesing e Achille Müntz , dois químicos agrícolas franceses trabalhando em Paris , provaram que a nitrificação é de fato um processo mediado por micróbios pelos experimentos com esgoto líquido e matriz artificial de solo (areia esterilizada com giz). Suas descobertas foram confirmadas logo (em 1878) por Robert Warington, que estava investigando a capacidade de nitrificação do solo do jardim na estação experimental de Rothamsted em Harpenden, na Inglaterra. R. Warington também fez a primeira observação de que a nitrificação é um processo de duas etapas em 1879, que foi confirmado por John Munro em 1886. Embora naquela época, se acreditasse que a nitrificação de duas etapas é separada em diferentes fases da vida ou traços de caráter de um único microorganismo.
O primeiro nitrificador puro (oxidante da amônia) foi provavelmente isolado em 1890 por Percy Frankland e Grace Frankland , dois cientistas ingleses da Escócia. Antes disso, Warington , Sergei Winogradsky e os Frankland's conseguiam estabelecer apenas culturas de enriquecimento nitrificante e não puras. Frankland e Frankland tiveram sucesso com um sistema de diluições em série com inóculo muito baixo e tempos de cultivo longos contados em anos. Sergei Winogradsky alegou isolamento de cultura puro no mesmo ano (1890), mas sua cultura ainda era uma co-cultura de bactérias oxidantes de amônia e nitrito. S. Winogradsky foi bem-sucedido apenas um ano depois, em 1891.
De fato, durante as diluições em série, oxidantes de amônia e oxidantes de nitrito foram separados sem saber, resultando em cultura pura com capacidade de oxidação de amônia apenas. Assim, Frankland e Frankland observaram que essas culturas puras perdem a capacidade de realizar as duas etapas. A perda da capacidade de oxidação do nitrito já foi observada por R. Warington . O cultivo do oxidante de nitrito puro aconteceu mais tarde durante o século 20, no entanto, não é possível ter certeza de quais culturas estavam sem contaminantes, pois todas as cepas teoricamente puras compartilham a mesma característica (consumo de nitrito, produção de nitrato).
Ecologia
Ambas as etapas estão produzindo energia para ser acoplada à síntese de ATP. Os organismos nitrificantes são quimioautótrofos e usam dióxido de carbono como sua fonte de carbono para o crescimento. Alguns AOB possuem a enzima urease , que catalisa a conversão da molécula de ureia em duas moléculas de amônia e uma molécula de dióxido de carbono. Nitrosomonas europaea , bem como populações de AOB que vivem no solo, demonstraram assimilar o dióxido de carbono liberado pela reação para fazer biomassa por meio do Ciclo de Calvin e coletar energia oxidando amônia (o outro produto da urease) em nitrito. Esta característica pode explicar o aumento do crescimento de AOB na presença de uréia em ambientes ácidos.
Na maioria dos ambientes, estão presentes organismos que irão completar as duas etapas do processo, produzindo nitrato como produto final. No entanto, é possível projetar sistemas nos quais o nitrito é formado (o processo de Sharon ).
A nitrificação é importante em sistemas agrícolas, onde o fertilizante é freqüentemente aplicado como amônia. A conversão dessa amônia em nitrato aumenta a lixiviação de nitrogênio porque o nitrato é mais solúvel em água do que a amônia.
A nitrificação também desempenha um papel importante na remoção de nitrogênio das águas residuais municipais . A remoção convencional é a nitrificação, seguida de desnitrificação . O custo desse processo reside principalmente na aeração (trazendo oxigênio para o reator) e na adição de uma fonte externa de carbono (por exemplo, metanol ) para a desnitrificação.
A nitrificação também pode ocorrer na água potável. Em sistemas de distribuição onde cloraminas são usadas como desinfetante secundário, a presença de amônia livre pode atuar como substrato para microorganismos oxidantes de amônia. As reações associadas podem levar ao esgotamento do desinfetante residual no sistema. A adição de íon clorito à água tratada com cloramina demonstrou controlar a nitrificação.
Junto com a amonificação , a nitrificação forma um processo de mineralização que se refere à decomposição completa da matéria orgânica, com a liberação dos compostos de nitrogênio disponíveis. Isso reabastece o ciclo do nitrogênio .
Química e Enzimologia
A nitrificação é um processo de oxidação de compostos de nitrogênio (efetivamente, perda de elétrons do átomo de nitrogênio para os átomos de oxigênio ) e é catalisada passo a passo por uma série de enzimas.
- ( Nitrosomonas , Comammox )
- ( Nitrobacter , Nitrospira , Comammox )
OU
Em Nitrosomonas europaea , a primeira etapa de oxidação (amônia a hidroxilamina ) é realizada pela enzima amônia monooxigenase (AMO).
A segunda etapa (hidroxilamina em nitrito) é realizada por etapas por duas enzimas diferentes. A hidroxilamina oxidoredutase (HAO), converte a hidroxilamina em óxido nítrico.
Outra enzima ainda desconhecida que converte óxido nítrico em nitrito.
A terceira etapa (nitrito em nitrato) é concluída em um organismo diferente.
Nitrificação no meio marinho
No ambiente marinho , o nitrogênio costuma ser o nutriente limitante , portanto, o ciclo do nitrogênio no oceano é de particular interesse. A etapa de nitrificação do ciclo é de particular interesse no oceano porque cria nitrato , a forma primária de nitrogênio responsável pela "nova" produção . Além disso, à medida que o oceano se torna enriquecido em CO 2 antropogênico , a diminuição resultante no pH pode levar a taxas decrescentes de nitrificação. A nitrificação pode potencialmente se tornar um "gargalo" no ciclo do nitrogênio.
A nitrificação, conforme declarado acima, é formalmente um processo de duas etapas; na primeira etapa, a amônia é oxidada em nitrito e, na segunda etapa, o nitrito é oxidado em nitrato. Diferentes micróbios são responsáveis por cada etapa do ambiente marinho. Vários grupos de bactérias oxidantes de amônia (AOB) são conhecidos no ambiente marinho, incluindo Nitrosomonas , Nitrospira e Nitrosococcus . Todos contêm o gene funcional monooxigenase de amônia ( AMO ) que, como o próprio nome indica, é responsável pela oxidação da amônia. Estudos metagenômicos mais recentes e abordagens de cultivo revelaram que alguns Thaumarchaeota (anteriormente Crenarchaeota) possuem AMO. Thaumarchaeotes são abundantes no oceano e algumas espécies têm uma afinidade 200 vezes maior com a amônia do que AOB, levando os pesquisadores a desafiar a crença anterior de que os AOB são os principais responsáveis pela nitrificação no oceano. Além disso, embora a nitrificação seja classicamente considerada verticalmente separada da produção primária porque a oxidação do nitrato por bactérias é inibida pela luz, a nitrificação por AOA não parece ser inibida pela luz, o que significa que a nitrificação está ocorrendo em toda a coluna de água , desafiando o clássico definições de produção "nova" e "reciclada" .
Na segunda etapa, o nitrito é oxidado a nitrato. Nos oceanos, esta etapa não é tão bem entendida quanto a primeira, mas as bactérias Nitrospina e Nitrobacter são conhecidas por realizar esta etapa no oceano.
Condições do solo que controlam as taxas de nitrificação
- Disponibilidade de substrato (presença de NH 4 + )
- Aeração (disponibilidade de O 2 )
- Solos bem drenados com 60% de umidade do solo
- pH (quase neutro)
- Temperatura (melhor 20-30 ° C) => A nitrificação é sazonal, afetada pelas práticas de uso da terra
Inibidores de nitrificação
Os inibidores de nitrificação são compostos químicos que retardam a nitrificação de fertilizantes com amônia , amônia ou ureia , que são aplicados ao solo como fertilizantes. Esses inibidores podem ajudar a reduzir as perdas de nitrogênio no solo que, de outra forma, seriam usados pelas plantações. Os inibidores de nitrificação são amplamente utilizados, sendo adicionados a aproximadamente 50% da amônia anidra aplicada em queda nos estados dos EUA, como Illinois. Eles são geralmente eficazes para aumentar a recuperação de fertilizantes de nitrogênio em plantações em linha, mas o nível de eficácia depende das condições externas e seus benefícios são mais prováveis de serem observados com taxas de nitrogênio abaixo do ideal.
As preocupações ambientais da nitrificação também contribuem para o interesse no uso de inibidores de nitrificação: o produto principal, nitrato , lixivia para as águas subterrâneas, produzindo toxicidade aguda em várias espécies de vida selvagem e contribuindo para a eutrofização das águas paradas. Alguns inibidores da nitrificação também inibem a produção de metano , um gás de efeito estufa.
A inibição do processo de nitrificação é facilitada principalmente pela seleção e inibição / destruição das bactérias que oxidam compostos de amônia. Uma infinidade de compostos que inibem a nitrificação, que podem ser divididos nas seguintes áreas: o sítio ativo da monooxigenase de amônia (AMO), inibidores mecanísticos e o processo de compostos N- heterocíclicos . O processo para o último dos três ainda não é amplamente compreendido, mas é proeminente. A presença de AMO foi confirmada em muitos substratos que são inibidores de nitrogênio, como dicianodiamida , tiossulfato de amônio e nitrapirina .
A conversão da amônia em hidroxilamina é a primeira etapa da nitrificação, onde o AH 2 representa uma gama de potenciais doadores de elétrons.
- NH 3 + AH 2 + O 2 → NH 2 OH + A + H 2 O
Esta reação é catalisada por AMO. Os inibidores desta reação ligam-se ao sítio ativo no AMO e previnem ou atrasam o processo. O processo de oxidação da amônia pelo AMO é considerado importante devido ao fato de que outros processos requerem a co-oxidação do NH 3 para o fornecimento de equivalentes redutores. Isso geralmente é fornecido pelo composto hidroxilamina oxidoredutase (HAO) que catalisa a reação:
- NH 2 OH + H 2 O → NO 2 - + 5 H + + 4 e -
O mecanismo de inibição é complicado por este requisito. A análise cinética da inibição da oxidação de NH 3 mostrou que os substratos de AMO apresentaram cinética variando de competitiva a não competitiva . A ligação e a oxidação podem ocorrer em dois locais diferentes no AMO: em substratos competitivos, a ligação e a oxidação ocorrem no local NH 3 , enquanto em substratos não competitivos ocorre em outro local.
Os inibidores baseados em mecanismo podem ser definidos como compostos que interrompem a reação normal catalisada por uma enzima. Este método ocorre pela inativação da enzima via modificação covalente do produto, que acaba por inibir a nitrificação. Por meio do processo, o AMO é desativado e uma ou mais proteínas são ligadas covalentemente ao produto final. Isso é mais proeminente em uma ampla gama de compostos de enxofre ou acetilênicos .
Compostos contendo enxofre, incluindo tiossulfato de amônio (um inibidor popular) operam produzindo compostos voláteis com fortes efeitos inibitórios, como dissulfeto de carbono e tioureia .
Em particular, a tiofosforil triamida tem sido uma adição notável onde tem o duplo propósito de inibir a produção de urease e nitrificação. Em um estudo dos efeitos inibitórios da oxidação pela bactéria Nitrosomonas europaea , o uso de tioéteres resultou na oxidação desses compostos a sulfóxidos , onde o átomo S é o principal local de oxidação por AMO. Isso está mais fortemente correlacionado ao campo da inibição competitiva.
Os compostos N-heterocíclicos também são inibidores de nitrificação altamente eficazes e são frequentemente classificados por sua estrutura de anel. O modo de ação para esses compostos não é bem compreendido: enquanto a nitrapirina, um inibidor e substrato de AMO amplamente utilizado, é um inibidor baseado no mecanismo fraco da referida enzima, os efeitos do referido mecanismo são incapazes de se correlacionar diretamente com a capacidade do composto de inibir a nitrificação. Sugere-se que a nitrapirina atue contra a enzima monooxigenase dentro da bactéria, impedindo o crescimento e a oxidação de CH 4 / NH 4 . Os compostos contendo dois ou três átomos de N no anel adjacentes ( piridazina , pirazol , indazol ) tendem a ter um efeito de inibição significativamente maior do que os compostos contendo átomos de N não adjacentes ou átomos de N no anel singulares ( piridina , pirrole ). Isso sugere que a presença de átomos de N no anel está diretamente correlacionada com o efeito de inibição dessa classe de compostos.
Inibição de metano
Alguns inibidores da nitrificação enzimática, como a urease, também podem inibir a produção de metano em bactérias metanotróficas . AMO mostra taxas de renovação cinética semelhantes à metano monooxigenase (MMO) encontrada em metanotróficos, indicando que MMO é um catalisador semelhante ao AMO para o propósito de oxidação do metano. Além disso, as bactérias metanotróficas compartilham muitas semelhanças com o NH
3oxidantes como Nitrosomonas . O perfil do inibidor de formas particuladas de MMO (pMMO) mostra similaridade com o perfil de AMO, levando à similaridade nas propriedades entre MMO em metanotróficos e AMO em autótrofos .
Preocupações ambientais

Os inibidores de nitrificação também são de interesse do ponto de vista ambiental por causa da produção de nitratos e óxido nitroso a partir do processo de nitrificação. O óxido nitroso (N 2 O), embora sua concentração atmosférica seja muito inferior à do CO 2, tem potencial de aquecimento global cerca de 300 vezes maior que o dióxido de carbono e contribui com 6% do aquecimento planetário devido aos gases de efeito estufa. Este composto também é notável por catalisar a quebra do ozônio na estratosfera . Os nitratos, um composto tóxico para a vida selvagem e pecuária e um produto da nitrificação, também são motivo de preocupação.
O solo, consistindo de argilas polianiônicas e silicatos , geralmente tem uma carga aniônica líquida. Conseqüentemente, o amônio (NH 4 + ) se liga fortemente ao solo, mas os íons nitrato (NO 3 - ) não. Porque nitrato é mais móvel, ele rouba em fontes de águas subterrâneas através de escoamento agrícola . Os nitratos nas águas subterrâneas podem afetar as concentrações das águas superficiais, seja por meio de interações diretas entre as águas subterrâneas e superficiais (por exemplo, ganhando alcance de fluxo, nascentes) ou de quando são extraídos para uso na superfície. Por exemplo, grande parte da água potável nos Estados Unidos vem de águas subterrâneas, mas a maioria das estações de tratamento de águas residuais descarrega em águas superficiais.
Animais selvagens como anfíbios, peixes de água doce e insetos são sensíveis aos níveis de nitrato e são conhecidos por causar morte e anomalias de desenvolvimento nas espécies afetadas. Os níveis de nitrato também contribuem para a eutrofização , um processo no qual grandes proliferações de algas reduzem os níveis de oxigênio em corpos d'água e levam à morte de criaturas que consomem oxigênio devido à anóxia. Acredita-se que a nitrificação também contribua para a formação de smog fotoquímico , ozônio ao nível do solo, chuva ácida , mudanças na diversidade de espécies e outros processos indesejáveis. Além disso, os inibidores de nitrificação também demonstraram suprimir a oxidação do metano (CH 4 ), um potente gás de efeito estufa , a CO 2 . Tanto a nitrapirina quanto o acetileno são supressores especialmente fortes de ambos os processos, embora os modos de ação que os distinguem não sejam claros.
Veja também
- razão f
- Processo de Haber
- Bactéria nitrificadora
- Fixação de nitrogênio
- Nitrificação-desnitrificação simultânea
- Comammox
Referências
links externos
- Nitrificação no centro da filtragem em fishdoc.co.uk
- Nitrificação na Universidade de Aberdeen · King's College
- Nitrificação Básica para Operadores de Lagoas Aeradas em lagoonsonline.com