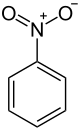
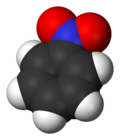
Nitrobenzeno - Nitrobenzene
|
|
|||

|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Nitrobenzeno |
|||
| Outros nomes
Óleo de nitrobenzol de mirbane |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100,002,469 |
||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 6 H 5 NO 2 | |||
| Massa molar | 123,11 g / mol | ||
| Aparência | líquido amarelado e oleoso | ||
| Odor | picante, como pasta de graxa de sapato | ||
| Densidade | 1,199 g / cm 3 | ||
| Ponto de fusão | 5,7 ° C (42,3 ° F; 278,8 K) | ||
| Ponto de ebulição | 210,9 ° C (411,6 ° F; 484,0 K) | ||
| 0,19 g / 100 ml a 20 ° C | |||
| Pressão de vapor | 0,3 mmHg (25 ° C) | ||
| -61,80 · 10 −6 cm 3 / mol | |||
| Viscosidade | 1,8112 mPa · s | ||
| Perigos | |||
|
|
|||
| Frases R (desatualizado) |
R10 , R23 / 24/25 , R40 , R48 / 23/24 , R51 / 53 , R62 |
||
| Frases S (desatualizado) |
(S1 / 2) , S28 , S36 / 37 , S45 , S61 |
||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | 88 ° C (190 ° F; 361 K) | ||
| 480 ° C (896 ° F; 753 K) | |||
| Limites explosivos | 1,8% -? | ||
| Dose ou concentração letal (LD, LC): | |||
|
LD 50 ( dose mediana )
|
780 mg / kg (rato, oral) 600 mg / kg (rato, oral) 590 mg / kg (camundongo, oral) |
||
|
LD Lo (o mais baixo publicado )
|
750 mg / kg (cão, oral) | ||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
TWA 1 ppm (5 mg / m 3 ) [pele] | ||
|
REL (recomendado)
|
TWA 1 ppm (5 mg / m 3 ) [pele] | ||
|
IDLH (perigo imediato)
|
200 ppm | ||
| Compostos relacionados | |||
|
Compostos relacionados
|
Cloreto de anilina benzenediazônio nitrosobenzeno |
||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
O nitrobenzeno é um composto orgânico com a fórmula química C 6 H 5 NO 2 . É um óleo amarelo pálido insolúvel em água com um odor de amêndoa . Ele congela para dar cristais amarelo-esverdeados. É produzido em grande escala a partir do benzeno como precursor da anilina . No laboratório, é ocasionalmente usado como solvente , especialmente para reagentes eletrofílicos .
Produção
O nitrobenzeno é preparado por nitração do benzeno com uma mistura de ácido sulfúrico concentrado , água e ácido nítrico . Essa mistura às vezes é chamada de "ácido misto". A produção de nitrobenzeno é um dos processos mais perigosos realizados na indústria química devido à exotermicidade da reação (Δ H = −117 kJ / mol).
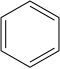 +
+ 
A capacidade mundial de nitrobenzeno em 1985 era de cerca de 1,7 × 10 6 toneladas .
O processo de nitração envolve a formação do íon nitrônio (NO 2 + ), seguido por uma reação de substituição eletrofílica aromática deste com benzeno. O íon nitrônio é gerado pela reação de ácido nítrico e um agente de desidratação ácido, normalmente ácido sulfúrico:
- HNO 3 + H + ⇌ NO 2 + + H 2 O
Usos
Aproximadamente 95% do nitrobenzeno produzido industrialmente é hidrogenado em anilina :
- C 6 H 5 NO 2 + 3 H 2 → C 6 H 5 NH 2 + 2 H 2 O
A anilina é um precursor de polímeros de uretano , produtos químicos de borracha , pesticidas , corantes (principalmente corantes azo ), explosivos e produtos farmacêuticos .
 A maior parte da anilina é consumida na produção de metilenodianilina , um precursor dos poliuretanos.
A maior parte da anilina é consumida na produção de metilenodianilina , um precursor dos poliuretanos.
Aplicações especializadas
O nitrobenzeno também é usado para mascarar odores desagradáveis em polidores de sapatos e pisos, curativos de couro, solventes de tintas e outros materiais. Redestilado, como óleo de mirbane, o nitrobenzeno tinha sido usado como um perfume barato para sabonetes . Ele foi substituído por produtos químicos menos tóxicos para essa finalidade. Um mercado comercial significativo para o nitrobenzeno é seu uso na produção do analgésico paracetamol (também conhecido como acetaminofeno) (Mannsville 1991). O nitrobenzeno também é usado nas células de Kerr , pois possui uma constante de Kerr incomumente grande . As evidências sugerem seu uso na agricultura como um estimulante de crescimento / floração de plantas.
Reações orgânicas
Além de sua conversão em anilina, o nitrobenzeno pode ser reduzido seletivamente a azoxibenzeno , azobenzeno , nitrosobenzeno , hidrazobenzeno e fenilidroxilamina . Tem sido usado como um oxidante suave em reações como a síntese de quinolina Skraup .
Segurança
O nitrobenzeno é altamente tóxico ( valor limite de 5 mg / m 3 ) e prontamente absorvido pela pele.
A exposição prolongada pode causar sérios danos ao sistema nervoso central , prejudicar a visão, causar danos ao fígado ou rins, anemia e irritação pulmonar. A inalação de vapores pode causar dor de cabeça, náusea, fadiga, tontura, cianose , fraqueza nos braços e pernas e, em casos raros, pode ser fatal. O óleo é prontamente absorvido pela pele e pode aumentar a freqüência cardíaca, causar convulsões ou raramente a morte. A ingestão pode causar dores de cabeça, tonturas, náuseas, vômitos e irritação gastrointestinal, perda de sensibilidade / uso nos membros e também pode causar sangramento interno.
O nitrobenzeno é considerado um provável carcinógeno humano pela Agência de Proteção Ambiental dos Estados Unidos e é classificado pelo IARC como um carcinógeno do Grupo 2B que é "possivelmente carcinogênico para humanos". Foi demonstrado que causa adenomas e carcinomas do fígado, rim e tireóide em ratos.
É classificado como uma substância extremamente perigosa nos Estados Unidos, conforme definido na Seção 302 do Ato de Planejamento de Emergência e Direito de Saber da Comunidade (42 USC 11002) dos EUA , e está sujeito a requisitos de relatórios rígidos pelas instalações que produzem, armazenam ou usá-lo em quantidades significativas.
Cultura popular
- O conto de 1927 The Avenging Chance, de Anthony Berkeley, discute os usos contemporâneos do nitrobenzeno. Também está no centro da trama no caso dos chocolates envenenados de Berkeley, em 1929.
- No romance policial de Nero Wolfe de 1937 , The Red Box, de Rex Stout , uma pessoa é assassinada por ter "óleo de mirbane" derramado em seu carro.