Cloreto de nitrosila - Nitrosyl chloride
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Cloreto de nitrosila
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.018.430 |
| Número EC | |
| Número E | E919 (agentes de envidraçamento, ...) |
| Malha | nitrosil + cloreto |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | 1069 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| NOCl | |
| Massa molar | 65,459 g mol −1 |
| Aparência | Gás amarelo |
| Densidade | 2,872 mg mL −1 |
| Ponto de fusão | −59,4 ° C (−74,9 ° F; 213,8 K) |
| Ponto de ebulição | −5,55 ° C (22,01 ° F; 267,60 K) |
| Reage | |
| Estrutura | |
| Diédrico, digonal | |
| Hibridação | sp 2 em N |
| 1,90 D | |
| Termoquímica | |
|
Entropia molar padrão ( S |
261,68 JK −1 mol −1 |
| 51,71 kJ mol −1 | |
| Perigos | |
| Ficha de dados de segurança | inchem.org |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Compostos relacionados
|
|
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O cloreto de nitrosila é o composto químico com a fórmula NOCl. É um gás amarelo comumente encontrado como componente da água régia , uma mistura de 3 partes de ácido clorídrico concentrado e 1 parte de ácido nítrico concentrado . É um forte eletrófilo e agente oxidante . Às vezes é chamado de reagente de Tilden.
Estrutura e síntese
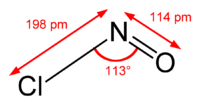
A molécula está dobrada. Existe uma ligação dupla entre N e O (distância = 1,16 Å) e uma ligação simples entre N e Cl (distância = 1,96 Å). O ângulo O = N-Cl é 113 °.
Produção
O cloreto de nitrosila pode ser produzido de várias maneiras.
- A combinação de ácido nitrosilsulfúrico e HCl proporciona o composto. Este método é usado industrialmente.
- HCl + NOHSO 4 → H 2 SO 4 + NOCl
- Um método de laboratório mais conveniente envolve a desidratação (reversível) do ácido nitroso por HCl
- HNO 2 + HCl → H 2 O + NOCl
- Pela combinação direta de cloro e óxido nítrico ; Esta reação reverte acima de 100 ° C.
- Cl 2 + 2 NO → 2 NOCl
- Por redução do dióxido de nitrogênio com cloreto de hidrogênio:
- 2NO 2 + 4 HCl → 2NOCl + 2H 2 O + Cl 2
Ocorrência na água régia
NOCl também surge da combinação de ácidos clorídrico e nítrico de acordo com a seguinte reação:
- HNO 3 + 3 HCl → 2 [Cl] + 2 H 2 O + NOCl
No ácido nítrico, o NOCl é prontamente oxidado em dióxido de nitrogênio . A presença de NOCl na água régia foi descrita por Edmund Davy em 1831.
Reações
O NOCl se comporta como um eletrófilo e um oxidante na maioria de suas reações. Com aceitadores de haleto , por exemplo , pentacloreto de antimônio , converte-se em sais de nitrosônio :
- NOCl + SbCl 5 → [NO] + [SbCl 6 ] -
Em uma reação relacionada, o ácido sulfúrico dá ácido nitrosilsulfúrico , o anidrido de ácido misto de ácido nitroso e sulfúrico:
- ClNO + H 2 SO 4 → ONHSO 4 + HCl
O NOCl reage com o tiocianato de prata para dar cloreto de prata e o pseudo - halogênio nitrosil tiocianato:
- ClNO + AgSCN → AgCl + ONSCN
Da mesma forma, ele reage com o cianeto de prata para dar cianeto de nitrosila .
O cloreto de nitrosila é usado para preparar complexos de nitrosila de metal . Com hexacarbonil de molibdênio , NOCl dá o complexo de dinitrosildicloreto:
- Mo (CO) 6 + 2 NOCl → MoCl 2 (NO) 2 + 6 CO
Ele dissolve a platina:
- Pt + 6 NOCl → (NO + ) 2 [PtCl 6 ] 2- + 4 NO
Aplicações em síntese orgânica
Além de seu papel na produção de caprolactama, o NOCl encontra alguns outros usos na síntese orgânica . Adiciona-se a alcenos para proporcionar α-cloro oximas . A adição de NOCl segue a regra de Markovnikov . Os cetenos também adicionam NOCl, dando derivados de nitrosil:
- H 2 C = C = O + NOCl → Onch 2 C (O) Cl
Os epóxidos reagem com o NOCl para dar derivados α-cloronitritoalquila. No caso do óxido de propileno, a adição prossegue com alta regioquímica:
Ele converte amidas em derivados N- nitroso. NOCl converte algumas aminas cíclicas em alcenos. Por exemplo, a aziridina reage com NOCl para dar eteno , óxido nitroso e cloreto de hidrogênio .
Aplicações industriais
NOCl e ciclohexano reagem fotoquimicamente para dar cloridrato de oxima de ciclohexanona . Este processo explora a tendência do NOCl de sofrer fotodissociação em radicais NO e Cl. O óxido é convertido em caprolactama , um precursor do Nylon-6 .
Segurança
O cloreto de nitrosila é muito tóxico e irritante para os pulmões, olhos e pele.
Referências
links externos
-
 Mídia relacionada ao cloreto de nitrosila no Wikimedia Commons
Mídia relacionada ao cloreto de nitrosila no Wikimedia Commons


